Борная кислота — ООО «Химпродукт»
- Химическая формула: h4BO3
- Плотность: 1,435 (15 °C)
- Рег. номер CAS: 10043-35-3
Бесцветное кристаллическое вещество в виде чешуек без запаха, имеет слоистую триклинную решётку, в которой молекулы кислоты соединены водородными связями в плоские слои, слои соединены между собой межмолекулярными связями (d = 0,318 нм).
При нагревании ортоборная кислота теряет воду и сначала переходит в метаборную кислоту, затем в тетраборную h3B4O7. При дальнейшем нагревании обезвоживается до борного ангидрида.
Борная кислота проявляет очень слабые кислотные свойства. Она сравнительно мало растворима в воде. Её кислотные свойства обусловлены не отщеплением протона Н+, а присоединением гидроксильного аниона.
Она легко вытесняется из растворов своих солей большинством других кислот. Соли её, называемые боратами, производятся обычно от различных полиборных кислот, чаще всего — тетраборной Н2В4О7, которая является значительно более сильной кислотой, чем ортоборная.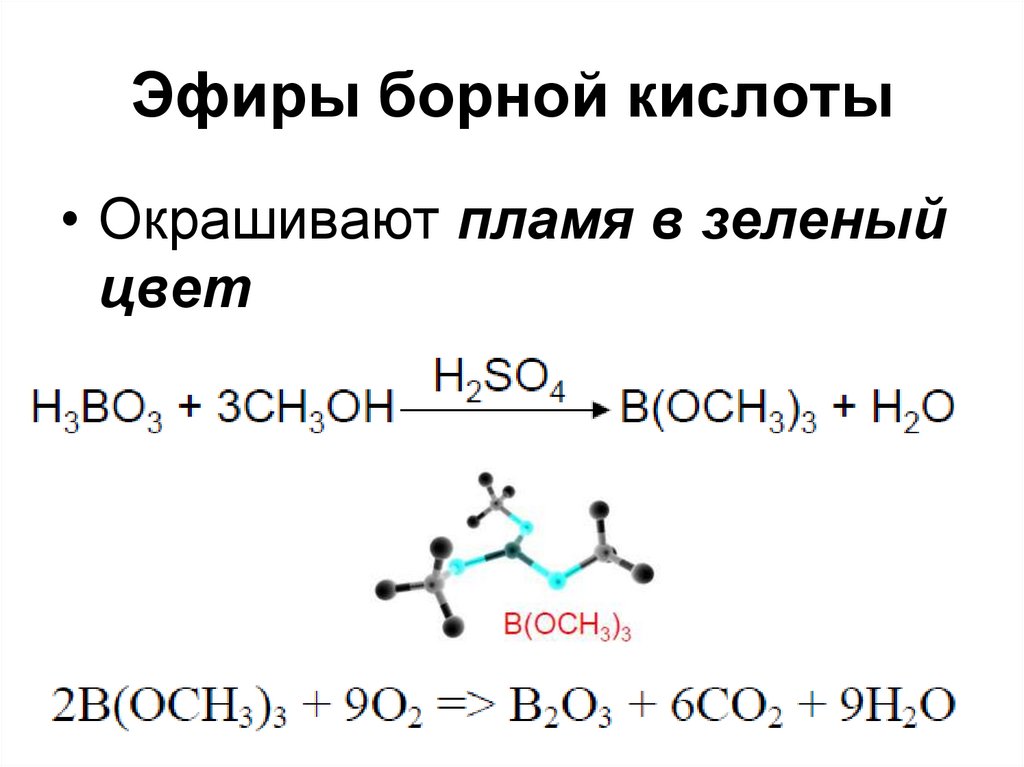
Очень слабые признаки амфотерности B(OH)3 проявляет, образуя малоустойчивый гидросульфат бора В(HSO4)3.
При нейтрализации ортоборной кислоты щелочами в водных растворах не образуются ортобораты, содержащие ион (ВО3)3−, поскольку ортобораты гидролизуются практически полностью, вследствие слишком малой константы образования. В растворе образуются тетрабораты, метабораты или соли других полиборных кислот.
Получение борной кислотыВ природе свободная борная кислота встречается в виде минерала сассолина, в горячих источниках и минеральных водах.
Борная кислота может быть получена путем смешения буры (Тетрабората натрия) с минеральной кислотой, такой как соляная кислота.
Также является продуктом гидролиза диборана или тригалогенидов бора.
Применение борной кислотыНаиболее распространённой солью борной кислоты является декагидраттетрабората натрия Na2B4O7•10h3O (техническое название — бура).
Борная кислота применяется в медицине с 60-х годов XIX века как антисептическое средство, не раздражающее ран и не имеющее вкуса, запаха и цвета. В современной медицине противомикробная эффективность борной кислоты считается низкой.
В современной медицине противомикробная эффективность борной кислоты считается низкой.
Применение борной кислоты:
- В ядерных реакторах в качестве поглотителя нейтронов, растворённого в теплоносителе.
- Борное удобрение.
- В лабораториях применяют для приготовления буферных растворов.
- В медицине — как самостоятельное дезинфицирующее средство для взрослых, а также в виде 2%-го раствора — для промывки кожи после попадания щелочей.
- Также на основе борной кислоты производятся различные комбинированные препараты (группа АТХ D08AD), например паста Теймурова.
- В фотографии — в составе мелкозернистых проявителей и кислых фиксажей для создания слабой кислотной среды.
- В ювелирном деле — как основа флюсов для пайки золотосодержащих сплавов.
- В литейном производстве — связующее при кислой футеровке печей, компонент защиты струи от окисления при разливке магниевых сплавов.
- В быту — уничтожение тараканов,муравьёв, клопов.

- В производстве керамики, оптоволокна,стекловолокна, стекла.
- В качестве антипирена для защиты древесины.
- В составе электролитов для меднения и никелирования.
Борная кислота может быть опасна только при бесконтрольном приеме внутрь. Опасная концентрация в организме человека (а особенно ребёнка) может возникнуть при регулярном применении. Смертельная доза при отравлении через рот для взрослого человека составляет 15–20 г, для детей — 4–5 г.
Хранение борной кислотыБорную кислоту упаковывают в пятислойные бумажные мешки марки НМ с полиэтиленовым вкладышем. Хранить следует в сухом помещении, без постороннего запаха.
БезопасностьОтносится к 3 классу опаснсоти по степени воздействия на организм человека. Пожаро- и взрывобезопасна.
Купить борную кислотуКомпания Химпродукт предлагает купить борную кислоту в Украине с наших складов в городах Киев, Харьков, Днепр, Одесса и Львов.
Подробную информацию, а также цену борной кислоты Вы можете узнать у наших менеджеров по телефонам:
+ 38 (098) 882–15–15 (Viber, Telegram, WhatsApp)
+ 38 (093) 880–15–15
+ 38 (066) 306–10–50
+ 38 (044) 228–08–72
либо задать вопрос на email:
Также заказать борную кислоту Вы можете на нашем сайте chem.ua
Отправка заказов по Украине осуществляется службами доставки и собственным транспортом.
Борная кислота свойства — Справочник химика 21
Константа кислотности борной кислоты настолько мала (5,8-10 ), что в обычных условиях ее нельзя титровать щелочью. Однако при взаимодействии с глицерином борная кислота образует комплекс, кислотные свойства которого значительно сильнее [c.117] Примером потенциометрического метода определения, осуществляемого с большой точностью, может служить титрование соляной кислоты в присутствии борной, так как /Сн.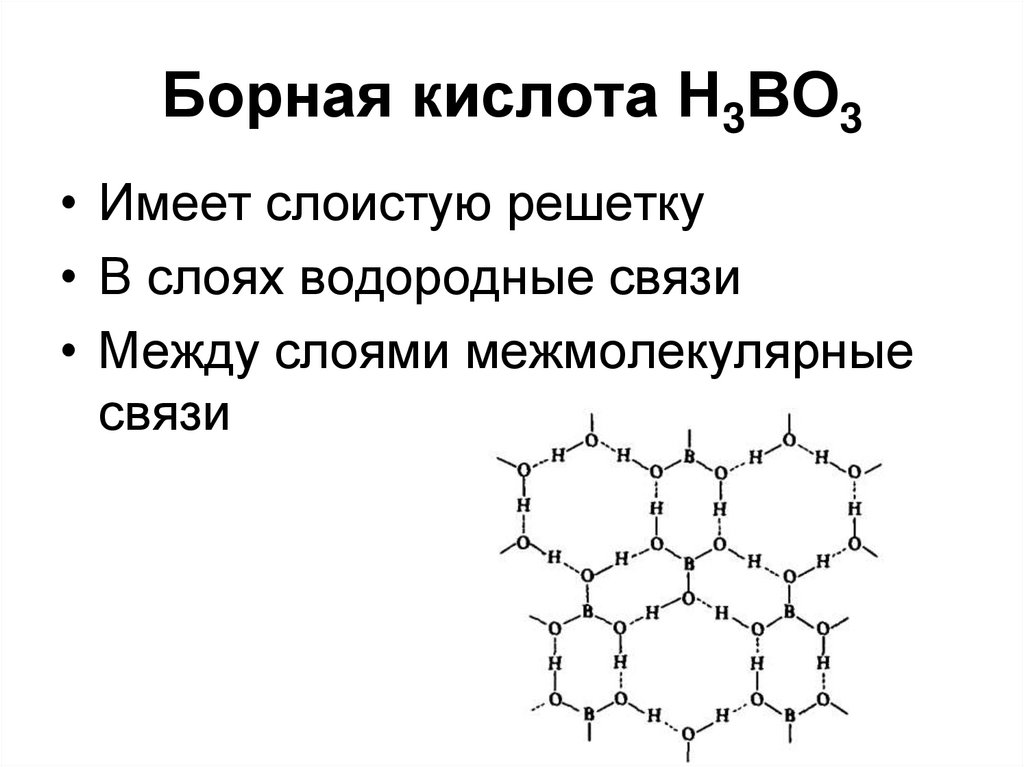 во, 10 (рК н.во, = 9,24). Борную кислоту, как известно, нельзя оттитровать кислотно-основным методом непосредственно. Однако если к раствору после завершения титрования соляной кислоты прибавить соответствующий реагент (маннит, глицерин и т. д.), усиливающий кислотные свойства борной кислоты, то ее можно определить количественно. [c.127]
во, 10 (рК н.во, = 9,24). Борную кислоту, как известно, нельзя оттитровать кислотно-основным методом непосредственно. Однако если к раствору после завершения титрования соляной кислоты прибавить соответствующий реагент (маннит, глицерин и т. д.), усиливающий кислотные свойства борной кислоты, то ее можно определить количественно. [c.127]
Борная кислота реагирует с некоторыми многоатомными спиртами, при этом образуются комплексные соединения. Эти комплексные соединения обладают свойствами кислот, с константами диссоциации значительно большими, чем константа диссоциации борной кислоты. Таким образом, при смешивании нейтральных растворов многоатомных спиртов с раствором борной кислоты диссоциация ее усиливается и становится возможным про- [c.343]
Бура и борная кислота издавна применяются в медицине как антисептики. Оксид бора (Н1) используют в производстве легкоплавких глазури и эмали, специальных сортов стекла.
С pH = 3,5—4. Подкисление раствора в этом случае вызовет только дополнительный расход кислоты. В качестве буферной добавки наилучшие результаты дает борная кислота. Многочисленные исследования заводов Южуралникеля и Норильского показали, что, несмотря на высокие буферные свойства аммония, никелевые осадки [c.339]
Ортоборная кислота Н3ВО3, или БаОз ЗН О, при 70—110°С постепенно теряет воду и превращается в метаборную кислоту НВО2 (ВаОз НаО), существующую в трех кристаллических формах с температурами плавления 176, 201 и 236 °С. При дальнейшем прокаливании образуется оксид бора В,Оз. При повышенных температурах борная дислота обладает некоторой летучестью так, при кипячении ее водных растворов она улетучивается с парами воды. Эти свойства борной кислоты предопределяют необходимость ее высушивания при невысоких температурах.
Такими свойствами обладала борная, кислота. В зону реакции ее вводили в количестве 4—5 вес. % от загрузки колонны в виде суспензии с окисляемыми углеводородами. Окисление нормальных алканов продолжалось 2—4 ч при 165—175° С. Воздух в зону реакции поступал через перфорированную пластину в количестве 500— 1000 л/ кг-ч). Изменение в широком диапазоне количества пропускаемого через реакционную массу воздуха существенно не влияло на характеристику продуктов окисления, поскольку весовая концентрация кислорода в воздухе оставалась в зоне реакции постоянной. [c.293]
Опыт 1. Борные кислоты, их получение и свойства [c.171]
Для буферных растворов используют соляную кислоту, хлорид калия, лимонную кислоту, гидрофосфат натрия, дигидрофосфат калия, борную кислоту, тетраборат натрия, гидрофталат калия, три-гидрооксалат калия (тетраоксалат), гидротартрат калия и др.
В главную подгруппу И1 группы входят алюминий, бор, галлий, индий и таллий. Положение алюминия в периодической системе хорошо согласуется с его амфотерностью. В самом деле, с одной стороны, алюминий расположен в периоде на границе между типичным металлом магнием и неметаллом кремнием. С другой стороны, алюминий в группе находится между бором и остальными элементами, для которых более характерны металлические свойства. Бор относится к неметаллам, его гидроксид Н3ВО3 (борная кислота) обладает только кислотными свойствами. Гидроксиды галлия, индия и таллия диссоциируют преимущественно по основному типу, а для таллия известен гидроксид Т10Н, который является силь-ным основанием. [c.267]
Опыт 2. Получение и исследование свойств борной кислоты [c. 60]
60]
В качестве буферной добавки в сульфатно-хлоридных электролитах широко используют борную кислоту, хотя буферные свойства таких электролитов невелики. Борная кислота проявляет максимальную буферирующую способность при pH = 9 (рК1 = 9,22), что сильно отличается от рабочего диапазона pH электролитов никелирования. Наиболее эффективными являются аминоуксусная и янтарная кислоты (20—30 г/л), в присутствии которых при рН = 3,5—4,5 и 50 °С без перемешивания электролита плотность тока на катоде можно увеличивать до 2—
Примем теперь во внимание отталкивание ядром центрального иона (лития, затем бериллия, бора и т. д.) протонов, содержащихся в гидроксильных группах. При переходе от гидроокиси лития к гидроокиси бериллия, к гидрату окиси бора и т. д. заряд ядра центрального иона возрастает, возрастает и отталкивание им протонов. Связь протонов с молекулой все более ослабляется, они получают возможность отщепляться от молекулы, т. е. появляются кислотные свойства. Основания сменяются кислотами, сила которых возрастает от борной кислоты к азотной. [c.32]
Основания сменяются кислотами, сила которых возрастает от борной кислоты к азотной. [c.32]
АНТИПИРЕНЫ — вещества, предохраняющие пропитанные ими различные органические материалы от гниения, воспламенения, разложения. Огнезащитными свойствами обладают солн, содержащие А1, ЫН4 , Са, Ь1 и др., а также кислотные радикалы (арсенат или арсенит, борат, бромид, ванадаг, вольфрамат, молибдат и т. д.). Наиболее употребительны А., содержащие соли аммония, щелочных и щелочноземельных металлов фосфорной, серной и соляной кислот (особенно сульфат и фосфат аммония), буру, борную кислоту. [c.28]
Однако при условий возрастания толщины пленок коэрцитивная сила может остаться постоянной Сильное влияиие на величину коэрцитивной силы оказывает pH раствора Особенно резко оно начинает сказываться прн переходе к растворам с рН> 8 В качестве буферных добавок используют в основном солн аммония и борную кислоту При возрастании концентрации буферных добавок магнитные свойства проходят через максимум [c. 59]
59]
Формы существования элементов этой группы мало изучены Указывалось на отсутствие связи между содержанием бора в нефтях и их удельным весом, а также содержанием асфальтосмолистых веществ. На этом основании высказано предположение о связи бора с маслами [937]. Однако более детальные исследования показали, что содернчанпе бора в маслах и асфальтенах крайне незначительно, а основная часть его концентрируется в смолах, вернее, в их омыляемых компонентах [938]. Вероятно, бор связан в нпх в виде комплексов с кислыми соединениями карбоновыми кислотами, фенолами и т. д., поскольку известно, что борные кислоты имеют свойства образовывать координационные соединения по типу [c.174]
Борную кислоту Н3ВО3, как известно, в водном растворе титровать нельзя, так как константа диссоциации ее мала (р/Са = = 9,24). Однако в присутствии некоторых органических веществ (маннита, глицерина) кислотные свойства борной кислоты усиливаются за счет образования более сильной, например боро-маннитовой кислоты [c. 133]
133]
Катализаторы позволяют увеличить выход углеродистого остатка, улучшить свойства углеграфитового волокна и уменьшить продолжительность карбонизации. В качестве каталитических добавок получения углеграфитовых волокнистых материалов применялись типичные антипирены смесь буры и диаммонийфосфата. Предлагались аммонийфосфат, смесь буры и борной кислоты, парообразные соединения железа, галогегады переходных металлов, соли сильных кислот и аммониевого основания — сульфат аммония, диаммонийфосфат, хлорид аммония. [c.64]
Второй разработкой института по улучшению качества электродов и снижению их удельного расхода стала пропитка уже графитированных заготовок или готовых электродов композициями неорганических веществ, способствующих снижению окислительного процесса при плавке. Такими свойствами обладают растворы борной кислоты, тетраборнокислого натрия, буры. Опытные партии таких электродов в отдельных случаях показывали снижение удельных расходов у потребителя до 25-30%. На основании разработанной технологии на Волгофадском металлургическом заводе Красный Октябрь в 1965 г. была сооружена полупромышленная установка по пропитке фафитированных электродов, используемых на этом заводе. Были также выпущены опытные партии таких электродов на всех электродных заводах. Но только электродное производство ЧЭМК в 1969 г. создало промышленную установку по такой пропитке. [c.125]
На основании разработанной технологии на Волгофадском металлургическом заводе Красный Октябрь в 1965 г. была сооружена полупромышленная установка по пропитке фафитированных электродов, используемых на этом заводе. Были также выпущены опытные партии таких электродов на всех электродных заводах. Но только электродное производство ЧЭМК в 1969 г. создало промышленную установку по такой пропитке. [c.125]
Катодный и анодный процессы очень чувствительны к концентрации ионов водорода, которая должна соответствовать pH 2,8—5,8. На катоде одновременно с никелем всегда выделяется водород. С уменьшением значения pH в объеме раствора (рНо) выход по току никеля падает, при повышенных значениях рНо — составляет 95—96 7о- Из-за диффузионных ограничений по ионам гидроксония значение pH в прикатодном слое (рН ) выше, чем рНо, и может достигать таких значений, при которых образуются гидроксиды и основные соли никеля. Последние включаются в катодный осадок и ухудшают его качество. Для поддержания постоянства pH и предотвращения образования гидроксида никеля в прикатодном слое в электролит никелирования вводят добавки, сообщающие ему буферные свойства, например борную кислоту. Более эффективными буферными добавками являются некоторые насыщенные дикарбоновые кислоты, такие, как янтарная кислота (СН2)г(СООН)2 или ацетат никеля N1 (СНзС00)2-4Н20. [c.38]
Для поддержания постоянства pH и предотвращения образования гидроксида никеля в прикатодном слое в электролит никелирования вводят добавки, сообщающие ему буферные свойства, например борную кислоту. Более эффективными буферными добавками являются некоторые насыщенные дикарбоновые кислоты, такие, как янтарная кислота (СН2)г(СООН)2 или ацетат никеля N1 (СНзС00)2-4Н20. [c.38]
СТЕКЛО (обыкновенное, неорганическое, силикатное) — прозрачный аморфный сплав смеси различных силикатов или силикатов с диоксидом кремния. Сырье для производства стекла должно содержать основные стеклообразующие оксиды 510а, В Оз, Р2О5 и дополнительно оксиды щелочных, щелочноземельных и других металлов. Необходимые для производства С. материалы — кварцевый песок, борная кислота, известняк, мел, сода, сульфат натрия, поташ, магнезит, каолин, оксиды свинца, сульфат или карбонат бария, полевые шпаты, битое стекло, доменные шлаки и др. Кроме того, при варке стекла вводят окислители — натриевую селитру, хлорид аммония осветлители — для удаления газов — хлорид натрия, триоксид мышьяка обесцвечивающие вещества — селен, соединения кобальта и марганца, дополняющие цвет присутствующих оксидов до белого для получения малопрозрачного матового, молочного, опалового стекла или эмалей — криолит, фторид кальция, фосфаты, соединения олова красители — соединения хрома, кадмия, селена, никеля, кобальта, золота и др. Общий состав обыкновенного С. можно выразить условно формулой N3,0-СаО X X65102. Свойства С. зависят от химического состава, условий варки и дальнейшей обработки. [c.237]
Общий состав обыкновенного С. можно выразить условно формулой N3,0-СаО X X65102. Свойства С. зависят от химического состава, условий варки и дальнейшей обработки. [c.237]
Ассортимент титруемых кислот и оснований можно расширить изменением их протолитических свойств. Так, борная кислота (р/Сд 9,24) при добавлении многоатомных спиртов (глицерин, маннит и др.) образует комплексные кислоты бора, которые вследст- [c.78]
Электрохимическим окислением алюминия в слабых электролитах (водные растворы борной кислоты и ее солей, растворы солей лимонной, янтарной, виннокаменной кислот) удается получить сплошную (непористую) тонкую (не более 1 мкм) и очень плотную оксидную пленку, обладающую достаточно высоким пробивным напряжением. Электроизоляционные свойства такого оксидного слоя обусловили применение алюминия в электролитических конденсаторах, обладаюших весьма высокой емкостью при малых размерах. Диэлектрическая проницаемость оксидной пленки, служащей диэлектриком такого конденсатора, около 10. Более перспективны танталовые конденсаторы (диэлектрическая проницаемость оксида тантала ТэгОз 27). [c.229]
Более перспективны танталовые конденсаторы (диэлектрическая проницаемость оксида тантала ТэгОз 27). [c.229]
Такое же пограничное положение занимает алюминий и в своей подгруппе. Так как в главных подгруппах с уменьшением порядкового номера элементов неметаллические свойства усиливаются, а металлические ослабевают, предшествуюш,ий алюминию в его подгруппе элемент — бор — проявляет уже только неметаллические свойства, является неметаллом. Его гидрат окиси проявляет только кислотные свойства. Это —борная кислота Н3ВО3. Элементы же, следующие за алюминием в подгруппе галлий, индий, таллий являются металлами. Эти металлы относятся к редким элементам и большого практического значения не имеют. [c.148]
Борная кислота, в отличие от других кислот, проявляет кислотные свойства за счет взаи.модействия о водой, которое приводит к образованию иона В(0Н).7. Напишите уравнение этой реакции и объясните, что является причиной ее нротеканпя. [c. 285]
285]
Бор в природе. Свойства и получение. В природе бор встречается в основном в виде борной кислоты НзВОз и солей борных кислот (например, буры N3 8407-IQHaO). Содержание бора в земной коре со-стайляет 1(Н%(масс.). Как природный элемент он состоит из двух изотопов 8В (19%) и sB (81%). [c.368]
Наибольшее практическое значение из соединений бора имеют кислородные соединения. Оксид В2О3 имеет ярко выраженные кислотные свойства при взаимодействии с водой образует ортоборную кислоту Н3ВО3. Орто-борная кислота — белые, чешуйчатые кристаллы, хорошо растворимые в горячей воде. Это очень слабая кислота ( 1 = 6-10- ). [c.171]
Оказалось, что системы как со сшивателем, так и без него, обладают нелинейно-вязкими свойствами. Методом минимизации структурного риска установлено, что реологические свойства изученных систем удовлетворительно описываются уравнением Гершеля-Балкли. Для образцов 21 16 и 2051 добавление борной кислоты не приводит к существенному изменению реологического поведения, росту пластического напряжения сдвига и консистентности, что говорит о неэффективности сшивки (рис. 3.22-3.23). В случае образца 2125 добавка борной кислоты резко изменила свойства системы и привела к возникновению аномальных реологических свойств, что видно из рис.3.24. Зависимость напряжения сдвига от скорости деформации принимает экстремальный характер с максимумом в области 5 с , что говорит об образовании достаточно прочной пространственной гелевой структуры. Область резкого линейного роста кривой до скорости деформации 5,537 с соответствует неразрушенной структуре, и система ведет себя как тело Шведова-Бингама с пластическим напряжением сдвига, равным 0,17 Па и структурной вязкостью, равной 1,45 Па с. Уменьшение напряжения сдвига при дальнейшем увеличении скорости деформации говорит о разрушении пространственной структуры, а последующий линейный участок кривой соответствует ее полному разрушению, при этом система ведет себя подобно ньютоновской жидкости с вязкостью 0,13 Па с. Для сравнения, образец 2125 при высоких скоростях сдвига обладает вязкостью порядка 0,046 Па с. [c.
3.22-3.23). В случае образца 2125 добавка борной кислоты резко изменила свойства системы и привела к возникновению аномальных реологических свойств, что видно из рис.3.24. Зависимость напряжения сдвига от скорости деформации принимает экстремальный характер с максимумом в области 5 с , что говорит об образовании достаточно прочной пространственной гелевой структуры. Область резкого линейного роста кривой до скорости деформации 5,537 с соответствует неразрушенной структуре, и система ведет себя как тело Шведова-Бингама с пластическим напряжением сдвига, равным 0,17 Па и структурной вязкостью, равной 1,45 Па с. Уменьшение напряжения сдвига при дальнейшем увеличении скорости деформации говорит о разрушении пространственной структуры, а последующий линейный участок кривой соответствует ее полному разрушению, при этом система ведет себя подобно ньютоновской жидкости с вязкостью 0,13 Па с. Для сравнения, образец 2125 при высоких скоростях сдвига обладает вязкостью порядка 0,046 Па с. [c. 87]
87]
Фторборатные электролиты составляются на основе фторбората никеля, крор/ie того они содержат небольшие количества свободной борфторнс-тоеодородной и борной кислот. Онн обладают хорошими буферными свойствами и большей устойчивостью по сравнению с некоторыми сульфатными электролитами никелирования Выход по гоку в этих электролитах достигает 100 % Они позволяют вести осаждение при высоких (до 20 А/дм=) плотностях тока [c.103]
Ряд патентов, не раскрывая химизма процесса, указывает на возможность ускорения окисления сырья и улучшения свойств битума. Так, для получения битума, имеющего более высокую пенетрацию при данной температуре размягчения, применяют следующие катализаторы и инициаторы окисления сырья кислородом воздуха двуокись марганца [488] хлорид алюминия [463] двуокись марганца и азотную кислоту [437] мелкораздробленный известняк [528] каустическую соду или углекислый натрий [348] бентонит или мелкоизмельченный кокс [315] серу [293] серную кислоту с добавлением металлических солей серной или борной кислот [388] металлические фторобораты [361] борную, фосфорную или мышьяковистую кислоты [406] пятиокнсь фосфора и его сульфиды (РгЗз, Р45з, Р45 ) [492] смесь пятиокиси фосфора и сополимеров изобутилена и стирола, смесь орто-фосфорной кислоты и борофтористого соединения [270] хлорат калия [479] хлорид или сульфат цинка, алюминия, железа, меди или сурьмы [306] хлорид цинка или [c. 157]
157]
Борная кислота легко образует высококонденсированные кислоты, подобные кремневым кислотам, а боратные стекла по свойствам напоминают силикатное стекло. Стекло пирекс служит для изготовления химической стеклянной и жаростойкой посуды это боралюмосиликатное стекло, содержащее лишь 4% ионов щелочных и щелочноземельных металлов. Такое стекло не обладает свойственной обычному стеклу очень слабой растворимостью в воде, а также имеет меньший коэффициент термического расширения, вследствие чего оно не трескается при резких сменах температур. [c.535]
Сода пищевая (бикарбонат натрия (NaH Oa))- Применяется в виде 3-5%-ного водного раствора. В виде 1%-ного — используется для нейтрализации кислот. Обладает моющим и бактерицидным свойствами. При попадании соды в глаза их немедленно обильно промывают водой, а также слабым раствором борной кислоты. [c.28]
Борная мазь 5% 25г
Состав. действующее вещество: кислота борная; 1 г мази содержит кислоты борной 0,05 г вспомогательные вещества: парафин белый мягкий.
Врачебная форма. Мазь 5%.
Основные физико-химические свойства: мазь белого или светло-желтого цвета без запаха. По внешнему виду мазь должна быть однородной.
Фармакологическая группа. Антисептические и дезинфицирующие средства. Препараты борной кислоты.
Код АТХ D08А D.
Фармакологические свойства.
Фармакологические. Борная кислота относится к группе антисептических средств. Оказывает антисептическое, фунгистатическое, а также противопедикулезную и вяжущее действие. Коагулирует белки (в том числе ферментные) микробных клеток, нарушает проницаемость клеточной оболочки. Задерживает рост и развитие бактерий. Оказывает слабое раздражающее действие на грануляционные ткани.
Фармакокинетика. Абсорбируется через поврежденную кожу, раневую поверхность, слизистую оболочку пищеварительного тракта (при случайном приеме внутрь).![]() Борная кислота может накапливаться в органах и тканях организма. Выводится медленно (при повторном поступлении происходит кумуляция).
Борная кислота может накапливаться в органах и тканях организма. Выводится медленно (при повторном поступлении происходит кумуляция).
Клинические характеристики.
Показания. Педикулез. Как антисептическое средство при опрелости и трещинах кожи, дерматите, пиодермии, экземе, остром и хроническом наружном отите.
Противопоказания. Хронический мезотимпанит с нормальной или малоизмененной слизистой оболочкой, травматические перфорации барабанной перепонки. Повышенная чувствительность к борной кислоты. Нарушение функции почек.
Взаимодействие с другими лекарственными средствами и другие виды взаимодействий. При одновременном применении с препаратами для наружного применения могут образовываться новые соединения с непредсказуемым эффектом.
Особенности применения. «Борну мазь 5%» не следует наносить на волосистые участки при острых воспалительных заболеваниях кожи. Следует избегать попадания мази в глаза (в случае попадания промыть глаза теплой водой). Не наносить на большие по площади поверхности тела. При индивидуальной непереносимости кислоты борной или другим компонентам препарата рекомендуется прекратить применение препарата.
Не наносить на большие по площади поверхности тела. При индивидуальной непереносимости кислоты борной или другим компонентам препарата рекомендуется прекратить применение препарата.
Применение в период беременности или кормления грудью. В период беременности и кормления грудью применение лекарственного средства противопоказано.
Способность влиять на скорость реакции при управлении автотранспортом или другими механизмами. Препарат не влияет на способность управлять транспортными средствами или работать с другими механизмами.
Способ применения и дозы. При педикулезе борную мазь наносить на волосистую часть головы в зависимости от степени зараженности, густоты и длины волос, по 10-15-25 г. Через 20-30 мин смыть теплой проточной водой с применением моющих средств. Волосы тщательно вычесывать густым гребнем. Применение при воспалительных заболеваниях наружного слухового прохода определяется врачом и зависит от характера патологического процесса. При опрелости и трещинах кожи мазь наносят тонким слоем на пораженные участки.
При опрелости и трещинах кожи мазь наносят тонким слоем на пораженные участки.
Дети. Опыт применения у детей отсутствует.
Передозировки. При длительном применении на обширных пораженных участках возможны проявления острого отравления: тошнота, рвота, диарея, нарушение кровообращения и угнетение центральной нервной системы, снижение температуры тела, еритроматозний сыпь, шок, кома. При длительном применении возможны проявления хронической интоксикации: истощение, стоматит, экзема, местный отек тканей, нарушение менструального цикла, анемия, судороги, алопеция. Лечение симптоматическое. Показаны гемотрансфузия, гемо- и перитонеальный диализ. В случае случайного употребления внутрь провести зондовое промывание желудка, назначить внутрь солевые слабительные средства, энтеросорбенты (активированный уголь), симптоматическую терапию. В случае тяжелого отравления принимать меры по поддержанию жизненно важных функций организма.
Побочные реакции. При длительном применении на обширных пораженных участках возможны тошнота, головная боль, рвота, спутанность сознания, диарея, кожная сыпь, десквамация эпителия, олигурия. Применение препарата может вызвать аллергические реакции (покраснение кожи, зуд, крапивница, отек). В единичных случаях — развитие анафилактической реакции, включая шок. Судороги.
При длительном применении на обширных пораженных участках возможны тошнота, головная боль, рвота, спутанность сознания, диарея, кожная сыпь, десквамация эпителия, олигурия. Применение препарата может вызвать аллергические реакции (покраснение кожи, зуд, крапивница, отек). В единичных случаях — развитие анафилактической реакции, включая шок. Судороги.
Срок годности. 3 года.
Условия хранения. Хранить в оригинальной упаковке при температуре не выше 25 ° С. Хранить в недоступном для детей месте.
Упаковка. По 25 г в тубах (в пачке из картона или без пачки).
Категория отпуска. Без рецепта.
Производитель / заявитель. ООО «Тернофарм».
Местонахождение производителя и адрес места осуществления его деятельности / местонахождение заявителя. ООО «Тернофарм». Украина, 46010, г.. Тернополь, ул. Фабричная, 4.Тел. / Факс: (0352) 521-444, www.ternopharm. com.ua
com.ua
Дата последнего посещения. 18.12.18
Борная кислота — свойства, получение и применение
Соединения бора
Семейство сплавов на основе системы бор-углерод-кремний — сверхтвёрдый материал с микротвёрдостью, превышающей 70 ГПа. Чрезвычайно
Соединения бора
2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12-Ундекафтор-1-карба-клозо-додекаборан(12) — борорганическое соединение с
Соединения бора
Арсенат бора — неорганическое соединение, бора и мышьяковой кислоты с формулой BAsO4O4), бесцветные кристаллы. Арсенат
Соединения бора
Бор — химический элемент 13-й группы, второго периода периодической системы с атомным номером 5. Бесцветное,
Соединения бора
Борид титана(II) — химическое соединение металла титана и бора с формулой TiB2. Борид титана(II) Общие
Соединения бора
Борид стронция — бинарное неорганическое соединение металла стронция и бора с формулой SrB6, чёрные
Тернофарм–производитель качественной фарм.
 продукции
продукцииСостав:
действующее вещество: boric acid;
1 мл кислоты борной 0,02 г
вспомогательные вещества: этанол 70%.
Лекарственная форма. Раствор для наружного применения, спиртовой 2%.
Основные физико-химические свойства: прозрачная бесцветная жидкость.
Фармакологическая группа.
Антисептические и дезинфицирующие средства. Код АТХ D08A D.
Фармакологические свойства.
Фармакологические. Препарат оказывает антисептическое действие. Коагулирует белки (в том числе ферменты) микробной клетки, нарушает проницаемость клеточной оболочки, благодаря чему задерживается рост и развитие бактерий.
Фармакокинетика. При наружном применении препарат абсорбируется через поврежденную кожу, раневую поверхность; при случайном приеме внутрь — через слизистую оболочку желудочно-кишечного тракта. Кислота борная может накапливаться в тканях организма. Выводится из организма медленно.
Кислота борная может накапливаться в тканях организма. Выводится из организма медленно.
Клинические характеристики.
Показания.
Пиодермия, мокнущая экзема, опрелости, острый и хронический средний отит.
Противопоказания.
Повышенная чувствительность к кислоте борной, нарушение функции почек, хронический мезотимпанит с нормальной или мало измененной слизистой оболочкой, травматические перфорации барабанной перепонки; период беременности и кормления грудью, для обработки молочных желез. Противопоказано применять детям (в том числе новорожденным).
Взаимодействие с другими лекарственными средствами и другие виды взаимодействий.
Взаимодействие пока неизвестна.
При одновременном применении любых других лекарственных средств следует сообщить врачу.
Особенности применения.
Не применять лекарственное средство на большие участки кожи, не применять для промывания полостей. Не допускать попадания препарата в глаза.
Не допускать попадания препарата в глаза.
Применение в период беременности или кормления грудью.
Препарат противопоказан в период беременности или кормления грудью.
Способность влиять на скорость реакции при управлении автотранспортом или другими механизмами.
Не влияет.
Способ применения и дозы.
Применять наружно.
При пиодермии, опрелости, экземе пораженные участки кожи обрабатывать с помощью салфетки, предварительно смоченной препаратом, 2-3 раза в сутки.
При отите в наружный слуховой проход вводить смоченные раствором турунды или закапывать по 3-5 капель 2-3 раза в сутки.
Дети.
Препарат противопоказан детям.
Передозировки.
В случае случайного употребления внутрь провести зондовое промывание желудка, назначить внутрь солевые слабительные средства, энтеросорбенты (активированный уголь), симптоматическую терапию.
Симптомы острого отравления: тошнота, рвота, диарея, нарушение кровообращения и угнетение центральной нервной системы, снижение температуры тела, шок, кома, эритематозная сыпь. В случае тяжелого отравления принимать меры по поддержанию жизненно важных функций организма, проводить гемодиализ или перитонеальный диализ, заменное переливание крови. При длительном применении препарата на больших по площади участках кожи могут возникать симптомы хронической интоксикации: отек тканей, истощение, стоматит, экзема, нарушение менструального цикла у женщин, анемия, судороги, алопеция. В этих случаях препарат следует отменить, провести симптоматическое лечение.
В случае тяжелого отравления принимать меры по поддержанию жизненно важных функций организма, проводить гемодиализ или перитонеальный диализ, заменное переливание крови. При длительном применении препарата на больших по площади участках кожи могут возникать симптомы хронической интоксикации: отек тканей, истощение, стоматит, экзема, нарушение менструального цикла у женщин, анемия, судороги, алопеция. В этих случаях препарат следует отменить, провести симптоматическое лечение.
Побочные реакции.
Применение препарата может вызвать аллергические реакции (покраснение кожи, зуд, крапивница, сыпь, отек). В единичных случаях — развитие анафилактической реакции, включая шок, десквамация эпителия.
При длительном применении, а также при наличии у пациента нарушения функции почек могут возникнуть тошнота, рвота, диарея, головная боль, спутанность сознания, олигурия, судороги.
В случае появления любых нежелательных явлений необходимо обратиться к врачу!
Срок годности. 3 года.
3 года.
Условия хранения.
Хранить при температуре не выше 25 ° С.
Хранить в недоступном для детей месте.
Упаковка.
По 10 мл, или по 20 мл во флаконах-капельницах (в пачке из картона или без пачки).
Категория отпуска. Без рецепта.
Производитель / заявитель.
ООО «Тернофарм».
Местонахождение производителя и его адрес места осуществления деятельности / местонахождение заявителя.
Украина, 46010, г. Тернополь, ул. Фабричная, 4.
Тел. / Факс: (0352) 521-444, www.ternopharm.com.ua
Дата последнего пересмотра. 21.06.18
Борная кислота: состав, назначение и применение
Борная кислота представляет собой медикамент, который знаком еще с детских времен. Наверняка у наших родителей и бабушек есть в аптечке данный препарат, хотя в аптеках продается множество альтернативных лекарств. Столь частое использование вещества обуславливается его ценными свойствами. Борная кислота применяется во многих отраслях.
Столь частое использование вещества обуславливается его ценными свойствами. Борная кислота применяется во многих отраслях.
Состав и форма выпуска
Данное вещество относят к слабым кислотам. Состоит оно из прозрачных кристаллов-чешуек без запаха. Средство производится в следующих формах:
- порошок с кисловатым вкусом в банках или упаковках;
- жидкость водная или спиртовая;
- флаконы в виде капельниц;
- мазь 5 или 10 %.
Определенная форма борной кислоты выбирается с учетом характеристик возникшего недуга. Алгоритм применения может также различаться.
Фармакологическое действие
Учитывая свойства солей борной кислоты, препарат обладает антибактериальным, противогрибковым, вяжущим, антисептическим, фунгистатическим, противопедикулезным и противопаразитарным фармакологическим действием. Данное вещество коагулирует белки патологической клетки. Кислота слабо раздражает грануляционные ткани.
Фармакокинетические свойства
Борная кислота беспрепятственно проникает через поверхность раны, а также слизистую органов пищеварения при возможном употреблении кислоты внутрь организма. Как утверждают медики, вещество имеет свойство накапливаться со временем и медленно выводиться.
Как утверждают медики, вещество имеет свойство накапливаться со временем и медленно выводиться.
Применение кислоты
Борную кислоту по назначению врача применяют при следующих болезнях:
- конъюнктивит;
- хронический отит в острой форме;
- экзема;
- опрелости;
- пиодермия;
- дерматит;
- заражение вшами;
- кольпит.
Чтобы вылечить заболевания кожи, в основном применяют спиртовую форму бора, которой смачиваются тампоны из ваты и обрабатывают пораженную кожу. Кроме того, раствором на основе спирта можно делать целебные примочки. Ведь антисептические свойства борной кислоты отлично действуют на раны.
Чтобы излечить отит, бор закапывают в пораженное ухо по 5 капель трижды в сутки. Курс процедур должен составлять максимум 5-6 дней. В случае возникновения кольпита назначают 10 % раствор. Изготавливают его из порошка кислоты, который также подходит для обработки кожи.
При развитии у человека педикулеза кислоту врачи назначают в форме мази. Единожды на 30 минут ее наносят на голову. Далее поверхность, обработанную кислотным составом, нужно хорошо промыть.
Единожды на 30 минут ее наносят на голову. Далее поверхность, обработанную кислотным составом, нужно хорошо промыть.
Иногда данный препарат назначают для выполнения определенных медицинских процедур. Например, бор в порошковой форме обычно назначают для вдувания в полость уха.
При конъюнктивите категорически запрещено закапывать кислоту в неразведенном виде! Для терапии этого недуга нужно приготовить некрепкий раствор, смешивая препарат с другими составляющими, следуя назначениям доктора.
Предостережение
Борную кислоту предполагается применять только после консультации врача и выполненного медицинского обследования, четко выполняя инструкцию. Исключительно квалифицированный доктор может назначить наиболее оптимальную и эффективную схему и форму борной кислоты, определить оптимальную длительность лечения, учитывая имеющуюся местную симптоматику.
Применение в косметологии
Бор довольно часто применяется в области красоты. Особенно хорошо данный препарат помогает бороться с прыщами и угрями. Известно, что данное средство имеет хорошие обеззараживающие и подсушивающие качества, эффективно понижая уровень жирности кожных покровов. Чтобы побороть проблему возникновения акне, достаточно:
Известно, что данное средство имеет хорошие обеззараживающие и подсушивающие качества, эффективно понижая уровень жирности кожных покровов. Чтобы побороть проблему возникновения акне, достаточно:
- обрабатывать жирные участки кожи водным раствором бора;
- частично прижигать воспаленные участки раствором на основе спирта.
Игривые веснушки можно ежедневно обрабатывать 3 % водным раствором, дополнительно добавив к нему небольшое количество бесцветной хны. Этот способ поможет выровнять тон, а также убрать пятнышки. Стоит отметить, что данную кислоту не рекомендуется применять самостоятельно. Использовать ее нужно предельно аккуратно, даже учитывая сниженную концентрацию данного вещества.
Другие области использования
Известно, что кислота бора с успехом используется в косметологии и медицине. Также средство может применяться и в других областях:
- ювелирное дело – борная кислота играет роль флюса для процесса пайки ювелирных сплавов;
- сельское хозяйство – данная кислота увеличивает усвояемость азота, что повышает урожайность примерно на 20 %, одновременно помогая растениям избавиться от различных заболеваний и увеличивая стойкость к морозам;
- стекольное производство – данное средство помогает добиться максимального блеска, прозрачности и теплового сопротивления, благодаря чему стекло приобретает химическую стойкость;
- против насекомых и тараканов;
- металлургия – кислота дает возможность увеличить прочность, а также чистоту стали, уменьшить температуру плавления, снизить возможное разрушение материалов;
- хозяйство — бор используют в качестве довольно эффективного чистящего и дезодорирующего средства.
 Это вещество дезинфицирует поверхности на кухне, помогает удалить жир и размягчить в унитазе стойкий налет.
Это вещество дезинфицирует поверхности на кухне, помогает удалить жир и размягчить в унитазе стойкий налет.
Данную кислоту нужно вносить в огород весь вегетативный период, поскольку она не переходит молодым стеблям от старых, требуя постоянного обновления. В боре особенно остро нуждаются растения, которые произрастают на заболоченных грунтах, где имеется большое количество карбонатов. К тому же бор нужно вносить с почву с высокой кислотностью. Предварительно грунт нужно раскислить щелочесодержащими веществами.
Самостоятельное приготовление раствора
Все смеси и растворы можно очень легко приготовить самостоятельно, используя для этого специальный порошок бора. Антибактериальное действие кислоты начинается с 2 %. Чтобы приготовить раствор на основе воды, нужно взять 100 мл горячей воды и растворить в ней 0,5 ч. л. кислоты. В результате выходит 3-4 % раствор.
Кроме того, кислота легко растворяется в спирте. Соотношения должны быть высчитаны объемными долями. Также кислоту можно смешивать с размягченным белым парафином или вазелином. Данный состав применяют наружно, делая спиртовые и водные составы, а при кожных болезнях раствор назначают в форме присыпки.
Также кислоту можно смешивать с размягченным белым парафином или вазелином. Данный состав применяют наружно, делая спиртовые и водные составы, а при кожных болезнях раствор назначают в форме присыпки.
Противопоказания
Крайне не рекомендуется использовать кислоту данного типа людям, которые страдают нарушенным функционированием почек, женщинам в период беременности и лактации, в детском и младенческом возрасте, а также в случае непереносимости компонентов. К тому же препараты данной кислоты не рекомендуют наносить на участки тела большого размера.
Передозировка
Если кислота будет случайно выпита, пациенту необходимо тщательно промыть желудок. Для этого предпочтительно использовать зонд. Также внутрь подают солевые растворы и энтеросорбенты. После этих процедур больному назначают симптоматическую терапию. В случае тяжелой передозировки нужно максимально поддерживать важные для полноценной жизни функции человека, выполнить перитонеальный диализ и переливание крови при необходимости.
Признаками передозировки кислотой данного типа являются диарея, эритематоз, стоматит, угнетение работы мозга, олигурия, нарушение кровообращения, в некоторых ситуациях развивается шок или кома.
Если предполагается длительное применение кислоты данного типа, могут через некоторое время возникать симптомы острой интоксикации – истощение организма, экзема, отечность, анемия, нарушения цикла менструации и даже судороги. В таком случае следует незамедлительно перестать использовать бор, выполнить симптоматическое лечение.
Побочные эффекты
При применении кислоты в дозах, значительно превышающих рекомендованные, могут довольно быстро возникать побочные эффекты. В результате неправильного использования данного препарата у человека могут появиться аллергические реакции: отек кожи, гиперемия, крапивница, высыпания и зуд. Очень редко может возникать анафилактическая реакция и десквамация эпителия.
Итог
В конце стоит упомянуть и о физико-химических свойствах борной кислоты. Она имеет температуру плавления больше 170 градусов, при этом превращаясь в метаборную кислоту или оксид бора. Растворима в глицерине при массе больше 25 %. Если говорить о физических свойствах борной кислоты и применении ее людьми, то она имеет вид белого порошка, который перерабатывается на нужное лекарственное средство и широко используется, о чем указано выше.
Она имеет температуру плавления больше 170 градусов, при этом превращаясь в метаборную кислоту или оксид бора. Растворима в глицерине при массе больше 25 %. Если говорить о физических свойствах борной кислоты и применении ее людьми, то она имеет вид белого порошка, который перерабатывается на нужное лекарственное средство и широко используется, о чем указано выше.
Существует поистине много методов применения борной кислоты, причем некоторые из них могут удивить. Но важно отметить, что использовать этот кислотный препарат можно исключительно по согласованию с лечащим врачом. Грамотное назначение поможет избежать довольно серьезных последствий.
Борная кислота — Material DB — RoHS
| Борная кислота | |
| Общие | |
|---|---|
| Систематическое наименование | Ортоборная кислота |
Хим. формула формула | H3BO3 |
| Физические свойства | |
| Состояние | твёрдое |
| Молярная масса | 61,83 г/моль |
| Плотность | 1,435 (15 °C) |
| Термические свойства | |
| Т. плав. | 170.9 °C, 444 K, 340 °F |
| Т. кип. | 300 °C, 573 K, 572 °F °C |
| Химические свойства | |
| pKa | 9,24 (I), 12,74 (II), 13,80 (III) |
| Растворимость в воде | 2.52 (0 °C) |
| Классификация | |
| Рег. номер CAS | 10043-35-3 |
| PubChem | 7628 |
| Рег. номер EINECS | 233-139-2 |
| SMILES | |
| InChI | |
| Кодекс Алиментариус | E284 |
| RTECS | ED4550000 |
| ChEBI | 33118 |
| ChemSpider | 7346 |
| Безопасность | |
| Токсичность | |
Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Бо́рная кислота́ (ортоборная кислота или лат. acidum Boricum) — слабая, одноосновная кислота Льюиса, часто используемая в качестве инсектицида, антисептика, огнезащитного состава, поглотителя нейтронов или предшественника для получения иных химических составов. Имеет химическую формулу H3BO3 (или B(OH)3).
Бесцветное кристаллическое вещество в виде чешуек без запаха, имеет слоистую триклинную решётку, в которой молекулы кислоты соединены водородными связями в плоские слои, слои соединены между собой межмолекулярными связями (d = 0,318 нм).
Метаборная кислота (HBO2) также представляет собой бесцветные кристаллы. Она существует в трёх модификациях — наиболее устойчивой γ-НВО2 с кубической решёткой, β-НВО2 с моноклинной решёткой и α-НВО2 с ромбической решёткой.
При нагревании ортоборная кислота теряет воду и сначала переходит в метаборную кислоту, затем в тетраборную H2B4O7. При дальнейшем нагревании обезвоживается до борного ангидрида.
При дальнейшем нагревании обезвоживается до борного ангидрида.
Водные растворы борной кислоты являются смесью полиборных кислот общей формулы Н3m-2nВmО3m-n. В природе встречается в виде минерала сассолина.
Нахождение в природе
В природе свободная борная кислота встречается в виде минерала сассолина, в горячих источниках и минеральных водах.
Получение
Борная кислота может быть получена путем смешения буры (Тетрабората натрия) с минеральной кислотой, такой как соляная кислота:
- Na2B4O7·10H2O + 2 HCl → 4 B(OH)3 [or H3BO3] + 2 NaCl + 5 H2O
Также является продуктом гидролиза диборана или тригалогенидов бора:[1]
- B2H6 + 6 H2O → 2 B(OH)3 + 6 H2
- BX3 + 3 H2O → B(OH)3 + 3 HX (X = Cl, Br, I)
Свойства
Борная кислота проявляет очень слабые кислотные свойства. Она сравнительно мало растворима в воде. Её кислотные свойства обусловлены не отщеплением протона Н+, а присоединением гидроксильного аниона:
Она сравнительно мало растворима в воде. Её кислотные свойства обусловлены не отщеплением протона Н+, а присоединением гидроксильного аниона:
- B(OH)3+h3O→H[B(OH)4]{\displaystyle {\mathsf {B(OH)_{3}+H_{2}O\rightarrow H[B(OH)_{4}]}}}
- Ka = 5.8·10−10 моль/л; pKa = 9.24.
Она легко вытесняется из растворов своих солей большинством других кислот. Соли её, называемые боратами, производятся обычно от различных полиборных кислот, чаще всего — тетраборной Н2В4О7, которая является значительно более сильной кислотой, чем ортоборная.
Очень слабые признаки амфотерности B(OH)3 проявляет, образуя малоустойчивый гидросульфат бора В(HSO4)3.
При нейтрализации ортоборной кислоты щелочами в водных растворах не образуются ортобораты, содержащие ион (ВО3)3−, поскольку ортобораты гидролизуются практически полностью, вследствие слишком малой константы образования [В(ОН)4]−. {2-}}}}
{2-}}}}
Наиболее распространённой солью борной кислоты является декагидрат тетрабората натрия Na2B4O7·10H2O (техническое название — бура).
При нагревании борная кислота растворяет оксиды металлов, образуя соли.
Со спиртами в присутствии концентрированной серной кислоты образует эфиры:
- h4BO3+ 3Ch4OH⟶ 3h3O+ B(OCh4)3{\displaystyle {\mathsf {H_{3}BO_{3}+\ 3CH_{3}OH\longrightarrow \ 3H_{2}O+\ B(OCH_{3})_{3}}}}
Образование борнометилового эфира В(ОСН3)3 является качественной реакцией на Н3ВО3 и соли борных кислот, при поджигании борнометиловый эфир горит красивым ярко-зеленым пламенем.
Опасность борной кислоты
Борная кислота может быть опасна только при бесконтрольном приеме внутрь. Опасная концентрация в организме человека (а особенно ребёнка) может возникнуть при регулярном применении. Смертельная доза при отравлении через рот для взрослого человека составляет 15–20 г, для детей — 4–5 г [2].
Борная кислота применяется в медицине с 60-х годов XIX века как антисептическое средство, не раздражающее ран и не имеющее вкуса, запаха и цвета. В современной медицине противомикробная эффективность борной кислоты считается низкой.
Из-за малой эффективности использование борной кислоты в качестве антисептического средства для детей, а также беременных кормящих женщин было запрещено 2 февраля 1987 года Министерством здравоохранения СССР по рекомендации Фармакологического комитета
[источник не указан 1357 дней]
Применение
- В ядерных реакторах в качестве поглотителя нейтронов, растворённого в теплоносителе.
- Борное удобрение.
- В лабораториях применяют для приготовления буферных растворов.
- В медицине — как самостоятельное дезинфицирующее средство для взрослых, а также в виде 2%-го раствора — для промывки кожи после попадания щелочей.
- Также на основе борной кислоты производятся различные комбинированные препараты (группа АТХ D08AD), например паста Теймурова.

- В фотографии — в составе мелкозернистых проявителей и кислых фиксажей для создания слабой кислотной среды.
- В пищевой промышленности зарегистрирована как пищевая добавка E284 (на территории России эта добавка не входит в список разрешённых к применению[3]).
- В ювелирном деле — как основа флюсов для пайки золотосодержащих сплавов.
- В литейном производстве — связующее при кислой футеровке печей, компонент защиты струи от окисления при разливке магниевых сплавов.
- В быту — уничтожение тараканов,муравьёв, клопов.
- В производстве керамики, оптоволокна,стекловолокна, стекла[4],
- В качестве антипирена для защиты древесины,
- В составе электролитов для меднения и никелирования.
См. также
Борная кислота — Структура, свойства, получение и применение
×
Извините !, эта страница сейчас недоступна для добавления в закладки.
Изображение будет скоро загружено
Что такое борная кислота?
Борная кислота — неорганическое соединение, которое представляет собой слабую одноосновную кислоту Льюиса бора.Хотя в некоторых химических реакциях действует как трехосновная кислота. Он также известен как борат водорода, борная кислота и ортоборная кислота. Его название по ИЮПАК — тригидрооксидобор.
Молекулярная формула борной кислоты — h4BO3
Структурная формула борной кислоты —
Когда борная кислота встречается в природе в виде минерала, она называется сассолитом. Это кристаллическое твердое вещество при комнатной температуре. Он входит в состав многих природных минералов, таких как бура, борацит, улексит и колеманит.Его соли содержатся в морской воде. Он также содержится во всех фруктах и многих растениях.
Вильгельм Хомберг впервые получил кристаллы борной кислоты в 1702 году. Он дал им название sal sedativum Hombergi (седативная соль Хомберга). Хотя соединения борной кислоты использовались еще со времен древних греков для очистки, консервирования продуктов и других видов деятельности.
СМОТРЕТЬ БОЛЬШЕ
Кристаллическая структура борной кислоты
Она имеет тригональную плоскую геометрию из-за трех атомов кислорода вокруг бора. В этой связи длина B-O составляет 136 пм, а O-H — 97 пм. Ниже приводится структура элементарной ячейки борной кислоты.
В этой связи длина B-O составляет 136 пм, а O-H — 97 пм. Ниже приводится структура элементарной ячейки борной кислоты.
Изображение будет загружено в ближайшее время.
Свойства борной кислоты
Физические свойства борной кислоты —
Это бесцветное или белое кристаллическое твердое вещество при комнатной температуре.
Его молярная масса 61,83 г / моль.
Его температура плавления составляет 170,9 ℃.
Его температура кипения составляет 300 ℃.
Растворим в воде.
Химические свойства борной кислоты —
h4BO3 170 ℃ → HBO2 + h3O
При 300 ℃ дает тетраборную кислоту. Реакция приведена ниже —
4HBO2 🡪 h3B4O7 + h3O
При нагревании выше 330 ℃ дает триоксид бора. Реакция приведена ниже —
Реакция приведена ниже —
h3B4O7 🡪 2B2O3 + h3O
B (OH) 3 + 3ROH 🡪 B (OR) 3 + 3h3O
B (OH) 3 + 6h3SO4 🡪 B (HSO4) 4- + 2HSO4- + 3h4O +
Получение борной кислоты
Na2B4O7.10h3O + 2HCl 🡪 4B (OH) 3 + 2NaCl + 5h3O
B2H6 + 6h3O 🡪 2B (OH) 3 + 6h3
BX3 + 3h3O 🡪 B (OH) 3 + 3HX (X = Cl, Br, I)
Использование борной кислоты
Мы используем борную кислоту с древних времен. В настоящее время он в основном используется в промышленности. Некоторые из его применений перечислены ниже —
Он используется в производстве моноволокна из стекловолокна.
Используется в ювелирной промышленности в сочетании с денатурированным спиртом.
Используется в производстве стекла для плоских ЖК-дисплеев.

Применяется в гальванике.
В качестве антипирена применяется смесь борной кислоты.
Применяется при изготовлении набивной массы.
Он также используется в медицинских целях, так как снижает вредное воздействие HF.
Борная кислота в смеси с бурой используется для сварки флюсов кузнецами.
Часто используется как антисептик, инсектицид, антипирен, поглотитель нейтронов и т. Д.
Используется для предотвращения или уничтожения существующей влажной и сухой гнили в древесине.
Используется в качестве основной буферной системы в плавательных бассейнах.
Он используется на некоторых атомных электростанциях как нейтронный яд.
Его смесь с нефтяным или растительным маслом работает как отличная смазка.
Это все о борной кислоте. Если вы ищете подробные учебные материалы по различным темам химии, зарегистрируйтесь на Vedantu или загрузите приложение Vedantu Learning для классов 6-10, IIT-JEE и NEET.
Формула борной кислоты — применение, свойства, структура и формула борной кислоты
Формула и структура: Химическая формула борной кислоты: H 3 BO 3 (или B (OH) 3 ). Его молекулярная формула: BH 3 O 3 , а его молярная масса составляет 61,83 г / моль. Химическая структура борной кислоты представлена ниже:
Центральный атом бора связан с тремя гидроксильными (-ОН) группами, которые способны образовывать прочную водородную связь. Его твердая кристаллическая структура состоит из параллельных слоев борной кислоты, удерживаемых вместе водородными связями.
Его твердая кристаллическая структура состоит из параллельных слоев борной кислоты, удерживаемых вместе водородными связями.
Происхождение: Борная кислота естественным образом встречается в вулканических районах и в некоторых минералах, таких как бура (например, сассолит). В небольших количествах он также содержится в морской воде, растениях и фруктах.
Приготовление: Борная кислота получается взаимодействием минералов, таких как бура (Na 2 B 4 O 7 · 10H 2 O), с сильными кислотами, такими как HCl:
Na 2 B 4 O 7 · 10H 2 O + 2 HCl → 4 H 3 BO 3 + 2 NaCl + 5 H 2 O
Его также можно получить гидролизом тригалогенидов бора (например, BBr 3 ) или диборана (B 2 H 6 ):
BBr 3 + 3 H 2 O → B (OH) 3 + 3 HBr
B 2 H 6 + 6 H 2 O → 2 B (OH) 3 + 6 H 2
Физические свойства: Борная кислота представляет собой белое кристаллическое вещество с плотностью 1. 435 г / мл, точка плавления 170,9 ° C и точка кипения 300 ° C.
435 г / мл, точка плавления 170,9 ° C и точка кипения 300 ° C.
Химические свойства: Борная кислота является слабой одноосновной кислотой и считается кислотой Льюиса. Растворяется в кипящей воде и безводной серной кислоте. При нагревании до высоких температур (более 170 ° C) он подвергается дегидратации с образованием метаборной кислоты (HBO 2 ):
H 3 BO 3 → HBO 2 + H 2 O
Применение: Борная кислота нетоксична с антибактериальными свойствами, и она в основном используется в качестве антисептического средства, лечения угрей, консерванта, инсектицида, буфера pH, химического вещества для плавательных бассейнов, антипирена и прекурсора для многих полезных химикатов.Он используется в промышленности для производства стекловолокна, бытовых изделий из стекла и стекла, используемого в ЖК-дисплеях.
Опасность для здоровья / воздействие на здоровье: Низкая концентрация борной кислоты не токсична. Однако борная кислота ядовита при проглатывании или вдыхании в больших количествах. Высокие концентрации борной кислоты могут потенциально привести к репродуктивным проблемам. Воздействие борной кислоты в течение длительного времени может вызвать повреждение почек.
БОРНАЯ КИСЛОТА | CAMEO Chemicals
Химический лист данных
Химические идентификаторы | Опасности | Рекомендации по ответу | Физические свойства | Нормативная информация | Альтернативные химические названияХимические идентификаторы
В Поля химического идентификатора включать общие идентификационные номера, NFPA алмаз U.S. Знаки опасности Министерства транспорта и общие описание химического вещества. Информация в CAMEO Chemicals поступает из множества источники данных.| Номер CAS | Номер ООН / NA | Знак опасности DOT | USCG CHRIS Код |
|---|---|---|---|
| никто | данные недоступны | ||
| Карманный справочник NIOSH | Международная карта химической безопасности | ||
| никто | |||
NFPA 704
данные недоступны
Общее описание
Белое твердое вещество без запаха. Температура плавления 171 ° C. Тонет и смешивается с водой. (USCG, 1999)
Температура плавления 171 ° C. Тонет и смешивается с водой. (USCG, 1999)
Опасности
Оповещения о реактивности
никто
Реакции воздуха и воды
Вода.
Пожарная опасность
Литературные источники указывают, что это соединение негорючее. (NTP, 1992)
Опасность для здоровья
Хотя о побочных эффектах при вдыхании пыли борной кислоты не сообщалось, она всасывается через слизистые оболочки.Проглатывание 5 граммов или более может вызвать раздражение желудочно-кишечного тракта и повлиять на центральную нервную систему. Контакт с пылью или водными растворами может вызвать раздражение глаз; хронических эффектов не обнаружено, но следует избегать постоянного контакта. Пыль и растворы впитываются через ожоги и открытые раны, но не через неповрежденную кожу. (USCG, 1999)
Профиль реактивности
БОРНАЯ КИСЛОТА — очень слабая кислота. Несовместим с карбонатами и гидроксидами щелочных металлов. Во время попытки получить триацетилборат смесь борной кислоты и уксусного ангидрида взорвалась при нагревании до 58-60 ° C [Chem.Англ. News 51: (34) 1973]. Реагирует бурно с сильным восстановителем металлическим калием.
Во время попытки получить триацетилборат смесь борной кислоты и уксусного ангидрида взорвалась при нагревании до 58-60 ° C [Chem.Англ. News 51: (34) 1973]. Реагирует бурно с сильным восстановителем металлическим калием.
Принадлежит к следующей реактивной группе (группам)
Потенциально несовместимые абсорбенты
Информация отсутствует.
Ответные рекомендации
В Поля рекомендаций ответа включать расстояния изоляции и эвакуации, а также рекомендации по пожаротушение, противопожарное реагирование, защитная одежда и первая помощь.В информация в CAMEO Chemicals поступает из различных источники данных.Изоляция и эвакуация
Нет доступной информации.
Пожарная
Средства пожаротушения: Водяной туман. (USCG, 1999)
Без огня
НЕБОЛЬШИЕ РАЗЛИВЫ И УТЕЧКА: Если вы разлили это химическое вещество, вам следует смочить твердый разлившийся материал водой, а затем перелить смоченный материал в подходящий контейнер. Используйте впитывающую бумагу, смоченную водой, чтобы собрать оставшийся материал.Поместите загрязненную одежду и впитывающую бумагу в паронепроницаемый полиэтиленовый пакет для последующей утилизации. Вымойте все загрязненные поверхности сильным мыльным раствором. Не входите в зараженную зону до тех пор, пока специалист по безопасности (или другое ответственное лицо) не убедится, что зона была должным образом очищена.
Используйте впитывающую бумагу, смоченную водой, чтобы собрать оставшийся материал.Поместите загрязненную одежду и впитывающую бумагу в паронепроницаемый полиэтиленовый пакет для последующей утилизации. Вымойте все загрязненные поверхности сильным мыльным раствором. Не входите в зараженную зону до тех пор, пока специалист по безопасности (или другое ответственное лицо) не убедится, что зона была должным образом очищена.МЕРЫ ПРЕДОСТОРОЖНОСТИ ПРИ ХРАНЕНИИ: Этот материал следует хранить при температуре окружающей среды. (NTP, 1992)
Защитная одежда
Химические очки; химически стойкие перчатки и одежда.(USCG, 1999)
Ткани для костюмов DuPont Tychem®
Нет доступной информации.
Первая помощь
ГЛАЗА: Сначала проверьте пострадавшего на предмет контактных линз и снимите, если они есть. Промойте глаза пострадавшего водой или физиологическим раствором в течение 20–30 минут, одновременно позвонив в больницу или токсикологический центр. Не наносите никаких мазей, масел или лекарств в глаза пострадавшему без специальных указаний врача. НЕМЕДЛЕННО доставьте пострадавшего после промывки глаз в больницу, даже если симптомы (например, покраснение или раздражение) не развиваются.
Не наносите никаких мазей, масел или лекарств в глаза пострадавшему без специальных указаний врача. НЕМЕДЛЕННО доставьте пострадавшего после промывки глаз в больницу, даже если симптомы (например, покраснение или раздражение) не развиваются.КОЖА: НЕМЕДЛЕННО затопите пораженную кожу водой, сняв и изолировав всю зараженную одежду. Осторожно промойте все пораженные участки кожи водой с мылом. При появлении таких симптомов, как покраснение или раздражение, НЕМЕДЛЕННО вызовите врача и будьте готовы перевезти пострадавшего в больницу для лечения.
ВДЫХАНИЕ: НЕМЕДЛЕННО покиньте зараженную зону; сделайте глубокий вдох на свежем воздухе. При появлении симптомов (таких как свистящее дыхание, кашель, одышка или жжение во рту, горле или груди) вызовите врача и будьте готовы перевезти пострадавшего в больницу.Обеспечьте надлежащую защиту органов дыхания спасателям, попадающим в неизвестную атмосферу. По возможности следует использовать автономный дыхательный аппарат (АДА); если недоступно, используйте уровень защиты выше или равный указанному в разделе «Защитная одежда».
ПРОГЛАТЫВАНИЕ: НЕ ВЫЗЫВАЙТЕ РВОТУ. Если пострадавший находится в сознании и не испытывает конвульсий, дайте 1 или 2 стакана воды для разбавления химического вещества и НЕМЕДЛЕННО позвоните в больницу или токсикологический центр. Будьте готовы перевезти пострадавшего в больницу по совету врача.Если пострадавший находится в конвульсиях или без сознания, не давайте ничего через рот, убедитесь, что дыхательные пути пострадавшего открыты, и положите пострадавшего на бок так, чтобы голова была ниже тела. НЕ ВЫЗЫВАЕТ РВОТУ. НЕМЕДЛЕННО доставьте пострадавшего в больницу. (NTP, 1992)
Физические свойства
Точка воспламенения: данные недоступны
Нижний предел взрываемости (НПВ): данные недоступны
Верхний предел взрываемости (ВПВ): данные недоступны
Температура самовоспламенения: данные недоступны
Температура плавления: 340 ° F (NTP, 1992)
Давление пара: данные недоступны
Плотность пара (относительно воздуха): данные отсутствуют
Удельный вес: 1. 435 при 68 ° F (USCG, 1999)
435 при 68 ° F (USCG, 1999)
Точка кипения: 572 ° F при 760 мм рт. (разлагается) (NTP, 1992)
Молекулярный вес: 61,83 (NTP, 1992)
Растворимость воды: От 10 до 50 мг / мл при 66 ° F (NTP, 1992)
Потенциал ионизации: данные недоступны
IDLH: данные недоступны
AEGL (рекомендованные уровни острого воздействия)
Информация AEGL отсутствует.ERPG (Руководство по планированию действий в чрезвычайных ситуациях)
Информация по ERPG отсутствует.PAC (критерии защитного действия)
| Химическая промышленность | PAC-1 | PAC-2 | PAC-3 |
|---|---|---|---|
| Борная кислота (10043-35-3) | 6 мг / м3 | 23 мг / м3 | 830 мг / м3 |
(DOE, 2016)
Нормативная информация
В Поля нормативной информации включать информацию из U. S. Сводный список раздела III Агентства по охране окружающей среды
Списки,
химический объект Министерства внутренней безопасности США
Стандарты борьбы с терроризмом,
и Управления по охране труда и здоровья США
Стандартный список управления производственной безопасностью особо опасных химических веществ
(подробнее об этих
источники данных).
S. Сводный список раздела III Агентства по охране окружающей среды
Списки,
химический объект Министерства внутренней безопасности США
Стандарты борьбы с терроризмом,
и Управления по охране труда и здоровья США
Стандартный список управления производственной безопасностью особо опасных химических веществ
(подробнее об этих
источники данных).Сводный список списков Агентства по охране окружающей среды
Нет нормативной информации.Стандарты по борьбе с терроризмом химического предприятия DHS (CFATS)
Нет нормативной информации.Список стандартов управления безопасностью процессов (PSM) OSHA
Нет нормативной информации.Альтернативные химические названия
В этом разделе представлен список альтернативных названий этого химического вещества, включая торговые наименования и синонимы.
- БАЗИЛИТ Б
- БОРНАЯ КИСЛОТА
- БОРНАЯ КИСЛОТА
- БОРНАЯ КИСЛОТА (B (OH) 3)
- BOROFAX
- ТРИГИДРОКСИД БОРА
- DIA FLEA-MATE
- DR.
 ‘S 1 FLEA TERMINATOR DF
‘S 1 FLEA TERMINATOR DF - ТЕРМИНАТОР FLEA DFPBO DR. 1
- ТЕРМИНАТОР FLEA TERMINATOR DR. DT
- ТЕРМИНАТОР FLEA TERMINATOR DR. DTPBO
- FLEA PRUFE
- ОРТОБОРАТ ВОДОРОДА
- NCI-C56417
- КИСЛОТА ОРТОБОРНАЯ
- ОРТОБОРНАЯ КИСЛОТА (B (OH) 3)
- ОРТОБОРНАЯ КИСЛОТА (h4BO3)
- SUPER FLEA ELIMINATOR
- ТРИ СЛОНА
- ТРИГИДРОКСИБОРАН
| Запись информации | ||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Версия | 2.0 | |||||||||||||||||||||||||||||||||
| Дата создания | 2013-04-25 07:56:50 UTC | |||||||||||||||||||||||||||||||||
| Дата обновления | 2014-12-24 20:26:32 UTC | |||||||||||||||||||||||||||||||||
| Регистрационный номер | T3D3799 | |||||||||||||||||||||||||||||||||
| Идентификация | ||||||||||||||||||||||||||||||||||
| Общее название | Борная кислота (h4BO3) | |||||||||||||||||||||||||||||||||
| Класс | Малая молекула | |||||||||||||||||||||||||||||||||
| Описание | борная кислота (борная кислота, также называется борной кислотой), борная кислота (орто-борная кислота), также называется борной кислотой 4BO3 слабая кислота бора, часто используемая в качестве антисептика, инсектицида, антипирена, поглотителя нейтронов или предшественника других химических соединений. Он имеет химическую формулу h4BO3 (иногда обозначается как B (OH) 3) и существует в виде бесцветных кристаллов или белого порошка, растворяющегося в воде. Встречаясь в виде минерала, он называется сассолитом. Борат — это загрязнитель пищевых продуктов, образующийся при контакте бумаги и картона с пищевыми продуктами. Он имеет ограниченное использование в качестве антибактериального средства в икре. Он имеет химическую формулу h4BO3 (иногда обозначается как B (OH) 3) и существует в виде бесцветных кристаллов или белого порошка, растворяющегося в воде. Встречаясь в виде минерала, он называется сассолитом. Борат — это загрязнитель пищевых продуктов, образующийся при контакте бумаги и картона с пищевыми продуктами. Он имеет ограниченное использование в качестве антибактериального средства в икре. | |||||||||||||||||||||||||||||||||
| Состав типа |
| |||||||||||||||||||||||||||||||||
| Химическая структура | ||||||||||||||||||||||||||||||||||
| Синонимы |
| |||||||||||||||||||||||||||||||||
| Химическая форма ula | BH 3 O 3 | |||||||||||||||||||||||||||||||||
| Средняя молекулярная масса | 61.833 г / моль | |||||||||||||||||||||||||||||||||
| Моноизотопная масса | 62,018 г / моль | |||||||||||||||||||||||||||||||||
| Регистрационный номер CAS | 10043-35-3 | |||||||||||||||||||||||||||||||||
| Название IUPAC | борная кислота | 9024 | ||||||||||||||||||||||||||||||||
| УЛЫБКА | OB (O) O | |||||||||||||||||||||||||||||||||
| Идентификатор InChI | InChI = 1S / Bh4O3 / c2-1 (3) 4 / h3-4H | |||||||||||||||||||||||||||||||||
| FFIKLey40 KGB-ключ KGB | ||||||||||||||||||||||||||||||||||
| Химическая таксономия | ||||||||||||||||||||||||||||||||||
| Описание | относится к классу неорганических соединений, известных как различные бораты. Это неорганические соединения, в которых наибольшим оксоанионом металла является борат, с которым либо атомы, либо атомы неметалла не связаны. Это неорганические соединения, в которых наибольшим оксоанионом металла является борат, с которым либо атомы, либо атомы неметалла не связаны. | |||||||||||||||||||||||||||||||||
| Kingdom | Неорганические соединения | |||||||||||||||||||||||||||||||||
| Super Class | Смешанные соединения металлов и неметаллов | |||||||||||||||||||||||||||||||||
| Класс | Разные смеси металлов и неметаллов | |||||||||||||||||||||||||||||||||
| Подкласс | ||||||||||||||||||||||||||||||||||
| Прямой родитель | Разные бораты | |||||||||||||||||||||||||||||||||
| Альтернативные родители | ||||||||||||||||||||||||||||||||||
| Заместители |
| |||||||||||||||||||||||||||||||||
| Молекулярный каркас | Недоступно | |||||||||||||||||||||||||||||||||
| Внешние дескрипторы | ||||||||||||||||||||||||||||||||||
| Биологические свойства | ||||||||||||||||||||||||||||||||||
| Статус | ||||||||||||||||||||||||||||||||||
| Сотовая связь | ||||||||||||||||||||||||||||||||||
| Местоположение биожидкости | Недоступно | |||||||||||||||||||||||||||||||||
| Местоположение ткани | Недоступно | |||||||||||||||||||||||||||||||||
| Пути | Недоступно | |||||||||||||||||||||||||||||||||
| Химические роли | Недоступно | |||||||||||||||||||||||||||||||||
| Физические свойства | ||||||||||||||||||||||||||||||||||
| Состояние | Твердый | |||||||||||||||||||||||||||||||||
| Внешний вид | Белый порошок. | |||||||||||||||||||||||||||||||||
| Экспериментальные свойства |
| |||||||||||||||||||||||||||||||||
| Прогнозируемые свойства | ||||||||||||||||||||||||||||||||||
| Spectra | ||||||||||||||||||||||||||||||||||
| Spectra | 9024 9024 Тип Spectra | 9024 9024 View | ||||||||||||||||||||||||||||||||
| Прогнозируемый спектр ГХ-МС | Прогнозируемый спектр ГХ-МС — ГХ-МС (без производных) — 70 эВ, положительный | всплеск20-0002-00000-bbc2ef0502723cb1626red | JSpectraicted | МС / МСПрогнозируемый спектр ЖХ-МС / МС — 10 В, положительный | spl ash20-03di-00000-677c9c32b74aec8966ea | JSpectraViewer | ||||||||||||||||||||||||||||
| Прогнозируемый ЖХ-МС / МС | Прогнозируемый Спектр ЖХ-МС / МС — 20 В, положительный | splash120-03di-00000840290 | splash120-03di-00000-b1e39 ЖХ-МС / МС | Прогнозируемый спектр ЖХ-МС / МС — 40 В, положительный | всплеск 20-03di-00000-62bf52315368ab01f8d0 | JSpectraViewer | ||||||||||||||||||||||||||||
| Прогнозируемый ЖК-МС / МС | Расчетный спектр ЖХ-МС / МС | 10 В, отрицательный | splash 20-03di-00000-83fb7281cdb2fa8b9902 | JSpectraViewer | ||||||||||||||||||||||||||||||
| Прогнозируемый ЖХ-МС / МС | Прогнозируемый Спектр ЖХ-МС / МС — 20В, E403000000290BB-MS-MS | 0000 JB030000 9025-03 | ||||||||||||||||||||||||||||||||
| Прогнозируемый ЖХ-МС / МС | Прогнозируемый спектр ЖХ-МС / МС — 40 В, отрицательный | всплеск 20-03di-00000-08dde520c636be4 90 258 | JSpectraViewer | |||||||||||||||||||||||||||||||
| Недоступно | ||
| Смертельная доза | Недоступно | |
|---|---|---|
| Канцерогенность (классификация IARC) | Нет признаков канцерогенности для человека (не перечислено IARC). | |
| Использование / источники | Недоступно | |
| Минимальный уровень риска | Недоступно | |
| Влияние на здоровье | Недоступно | |
| Симптомы | 9024Y 9024Y Недоступно Лечение: промыть открытые глаза под проточной водой в течение нескольких минут. ПРОГЛАТЫВАНИЕ: не вызывать рвоту. Прополоскать рот водой (никогда не давать ничего через рот человеку без сознания).Немедленно обратитесь за медицинской помощью. КОЖА: следует немедленно обработать, промыть пораженные части в холодной проточной воде в течение не менее 15 минут, а затем тщательно промыть водой с мылом. При необходимости человек должен принять душ и сменить загрязненную одежду и обувь, а затем обратиться за медицинской помощью. ВДЫХАНИЕ: подача свежего воздуха. При необходимости сделайте искусственное дыхание.||
| Нормальные концентрации | ||
| Недоступно | ||
| Аномальные концентрации | ||
| Недоступно | ||
| Внешние ссылки | ||
| Внешние ссылки | ||
| Идентификатор соединения PubChem | 7628 | |
| Идентификатор ChEMBL | CHEMBL42403 | |
| ChemSpider ID | ||
| OMIM ID | ||
| ChEBI ID | 33118 | |
| BioCyc ID | Недоступно | |
| CTD ID | ID StD | Недоступно |
| BO3 | ||
| ACToR ID | Недоступно | |
| Ссылка на Википедию | Недоступно | |
| Справочные материалы | ||
| Синтез Справочный материал | ||
| Общие ссылки |
| |
| Регуляция гена | ||
| Гены с повышенной регуляцией | Недоступно | |
| Гены с пониженной регуляцией | Недоступно | |
| Запись информации | |||
|---|---|---|---|
| Версия | 4.0 | ||
| Статус | Ожидается, но не определено количественно | ||
| Дата создания | 2012-09-11 20:44:48 UTC | ||
| Дата обновления | 2019-07-23 06:19:23 UTC | ||
| Идентификатор HMDB | HMDB0035731 | ||
| Вторичные регистрационные номера | |||
| Идентификация метаболита | |||
| Общее название | |||
| Структура | × Структура для HMDB0035731 (Борная кислота (h4BO3))Закрыть | ||
| Синонимы | ChEBI | ||
| b (OH) 3 | ChEBI | ||
| Тригидроксид бора | ChEBI | ||
| h4BO3 | Генератор | ||
| Ортобиновая кислота | Генератор | ||
| bate (h4BO3) | Генератор | ||
| bic acid (h4BO3) | HMDB | ||
| (10b) Ортоборная кислота | HMDB | 9025 3||
| 1332-77-0 (двухкалиевая соль) | HMDB | ||
| Кислота борная | HMDB | ||
| Ant flip | HMDB | HMDB | |
| Бораковая кислота | HMDB | ||
| Борат | HMDB | ||
| Борат (b4O7 (2-)) | HMDB4 | HMDB4 | борная кислота (h410BO3)HMDB |
| борная кислота (JP15 / nf) | HMDB | ||
| борная кислота, Acs | HMDB | ||
| HMDB | |||
| Промывка глаз Collyrium | HMDB | ||
Dr. Терминатор от блох ‘S 1 DF Терминатор от блох ‘S 1 DF | HMDB | ||
| Терминатор от блох Dr.’S 1 dfpbo | HMDB | ||
| Терминатор от блох Dr.’S 1 DT | HMDB | ||
| HMDB | |||
| dtpbo | HMDB | ||
| Flea prufe | HMDB | ||
| Гептаоксотетра-борат (2-) | HMDB | ||
| Homberg3 | |||
| HMDB | |||
| Kjel-sorb | HMDB | ||
| Ортборная кислота | HMDB | ||
| Ортоборная кислота (b (OH) 3) | HMDB | ||
| Супер уничтожитель блох | HMDB | ||
| Тетраборат | HMDB | ||
| Три слона | 904 03 HMDB|||
| Trihydroxidoboron | HMDB | ||
| Trihydroxyborane | HMDB | ||
| Trihydroxyborone | HMDB | ||
| бора оксид-гидроксид | MeSH | ||
 833
833OB (O) O
InChI = 1S / Bh4O3 / c2-1 (3) 4 / h3-4H
- Борат
- Соль неорганическая
- Неорганическая соль металлоидов
Источник:
Биологическое местонахождение:
Промышленное применение:
Биологическая роль:
| Свойство | Значение | Ссылка |
|---|---|---|
| Точка плавления | 171 ° C | Недоступно |
| Точка кипения 0258 | Недоступно | |
| Растворимость в воде | 50 мг / мл при 25 ° C | Недоступно |
| LogP | 0. 18 18 | Недоступно |
| Spectrum Type | Описание | Splash Key | splash20-0002-00000-bbc2ef0502723cb1626e | Спектр | |
|---|---|---|---|---|---|
| Прогнозируемый ЖХ-МС / МС | Прогнозируемый спектр ЖХ-МС / МС Положительный | всплеск 20-03di-00000-677c9c32b74aec8966ea | Спектр | ||
| Прогнозируемый ЖХ-МС / МС | Прогнозируемый Спектр ЖХ-МС / МС — 20 В, Положительный | splash20-03DI-8000-90ff | |||
| Прогнозируемый ЖХ-МС / МС | Прогнозируемый спектр ЖХ-МС / МС — 40 В, положительный | брызги 20-03di-00000-62bf52315368ab01f8d0 | Спектр | ||
| Прогнозируемый спектр ЖХ-МС / МС | Прогнозируемый спектр ЖХ-МС / МС — 10 В, отрицательный | всплеск 20-03di-00000-83fb7281cdb2fa8b9902 | MS | MS Spectrum Прогнозируемый спектр ЖХ-МС / МС — 20 В, отрицательный всплеск 20-03di-00000-eb0715d970431bb2a1b3 | Спектр |
| Прогнозируемый ЖХ-МС / МС | Прогнозируемый ЖК-МС / МС | отрицательный всплеск 9020 В 03di-Spectrum |
Борная кислота | Энциклопедия.
 com
comОБЗОР
Борная кислота (BORE-ik ASS-id) представляет собой бесцветный, белый или бесцветный порошок или кристаллический материал без запаха, слегка маслянистый, который медленно разлагается при нагревании, превращаясь сначала в метаборную кислоту (HBO 2 ), затем к пироборной кислоте (H 2 B 4 O 7 ) и, в конечном итоге, к оксиду бора (B 2 O 3 ). Растворимость соединения во многом зависит от температуры. В холодной воде около 5 граммов (0,2 унции) борной кислоты растворяются в 100 мл (3.4 унции) воды, а при 100 ° C (212 ° F) его растворимость увеличивается до 25 граммов (0,9 унции) в 100 мл (3,4 унции) воды.
ОСНОВНЫЕ ФАКТЫ
ДРУГИЕ НАИМЕНОВАНИЯ:
Ортоборная кислота; ортоборат водорода; борная кислота
ФОРМУЛА:
H 3 BO 3
ЭЛЕМЕНТЫ:
Водород, бор, кислород
ТИП СОЕДИНЕНИЯ:
Неорганическая кислота
СОСТОЯНИЕ:
02 Твердый1AR 61. 83 г / моль
83 г / мольТОЧКА ПЛАВЛЕНИЯ:
170,9 ° C (339,6 ° F)
ТОЧКА КИПЕНИЯ:
Разлагается выше точки плавления
РАСТВОРИМОСТЬ:
Немного растворим в воде, этиловом спирте и глицерине
Борная кислота естественным образом встречается в ряде мест, где она выпала из горячих источников. Это может происходить тогда в форме минерала сассолита. Учитывая его изобилие в природе, неудивительно, что это соединение было известно и использовалось людьми на протяжении многих веков.Например, известно, что греки использовали борную кислоту в качестве антисептика, для консервирования продуктов и в качестве чистящего средства. Считается, что первым человеком, который приготовил борную кислоту в Европе, был немецкий химик Вильгельм Хомберг (1652–1715), который в 1702 году обработал натуральную буру (Na 2 B 4 O 7 · 10H 2 O). с кислотой, чтобы получить продукт, который он назвал седативной солью, вероятно, формой борной кислоты. Химическая структура соединения была определена в 1808 году французскими исследователями Луи-Жозефом Гей-Люссаком (1778–1850) и Луи-Жаком Тенаром (1777–1857).
Химическая структура соединения была определена в 1808 году французскими исследователями Луи-Жозефом Гей-Люссаком (1778–1850) и Луи-Жаком Тенаром (1777–1857).
КАК ЭТО ПРОИЗВОДИТСЯ
Наиболее распространенный метод получения борной кислоты — обработка относительно большого количества буры соляной или серной кислотой и кристаллизация борной кислоты, которая образуется в реакции. Менее распространенный метод приготовления включает обработку солевых растворов буры хелатирующим агентом, который связывается с боратами, присутствующими в рассоле, которые затем могут быть преобразованы в борную кислоту.
ОБЫЧНОЕ ИСПОЛЬЗОВАНИЕ И ПОТЕНЦИАЛЬНАЯ ОПАСНОСТЬ
Наибольшее количество борной кислоты используется в производстве термостойкого (боросиликатного) стекла, стекловолокна, фарфоровых эмалей, посуды, лабораторной посуды и других специализированных видов стекла и керамики. материалы.В 2004 году на эти цели было направлено около 80 процентов всей борной кислоты, используемой в США. Хотя на него приходится гораздо меньшее количество борной кислоты, еще одно хорошо известное применение этого соединения — это антисептик в жидких средах для глаз, мазях и жидкостях для полоскания рта. Он также используется в качестве консерванта в пищевых продуктах и как фунгицид для цитрусовых культур. В Соединенных Штатах на фруктах, обработанных борной кислотой, разрешено содержание не более 8 частей на миллион.
Хотя на него приходится гораздо меньшее количество борной кислоты, еще одно хорошо известное применение этого соединения — это антисептик в жидких средах для глаз, мазях и жидкостях для полоскания рта. Он также используется в качестве консерванта в пищевых продуктах и как фунгицид для цитрусовых культур. В Соединенных Штатах на фруктах, обработанных борной кислотой, разрешено содержание не более 8 частей на миллион.
Интересные факты
- Наиболее распространенными источниками борной кислоты являются горячие источники и вулканические объекты, такие как минеральные источники в Виши и Экс-ла-Шапель во Франции и Висбаден в Германии, вокруг вулканических регионов Тосканы в Италии и в сухих озерах Калифорнии и Невады, таких как Калифорнийское озеро Боракс.
- Борная кислота когда-то использовалась в качестве ингредиента в тальке и порошках для подгузников, а также в мазях от опрелостей из-за ее антисептических свойств. Однако в конечном итоге это соединение было запрещено для такого использования, когда регулирующие органы решили, что он слишком токсичен, если он случайно попал в организм через открытую рану или при проглатывании.
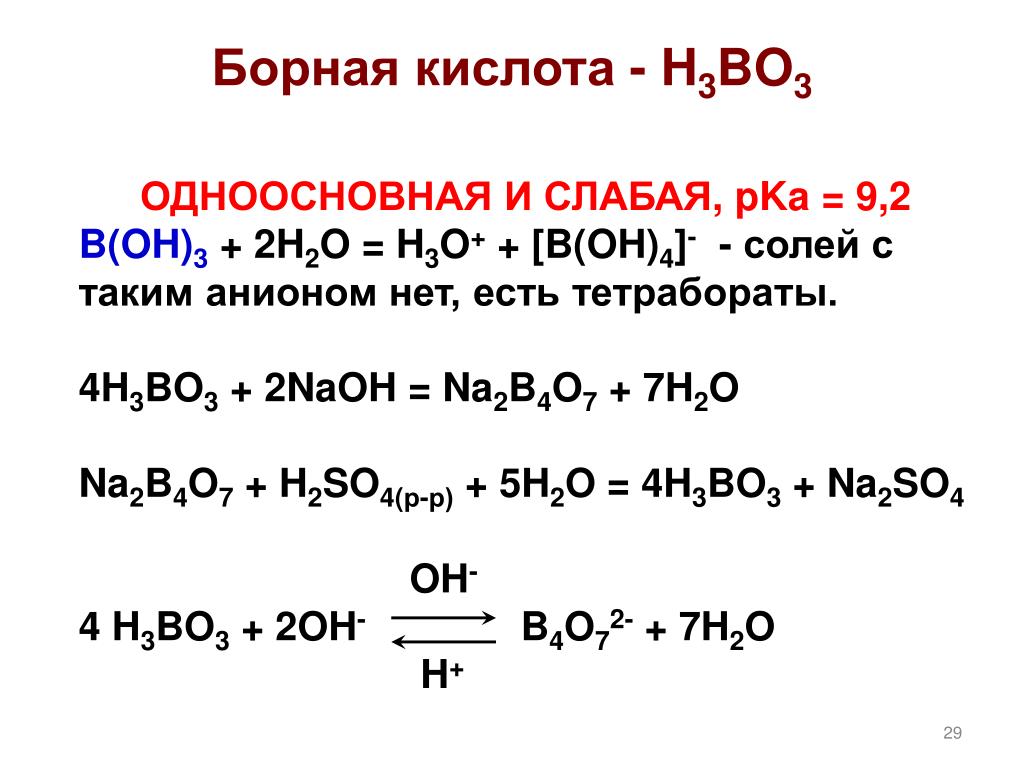
Некоторые другие важные области применения борной кислоты включают следующее:
- При производстве огнестойких материалов;
- В качестве пестицида для лечения тараканов, куропаток, термитов, блох, огненных муравьев, многоножек, кузнечиков и слизней;
- В качестве флюса при сварке и пайке;
- При синтезе многих соединений бора;
- Завершить производство кожаных и меховых изделий;
- При производстве латексных красок; и
- При никелировании металлических изделий.
Борная кислота токсична при проглатывании. Это вызывает тошноту, рвоту, диарею и спазмы желудка. В крайних случаях это может вызвать коллапс системы кровообращения, делирий, судороги, кому и смерть. Проглатывание не более 5 граммов (0,2 унции) борной кислоты может привести к смерти младенца. Проглатывание от 15 до 20 граммов (от 0,5 до 0,7 унции) взрослым также может быть смертельным. Борная кислота также может вызывать раздражение кожи, что в крайних случаях может привести к состоянию, известному как боризм. Боризм характеризуется сухостью кожи, высыпаниями на коже и слизистых оболочках и желудочными расстройствами.
Боризм характеризуется сухостью кожи, высыпаниями на коже и слизистых оболочках и желудочными расстройствами.
слов, которые нужно знать
- РАСТВОРИТЕЛЬ
- Раствор, который насыщен или почти насыщен хлоридом натрия или другими неорганическими солями.
- Хелатирующий агент
- Органическое соединение, которое связывает («захватывает») какое-то конкретное соединение или соединения, присутствующие в смеси.
- FLUX
- Материал, понижающий температуру плавления другого вещества или смеси веществ, или используемый для очистки металла.
ДОПОЛНИТЕЛЬНАЯ ИНФОРМАЦИЯ
«Бура, борная кислота и бораты». ИПМ Аляски. http://www.ipmofalaska.com/files/Borates.html (по состоянию на 12 октября 2005 г.).
«Борная кислота: техническое описание». Manufacturas Los Andes. http://www.mandes.com.ar/technic-boric-acid.php (по состоянию на 12 октября 2005 г.).
Поттер, Майк. «Устранение тараканов». Энтомологический университет Кентукки. http://www.uky.edu/Agriculture/Entomology/entfacts/struct/ef614.htm (по состоянию на 12 октября 2005 г.).
Энтомологический университет Кентукки. http://www.uky.edu/Agriculture/Entomology/entfacts/struct/ef614.htm (по состоянию на 12 октября 2005 г.).
Борная кислота — Sciencemadness Wiki
Кислота борная. Из Википедии | |
| Имена | |
|---|---|
| Название ИЮПАК Борная кислота | |
| Другие названия Борная кислота | |
| Недвижимость | |
| H 3 O 3 B | |
| Молярная масса | 61.83 г / моль |
| Внешний вид | белое твердое вещество |
| Запах | Без запаха |
| Плотность | 1,435 г / см 3 |
| Температура плавления | 170,9 ° С (339,6 ° F, 444,0 К) |
| Температура кипения | 300 ° С (572 ° F, 573 К) (разложение) |
| 2,52 г / 100 мл (0 ° C) 4,72 г / 100 мл (20 ° C) 5.  7 г / 100 мл (25 ° C) 7 г / 100 мл (25 ° C) 19,10 г / 100 мл (80 ° C) 27,53 г / 100 мл (100 ° C) | |
| Растворимость | Растворим в этаноле, метаноле Умеренно растворим в этиленгликоле, глицерине, пиридине Слабо растворим в ацетоне, этилацетате |
| Растворимость в этаноле | 9,44 г / 100 мл (25 ° C) |
| Растворимость в метаноле | 17,39 г / 100 мл (25 ° C) |
| Давление пара | ~ 0 мм рт. |
| Кислотность (p K a ) | 9.24, 12,4, 13,3 |
| Опасности | |
| Паспорт безопасности | Sigma-Aldrich |
| Летальная доза или концентрация ( LD , LC ): | |
| 2660 мг / кг (крыса, перорально) | |
| Родственные соединения | |
Родственные соединения | Borax Триоксид бора |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобокс | |
Борная кислота ( H 3 BO 3 ) является наиболее доступным соединением бора.
Недвижимость
Химическая промышленность
Борная кислота упоминается как «кислота только по названию» и даже слишком слаба, чтобы реагировать с твердыми веществами, такими как карбонат меди. Он не производит протоны в воде: вместо этого он изолирует гидроксид-ионы из раствора, образуя H 3 O и B (OH) 4 —
Борная кислота, нагретая до температуры выше 300 ° C, теряет воду с образованием в конечном итоге триоксида бора, который может использоваться в термитной реакции с магнием для получения элементарного бора.Диборид магния также производится в качестве побочного продукта.
- 4 H 3 BO 3 + 7 Mg → 2 B + MgB 2 + 6 MgO + 6 H 2 O
Он образует эфир триметилбората с метанолом, который горит бриллиантовым зеленым, и аналогично образует триэтилборат с этанолом, который также горит зеленым.
При реакции с гидроксидами щелочных металлов образуются боратные соли.
Борная кислота реагирует в спиртовом растворе с двумя молекулами куркумина с образованием розоцианина, темно-зеленого ионного твердого вещества, которое образует темно-красные растворы.
Физические
Борная кислота плохо растворяется в воде. Также он слабо растворяется в низших спиртах и ацетоне.
Наличие
Самый простой способ приобретения — в универмагах или хозяйственных магазинах, где он продается в относительно чистом виде как средство от тараканов или другие пестициды. Борная кислота также продается в аптеках.
Наконец, его также можно очень дешево купить в Интернете или у поставщиков лабораторий.
Препарат
При смешивании соляной кислоты и буры образуется борная кислота, которая из-за своей низкой растворимости выпадает в осадок в холодной воде.
Проектов
Погрузочно-разгрузочные работы
Безопасность
Поскольку это очень слабая кислота, борная кислота не вызывает коррозии, но может вызывать раздражение. Борная кислота не должна потребляться или вдыхаться в больших количествах. Следует ограничить длительное воздействие.
Борная кислота не должна потребляться или вдыхаться в больших количествах. Следует ограничить длительное воздействие.
Борная кислота легко убивает насекомых — ее часто называют убийцей тараканов.
Хранилище
Специального хранения не требуется. Можно хранить в любой чистой бутылке или сумке.
Утилизация
Небольшое количество борной кислоты можно вылить в канализацию, так как она мало токсична для окружающей среды.Большие количества следует отправлять на объекты для захоронения. Отработанная борная кислота также может использоваться как инсектицид.
Список литературы
Соответствующие темы Sciencemadness
.

 Терминатор от блох ‘S 1 DF
Терминатор от блох ‘S 1 DF (2004) Словарь пищевых соединений с CD-ROM: Добавки, ароматизаторы и ингредиенты. Бока-Ратон: Чепмен и Холл / CRC.
(2004) Словарь пищевых соединений с CD-ROM: Добавки, ароматизаторы и ингредиенты. Бока-Ратон: Чепмен и Холл / CRC. Это неорганические соединения, в которых наибольшим оксоанионом металла является борат, с которым либо атомы, либо атомы неметалла не связаны. Борная кислота (h4BO3) — это лекарственное средство. Борная кислота (h4BO3) — чрезвычайно слабое основное (по существу нейтральное) соединение (на основе его pKa). Борная кислота (h4BO3) присутствует во всех живых организмах, от бактерий до человека. Вне человеческого тела борная кислота (h4bo3) в среднем содержится в самых высоких концентрациях в гранатах. борная кислота (h4bo3) также была обнаружена, но не определена в нескольких различных продуктах, таких как инжир, французский банан и красная смородина.Это может сделать борную кислоту (h4bo3) потенциальным биомаркером для употребления этих продуктов. Он имеет ограниченное использование в качестве антибактериального средства в икре. Борная кислота (h4BO3) — потенциально токсичное соединение. Нет признаков канцерогенности для человека (не внесен в список IARC). Прополоскать рот водой (никогда не давать ничего через рот человеку без сознания).
Это неорганические соединения, в которых наибольшим оксоанионом металла является борат, с которым либо атомы, либо атомы неметалла не связаны. Борная кислота (h4BO3) — это лекарственное средство. Борная кислота (h4BO3) — чрезвычайно слабое основное (по существу нейтральное) соединение (на основе его pKa). Борная кислота (h4BO3) присутствует во всех живых организмах, от бактерий до человека. Вне человеческого тела борная кислота (h4bo3) в среднем содержится в самых высоких концентрациях в гранатах. борная кислота (h4bo3) также была обнаружена, но не определена в нескольких различных продуктах, таких как инжир, французский банан и красная смородина.Это может сделать борную кислоту (h4bo3) потенциальным биомаркером для употребления этих продуктов. Он имеет ограниченное использование в качестве антибактериального средства в икре. Борная кислота (h4BO3) — потенциально токсичное соединение. Нет признаков канцерогенности для человека (не внесен в список IARC). Прополоскать рот водой (никогда не давать ничего через рот человеку без сознания). ПРОГЛАТЫВАНИЕ: не вызывать рвоту. ВДЫХАНИЕ: подача свежего воздуха. Борная кислота (h4BO3), также называемая боратом водорода, борная кислота, борная кислота (h4BO3) — слабая кислота бора, часто используемая в качестве антисептика, инсектицида, антипирена, поглотителя нейтронов или предшественника других химических соединений.Встречаясь в виде минерала, он называется сассолитом. При необходимости человек должен принять душ и сменить загрязненную одежду и обувь, а затем обратиться за медицинской помощью.
ПРОГЛАТЫВАНИЕ: не вызывать рвоту. ВДЫХАНИЕ: подача свежего воздуха. Борная кислота (h4BO3), также называемая боратом водорода, борная кислота, борная кислота (h4BO3) — слабая кислота бора, часто используемая в качестве антисептика, инсектицида, антипирена, поглотителя нейтронов или предшественника других химических соединений.Встречаясь в виде минерала, он называется сассолитом. При необходимости человек должен принять душ и сменить загрязненную одежду и обувь, а затем обратиться за медицинской помощью.