Еще во время роста культур можно на порядок снизить в них содержание нитратов
Каждому хочется по максимуму обезопасить свой участок от накопления нитратов, солей азотной кислоты. Оказывается, есть способы, чтобы свести их к минимуму в овощах и фруктах во время роста. Но обо всем по порядку. Азот растениям необходим как воздух. Без него они просто не смогут развиваться. И хочу заметить, что культур с нулевым содержанием нитратов просто не бывает. Они все в той или иной степени накапливают их. Почему так бывает? Давайте разбираться. А поможет нам в этом кандидат сельскохозяйственных наук Анна Гордеева.У каждого свои пристрастия
Растения во время роста извлекают из почвы нитраты и превращают их в аминокислоты. Но это происходит только во время созревания плодов. Если культура не успеет израсходовать весь поступающий из почвы азот, то он в виде нитратов окажется в овощах и фруктах.Да и в течение всего сезона растения поглощают соли азотной кислоты с разной скоростью.
Надо сказать, что не все культуры одинаково накапливают нитраты. Рекордсменами считаются листовые салаты, пряные травы, свекла, зеленый лук, редис. А вот в бобовых, брюссельской капусте, сладком перце, картофеле, томатах, репчатом луке их меньше. Обратите внимание на таблицу № 1.
Да и в самом растении нитраты «разбегаются» по разным частям. Больше всего их накапливается в прожилках и стеблях, ведь именно по ним из земли поступают вода и питательные вещества. Поэтому в листовых овощах (салате, шпинате, мангольде) и пряных травах (укропе, кинзе и других) нитратов всегда больше, чем в других культурах.
В капусте, к примеру, они собираются в кочерыжке и верхних листьях.
У огурца, патиссона и кабачка соли азотной кислоты активно накапливают оба их конца и кожура. Но чем ближе к семенам, тем их меньше.
У моркови самые нитратные светлая сердцевина и верхняя часть. У баклажана — мякоть ближе к плодоножке. Картофель активно накапливает соли азотной кислоты под кожурой и в сердцевине клубня.
В тыкве больше всего нитратов возле плодоножки, а также в семенной камере. Мало их и в арбузной мякоти, да и распределены они равномерно. А вот в кожуре — побольше.
Длинноплодный редис припасает нитратов больше, чем округлой формы. Особенно в нижней части, в серединке их поменьше. Также тепличный редис более нитратозависимый, чем выращенный на улице.
У гороха нитратами насыщены молодые стручки, причем чем выше по стеблю они расположены, тем вредных солей больше.
У репчатого лука меньше всего их в средней части, зато очень много вверху и внизу, особенно в донце. Зеленый же лук больше всего накапливает нитратов в нижней части пера, примыкающей в луковице.
Зеленый же лук больше всего накапливает нитратов в нижней части пера, примыкающей в луковице.
У столовой свеклы запасы нитратов в сердцевине и на кончике корня. И в крупных (более 100 г) корнеплодах вредных солей больше, чем в мелких.
Содержание нитратов зависит от возраста растений. Допустим, молодые морковь и свекла, убранные в июле как «пучковый товар», более нитратные, чем полностью вызревшие. Есть разница и по сортам: ранние более активно накапливают соли азотной кислоты.
Вносит свою лепту погода. В условиях влажного и прохладного лета даже при использовании исключительно органических удобрений содержание нитратов в почве и растениях увеличивается. Больше накапливается их и во время засухи. Да и вообще любые температурные качели не на пользу. Чем чаще растения страдают от перепада температур (от 8 градусов и больше), тем обильнее накапливают вредные соединения. Защитить посадки можно, выращивая их в теплице или парнике. Или хотя бы под укрытием, чтобы в случае резких похолоданий или на ночь выставлять над самыми нежными культурами дуги и набрасывать на них спанбонд или пленку.
Доказано, что на содержание нитратов в овощах существенное влияние оказывает и почва. И чем богаче она гумусом, тем их больше.
Но, как правило, первопричина повышенного содержания солей азотной кислоты в овощных и зеленных культурах — все же нарушение агротехники, в частности злоупотребление азотными удобрениями (таблица № 2). Причем под подозрение попадают не только минеральные, но и органические. Навоз, к примеру. Поэтому использовать его как подкормку можно только после компостирования. А за 35 — 45 дней до сбора урожая нужно вообще прекратить азотные подкормки. Чтобы овощи не набрали лишних нитратов, перед внесением азота кислую почву обязательно известкуют.
Минеральные удобрения нужно вносить вместе с органическими, заранее перемешав их для более равномерного распределения по грядке. Такая комбинация оптимизирует поступление азота и не позволит растениям создать из него запасный фонд нитратов.
На пользу посадкам и сидераты, особенно смеси трав — вико-овсяная или горохово-овсяная. Благодаря им солей азотной кислоты будет в 1 — 2 раза меньше, чем при использовании только одних минеральных удобрений.
Благодаря им солей азотной кислоты будет в 1 — 2 раза меньше, чем при использовании только одних минеральных удобрений.
Хороший эффект дает включение в огородный «рацион» травяных настоев. Их готовят из люпина, клевера, одуванчика, лебеды, крапивы и других сорняков. А если по осени их зеленую массу заделать в почву, перемешав с толченым углем или золой, то весной азотные удобрения можно и не вносить на участок.
Калий против азота
Отличными помощниками в борьбе с нитратами могут стать калийные удобрения: они снижают негативный эффект от избытка азота. Причем на всех культурах. Фосфорные же практически не влияют на накопление солей азотной кислоты. Но в то же время если их активно использовать вместе с азотом, то нитраты будут просто зашкаливать.Под запретом азотные удобрения и во второй половине вегетации — с середины июля. Мало того что растение, забыв о плодах, начинает активно гнать зеленую массу, так еще резко возрастает и количество нитратов. Опытами установлено, что азотная подкормка в конце июля — начале августа в 1,2 — 1,5 раза повышает их содержание в капусте, моркови и столовой свекле.
А вот калий, снижающий их накопление, наоборот, лучше всего вносить во второй половине вегетации, когда происходит синтез запасных веществ и растение активно аккумулирует витамины, сахара и сухие вещества. Также ускоряют расход азотных удобрений подкормки, содержащие железо и молибден.
Между болезнью растений и находящимися в них нитратами есть прямая связь. Здоровые культуры дают и более чистый урожай. Ведь во время созревания азотные соединения успевают переработаться в полезные белки. Поэтому в любимых всеми молодых огурчиках нитратов намного больше, чем в полностью созревших. Но в переросших и перезревших зеленцах их еще больше.
Очень много нитратов накапливается и в плодах с механическими повреждениями. «Раненый» овощ — больной овощ.
Не лучший союзник в борьбе за чистые продукты и тень. Если растению не хватает света, оно не полностью перерабатывает нитраты, что приводит к их накоплению. Поэтому старайтесь прореживать посадки и не допускайте зарастания грядок и междурядий сорняками, не только затеняющими культурные растения, но и отнимающими у них питание.
Даже если в вашем огородном сезоне все было совсем не так, как задумывалось, содержание нитратов можно снизить даже в почти готовой продукции. Во-первых, растения можно… обмануть, преподнеся им вместо азота регуляторы роста. За 2 — 3 недели до уборки урожая обработайте посадки «Эпином Экстра», «Цирконом», «Экосилом», «Гуматом натрия» или другим аналогичным препаратом. Рост растений не прекратится, а нитраты не будут накапливаться.
Еще один способ улучшить состояние культур, особенно зеленных, — обильный полив за 2 — 3 дня до срезки. Да и сам сбор желательно проводить вечером, после захода солнца. Ночная срезка в сочетании с поливом почти наполовину снизит содержание нитратов в зелени. Не единожды проверено и доказано, что в собранных утром плодах солей азотной кислоты всегда больше, чем в срезанных вечером.
Зависит нитратный показатель и от условий хранения выращенных овощей и картофеля. Если все сделано правильно, то через полгода содержание в них нитратов снизится в 2,5 — 3 раза.
Умная готовка
Можно снизить количество нитратов и в уже собранном урожае. Для этого овощи и зелень надо хотя бы полчаса подержать в холодной воде. За это время соли азотной кислоты перейдут в воду и в продуктах их станет заметно меньше. Также наполовину уменьшит их количество и термическая обработка. При варке овощей воду после закипания лучше слить и добавить новую, в которой и продолжать готовить. Правда, при этом возрастают потери полезных веществ. Варка на пару в меньшей степени снижает количество нитратов в готовом продукте. Бланшировка, тушение и жарка вообще практически не меняют их концентрацию в блюде. Замедляют выход нитратов подсаливание и добавление специй. Поэтому соль и приправы лучше вносить в конце варки.Сочные овощи (томаты, перец, огурцы, редис и т. д.) желательно кушать свежими. Чем дольше они хранятся, тем больше в них (в результате испарения влаги) накапливается вредных веществ. В маринованных плодах нитратов заметно меньше, чем в свежих: не нужные нам соли переходят в рассол.
д.) желательно кушать свежими. Чем дольше они хранятся, тем больше в них (в результате испарения влаги) накапливается вредных веществ. В маринованных плодах нитратов заметно меньше, чем в свежих: не нужные нам соли переходят в рассол.
Зелень (петрушку, сельдерей, укроп, мяту) лучше хранить в засушенном или замороженном виде. А если убрать стебли, то количество нитратов уменьшится еще на 15 — 20 процентов.
Снизить риск от потребления нитратов можно и во время еды, например, запивая салат из листовой зелени любым соком или напитком с высоким содержанием витамина С. Аскорбиновая кислота блокирует переход нитратов в более вредные нитриты.
ФАКТ
В плоде нитратов много, если:
♦ огурец насыщенного темно-зеленого цвета, пустой внутри и желтоватый на разрезе,
♦ корнеплоды растрескались,
♦ у зелени стебли мощные и темно-зеленые,
♦ у томата волокна желтоватого цвета и очень заметные,
♦ разрезанное яблоко долго не темнеет,
♦ у внешне зрелого плода нет ни вкуса, ни аромата,
♦ семена не вызрели,
♦ кожура толстая.
КСТАТИ
У здорового человека природой предусмотрен механизм восстановления гемоглобина. Но при пониженной кислотности желудочного сока, проблемах с печенью или почками (а если еще и нитратов поступает слишком много) система защиты не срабатывает — затрудняется дыхание, нарушается обмен веществ.
Всемирная организация здравоохранения считает допустимым потребление в сутки не более 5 мг нитратов на 1 кг массы тела.
Определение нитратов в растениях. Количественное определение нитратов в продуктах растительного происхождения
Текст работы размещён без изображений и формул.
Полная версия работы доступна во вкладке «Файлы работы» в формате PDF
Введение
Актуальность:
Проблема нитратов активно обсуждается общественностью нашей страны, но что это такое на самом деле, насколько они опасны, не каждый до конца разбирался.
Нитраты — это соли азотной кислоты, которые поглощаются растениями из почвы, превращаясь потом в растительные белки. Если же их содержание в продуктах очень большое, то они, попадают в организм не в виде белка, а в «чистом» виде», даже если полностью отказаться от применения удобрений, то наличие нитратов в растительных плодах останется неизменным.
Нитраты существовали на земле задолго до появления человека, без них, невозможна сама жизнь. Они (нитраты) являются источником азота, имеющего большое значение в жизни растений. Зачастую, их используют для нормального снабжения растений азотом, которое повышает интенсивность фотосинтеза, увеличивает ассимиляционную поверхность листьев и срок их жизни.
В малых количествах нитраты постоянно присутствуют в организме человека, как и в растениях, и не вызывают негативных явлений, но при неправильном применении азотистых удобрений в большей степени овощи и фрукты накапливают в себе опасное для человеческого организма количество нитратов.
Но главными помощниками в борьбе с нитратами являются витамины.
Витамины — активные химические соединения, участвующие в обмене веществ организма и поддерживающие нормальный гомеостаз. Одним из самых нужных и важных для здоровья человека витаминов является аскорбиновая кислота — Витамин С (аскорбиновая кислота).
В чем полезные свойства витамина С? Он участвует в процессах кроветворения, благотворно влияет на функции иммунной, нервной системы, является стимулятором в работе эндокринных желез, без его участия невозможно нормальное усвоение железа. Также витамин С обладает мощными антиоксидантными свойствами, борется со свободным радикалами и выводит их из организма.
Цель:
Выявить особенности содержания нитратов в плодах различных овощных культур.
Задачи:
Определить концентрацию нитратов в плодах различных овощных культур.
Установить наиболее безопасные в отношении нитратов плоды овощных культур.
Глава 1. Литературный обзор
Проблема распространения нитратов в природе
Нитраты и нитриты широко распространены в окружающей среде, главным образом в почве и воде. Они являются элементом питания растений, а также естественным компонентом пищевых продуктов растительного происхождения. Высокая концентрация нитратов в почве абсолютно не токсична для растений, наоборот, она способствует усиленному росту растений, более активному протеканию процесса фотосинтеза, и в конечном итоге — более высокому урожаю.
Основным источником азота для растений являются соли азотной кислоты (нитраты) и соли аммония.
В естественных условиях питание азотом происходит путём потребления растениями аниона NO 3 — и катиона NH 4 + , находящихся в почвенном растворе и в обменно-поглощенном почвенными коллоидами состоянии. Поступившие в растения минеральные формы азота проходят сложный цикл превращения, в конечном итоге включаясь в состав органических азотистых соединений — аминокислот, амидов и, наконец, белка. Синтез органических азотистых соединений происходит через аммиак, образованием его завершается и их распад.
Синтез органических азотистых соединений происходит через аммиак, образованием его завершается и их распад.
Нитратный азот не может непосредственно использоваться растениями для синтеза аминокислот.
Нитраты в растениях изначально подвергаются ступенчатому — через нитрит, гипонитрит и гидроксиламин — ферментативному восстановлению до аммиака:
Восстановление нитратов происходит с участием ферментов, содержащих микроэлементы — молибден, медь, железо и марганец,— и требует затрат энергии, аккумулируемой в растениях при фотосинтезе и окислении углеводов. Восстановление нитратов в растениях осуществляется по мере использования образующегося аммиака на синтез органических азотистых соединений. Они являются естественными продуктами обмена азотистых веществ любого живого организма — растительного и животного, поэтому продуктов, не содержащих нитраты, в природе не бывает. Даже в организме человека в сутки образуется и используется в обменных процессах 100 мг и более нитратов. Из них, ежедневно попадающих в организм взрослого человека, 70% поступает с овощами, 20% — с водой и 6% — с мясом и консервированными продуктами.
Условия азотного питания оказывают большое влияние на рост и развитие растений. При достаточном снабжении растений азотом в них усиливается синтез органических азотистых веществ. Растения образуют мощные листья и стебли с интенсивно-зеленой окраской, хорошо растут и кустятся; улучшается формирование и развитие органов плодоношения. В результате — резко повышаются урожай и содержание в нём белка. Однако при одностороннем избытке азота задерживается созревание растений, они образуют большую вегетативную массу, но мало зерна или клубней и корнеплодов; у зерновых и льна избыток азота может вызывать полегание.
При недостатке азота — рост растений резко замедляется, листья бывают мелкие, бледно-зеленой окраски, что связано с нарушением синтеза хлорофилла, преждевременно желтеют, стебли становятся тонкими и слабо ветвятся. Ухудшаются также формирование и развитие репродуктивных органов и налив зерна, сильно снижаются урожай и содержание белка в нём.
Избыточное количество нитратов вызывает не нормальный ход функционирования природных экосистем и живых организмов, происходит снижение биологической ценности продукции и возрастает негативное воздействие на человека и животных.
Образование и накопление нитратов в почве и в воде становится экологическим фактором, определяющим не только режим питания растений, обмен веществ и продуктивность, но и качество урожая, воды и воздуха. Содержание нитратов в избыточных количествах ухудшает биологическое качество растительной продукции, создает потенциальную опасность для здоровья человека и животных. Ярким примером может послужить их действие на развитие вредной микрофлоры кишечника, что приводит к попаданию в организм человека токсинов, т.е. ядовитых веществ, интоксикации и отравлению организма.
Нитраты заметно снижают концентрацию витаминов, которые, в свою очередь, способствуют сопротивляемости организма неблагоприятным воздействиям внешней среды, в результате чего замедляется обмен веществ в организме. 4
4
Проблема содержания нитратов в овощах и меры по их предотвращению
Нитраты (соли азотной кислоты) — это необходимый атрибут круговорота азота в природе, важная часть азотного питания растений, без которых невозможны сложные биологические процессы синтеза белка. Сами нитраты в растениях восстанавливаются до нитритов, которые, подвергаясь дальнейшим превращениям, дают аммиак (Nh4), основу питания растений.
Азот необходим растениям для строительства белка. Если его недостаточно, растения становятся бледными, их листья желтеют. В них замедляется или полностью прекращается синтез хлорофилла, такое заболевание называется хлороз.
В почве азот накапливается очень медленно. Ежегодно снимая урожай, человек получает значительную часть азотных соединений из почвы. Они не успевают там восстанавливаться, и их содержание все время падает. Получить высокий урожай без достаточного количества азота в почве невозможно.
Само по себе присутствие нитратов в растениях — нормальное явление, но излишнее увеличение их крайне нежелательно, т. к. они обладают высокой токсичностью для человека, вернее, их восстановленная форма — нитриты.
к. они обладают высокой токсичностью для человека, вернее, их восстановленная форма — нитриты.
По нормам Всемирной организации здравоохранения (ВОЗ), допустимой суточной дозой нитратов является 5 мг на 1 кг веса. Если взять за средний вес человека 75 кг, то получится допустимая дневная доза — 375 мг.
Накопление нитратов в овощах зависит не только от доз и сроков внесения минеральных подкормок, но и от своих биологически-видовых особенностях и способностей к накоплению нитратов. Среди факторов внешней среды на их содержание в растениях больше всего влияет влажность, свет, температура воздуха и почвы, которые, действуя в комплексе, усиливают или ослабляют свое взаимодействие.
Так же изменение влажности сильно сказывается на накоплении нитратов, интенсивное увлажнение почвы усиливает поглощение нитратов корнями, что в сочетании с пониженными температурами ведёт к избыточному накоплению нитратов.
В снижении их содержания в овощной продукции может помочь выбор оптимальных сроков уборки урожая. Так, уборку листовых овощей следует проводить в вечерние часы, так как в это время в них содержится на 30—40% меньше нитратов. 5
Так, уборку листовых овощей следует проводить в вечерние часы, так как в это время в них содержится на 30—40% меньше нитратов. 5
Существуют простые способы уменьшения содержания нитратов:
Тщательно промывать овощи и фрукты — уменьшает на 10%;
Механическая очистка — на 15-20%;
Варка овощей, особенно очищенных и нарезанных, — на 50%;
Зелень вымачивать перед употреблением в холодной воде 1-1,5 часа — 20-30%;
Уменьшается содержание нитратов при квашении, солении, мариновании.
В этом случае основное средство профилактики — сокращение сроков хранения.
Все салаты, а особенно овощные соки и пюре для детей, следует готовить или вскрывать консервированные непосредственно перед употреблением.
При необходимости готовые продукты хранить лучше в холодильнике, и не больше суток. Стерилизация (кипячение) соков, супов — убивая микрофлору, также подавляет образование нитритов.
Приобретая овощные культуры в магазине или на рынке, мы не знаем всех подробностей ухода за ними. Поэтому выбор овощей стоит производить грамотно и правильно.
Поэтому выбор овощей стоит производить грамотно и правильно.
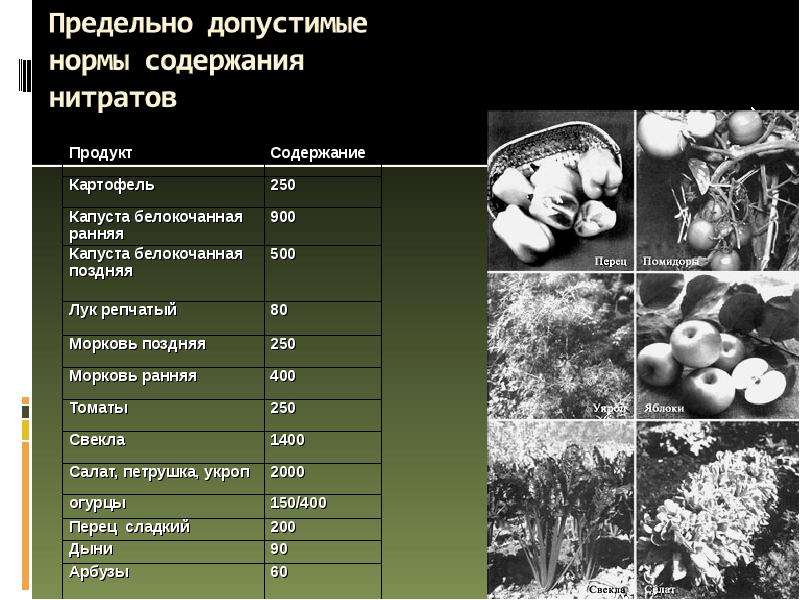
Предельно допустимые концентрации содержания нитратов в овощах
Предельно допустимые концентрации нитратов в продуктах растениеводства
(данные института питания РАМН)
Продукт | |
Картофель | |
Капуста белокочанная ранняя | |
Капуста белокочанная поздняя | |
Морковь ранняя | |
Морковь поздняя | |
Томаты | |
Огурцы | |
Свекла столовая | |
Лук репчатый | |
Листовые овощи (салат, петрушка, укроп) | |
Перец сладкий | |
Кабачки | |
Баклажаны | |
Дыни | |
Редис | |
Арбузы | |
Виноград | |
Яблоки, груши |
Индивидуальные особенности некоторых овощных культур в отношении накопления нитратов.

Накопление нитратов носит наследственно закрепленный характер. Зерновые культуры практически не накапливают нитратов. Среди семейств овощных культур наибольшей способностью к накоплению нитратов отличаются Капустные, Тыквенные, Сельдерейные.
Наибольшее количество нитратов накапливают: редька, свекла столовая, капуста, салат шпинат, редис, картофель.
Томаты, перец сладкий, баклажан, чеснок, горох — отличаются низким содержанием нитратов- 20-300 мг/кг.
У ряда овощных и бахчевых культур выявлена сортовая специфика накопления нитратов.
Видовые и сортовые различия по накоплению нитратов обусловлены генетически закрепленными возможностями редуцирующей системы растений, в частности уровнем нитратредуктазной активности, а также разной реакцией на условия окружающей среды и режим минерального питания.
Видовые различия накопления нитратов часто обусловлены локализацией нитратов в отдельных органах растений, что, в свою очередь, связано с физиологической специализацией и морфологическими особенностями отдельных органов, типом и расположением листьев, размером листовых черешков и жилок, диаметром центрального цилиндра в корнеплодах.
Нитраты практически отсутствуют в зерне злаков и сосредоточены, в этом случае, в листьях и стеблях. Зеленые культуры накапливают большое количество нитратов в стеблях и черешках листьев. Это вызвано тем, что стебли и черешки являются путями транспорта нитратов к другим органам растений.
Накопление нитратов меняется в зависимости от типа органа растения. В клубнях картофеля низкий уровень содержания нитратов обнаружен в мякоти клубня, тогда как в кожуре и сердцевине их содержание было больше по сравнению со средней частью в 1-1,3 раза.
Сердцевина, кончик и верхушка столовой свеклы отличаются от остальных частей корнеплода повышенным содержанием нитратов.
В белокочанной капусте наибольшая концентрация нитратов наблюдается в верхней части стебля. Верхние листья содержат в два раза больше нитратов, больше, чем внутренние. Особенно велико содержание нитратов в черешках листьев.
В моркови высокое содержание нитратов наблюдается в верхушке и на конце корнеплода, а также в сердцевине, причем содержание нитратов уменьшается от кончика к верхушке.
Глава 2. Объекты и методы исследования
2.1. Экспресс-метод определения нитратов в плодах овощных культур
Самым оптимальным методом является измерение нитратов приборами предназначенными для данных целей. Но также возможно выбирать овощи без специальных устройств.
Как выбрать овощи не содержащие нитраты без вспомогательных приборов?
Так как, допустимая суточная доза нитратов для взрослого человека составляет 325 мг в сутки, то чтобы уложиться в эти допуски (300 — 325 миллиграммов нитратов в сутки), совсем необязательно иметь собственные дорогостоящие приборы для определения нитратов или ходить за покупками с индикаторными бумажками. Положитесь на государственный контроль, который, конечно, не без трудностей, но постепенно повсеместно налаживается, и воспользуйтесь нашими советами.
Первым признаком наличия нитратов является «химический» цвет — слишком яркий, искусственный. Старайтесь употреблять овощи с естественной окраской.
Второй признак — размер . Они отличаются, прежде всего размером: минимальное содержание нитратов чаще бывает в овощах среднего размера, Большинство мелких плодов — преимущественно молодые растения, для которых характерен избыток нитратов, как запас на будущее. Необычно крупные плоды — часто результат избыточного питания, в том числе и азотного. После этого следует оценить содержание нитратов индикаторными бумагами.
По количеству нитратов овощи сильно отличаются как внутри одной партии, так в разных партиях. Поэтому выбрать малонитратные овощи можно всегда, особенно в период массовой уборки.
Третий признак содержания химии в овощах и фруктах — это запах . Большинство овощей и фруктов не пахнут. Они напичканы нитратами и прочей химией.
Четвертый признак — вкус . Плоды горьковатого вкуса или вообще безвкусные также не стоит покупать.
Таким образом, мы можем немного управлять содержанием нитратов в продуктах потребления, но следует помнить, что вместе с нитратами ликвидируются и витамины.
Введите в свой рацион ягоды и фрукты, которые являются висячими плодами, в них нитратов мало.
Употребление зеленого чая может нейтрализовать нитраты, которые уже попали в организм. 10
Глава 3. Экспериментальное исследование
3.1 Особенности содержания нитратов в плодах различных овощных культур
Для измерения нитратов в овощах был использован прибор «СОЭКС Нитрат тестер». Количество нитратов в овощах измерялось в мг/кг. Результаты исследования заносим в таблицу.
Название овоща | Предельная норма | Итог мг/кг | |||||
Томат сорт | |||||||
Томат сорт Джина | |||||||
Огурец сорт Бенефис | |||||||
Лук сорт Золотистый | |||||||
Картофель сорт Невский | |||||||
Морковь сорт Лосиноостр-ская | |||||||
Баклажан сорт Алмаз | |||||||
Кабачок сорт Грибовский | |||||||
Перец сладкий сорт Ласточка | |||||||
Редис сорт Селеста |
Предельно допустимые концентрации нитратов в продуктах растениеводства (см. в пункте 1.3)
в пункте 1.3)
Выводы:
Результаты наших исследования показали, что наибольшая концентрация нитратов содержится в сладком перце, картофеле и редисе, при этом для данных культур характерно высокое содержание нитратов. Перец сладкий сорт Ласточка (при ПДК 200мг/кг)-167,4мг/кг; картофель сорт Невский (при ПДК 250 мг/кг)-165,2мг/кг; редис сорт Селеста (при ПДК 1500 мг/кг)-160,4 мг/кг (см. Приложение 1)
Наибольшее превышение ПДК по нитратам нами отмечено у лука сорта Золотистый на 31,8 мг/кг (см. Приложение 1)
Таким образом нами установлено наименьшая концентрация нитрата характерная для моркови сорта Лосиноостровская (46,8 мг/кг) и баклажана сорта Алмаз (66,8 мг/кг), поэтому все исследованные сорта образцы можно считать экологически безопасными в этом отношении, за исключением лука сорта Золотистый, где нами отмечено превышение нитратов, при норме 80 мг/кг, более чем на 30 мг/кг, что можно объяснить, как индивидуальными особенностями данного сорта в отношении накоплений нитратов, так и почвенно-климатическими условиями его выращивания (см. Приложение 1)
Приложение 1)
Приложение 1
Список используемой литературы
Иванова И.В. «Вредное воздействие нитратов и нитритов на организм человека»
Тиво П.Ф, Саскевич Л.А. «Нитраты. Слухи и Реальность»
Пагуже Г.В. «Химия и повседневная жизнь человека»
Харьковская Н.Л, Лященко Л.Ф, Барышова Н.В. «Острожно- нитраты!»
Варкошкина Н.М. «Нитраты в растенях»
Лихолат Т.В. «Снижение нитратов в продукции растениеводства. Школа и производство»
Соколов О. Нитраты — под строгий контроль. Наука и жизнь
Сельскохозяйственный словарь-справочник. — Москва — Ленинград: Государстенное издательство колхозной и совхозной литературы «Сельхозгиз». Главный редактор: А. И. Гайстер. 1934.
Само по себе присутствие нитратов в растениях — нормальное явление, т.к. они являются источниками азота в этих организмах, но излишнее увеличение их крайне нежелательно, т.к. они (как мы уже знаем) обладают высокой токсичностью для человека сельско-хозяйственных животных.
Нитраты в основном скапливаются в корнях, корнеплодах, стеблях, черешках и крупных жилках листьев, значительно меньше их в плодах.
Нитратов также больше в зеленых плодах, чем в спелых. Из разных сельско-хозяйственных растений больше всего нитратов содержится в салате (особенно в тепличном), в редьке, петрушке, редисе, столовой свёкле, капусте, моркови, укропе:
- · в свекле и моркови больше нитратов в верхней части корнеплода, а в моркови также и в сердцевине его.
- · в капусте — в кочерыжке, в толстых черешках листьев и в верхних листьях.
Выяснено также, что у всех овощей и плодов больше всего содержатся нитраты в их кожице.
По способности накапливать нитраты овощи, плоды и фрукты делятся на 3 группы (2) :
- 1. с высоким содержанием (до 5000мг/кг сырой массы): салат, шпинат, свекла, укроп, листовая капуста, редис, зелёный лук, дыни, арбузы.
- 2. со средним содержанием (300-600мг): цветная капуста, кабачки, тыквы, репа, редька, белокачанная капуста, хрен, морковь, огурцы.

- 3. с низким содержанием (10-80мг): брюссельская капуста, горох, щавель, фасоль, картофель, томаты, репчатый лук, фрукты и ягоды.
С физиологической точки зрения, количество нитратного азота в растениях определяется соотношением:
- · процессов поглащения;
- · транспорта;
- · ассимиляции;
- · распределения его в разных органах и частях растения.
И все эти процессы обусловлены совокупностью почвенно-экологических условий, агротехнических и генетических факторов.
Таким образом, накопление нитратов в растениях зависит от комплекса многих причин:
- 1. от биологических особенностей самих растений и их сортов. Выяснено, что больше всего нитратов содержится в редисе сорта “Красный великан” по сравнению с другими её сортами (“розовый с белым кончиком”, “жара” и др.). Содержание нитратов зависит и от возраста растений: в молодых органах их больше (кроме шпината и овса). Меньше накапливается нитратов в гибридных растениях.
 Нитратов больше в ранних овощах, чем в поздних.
Нитратов больше в ранних овощах, чем в поздних. - 2. от режима минерального питания растений. Так, микроэлементы (особенно молибден) снижают содержание нитратов в редисе, редьке и цветной капусте; цинк и литий — в картофеле, огурцах и кукурузе. Уменьшается содержание нитратов в растениях и в результате замены минеральных удобрений на органические (навоз, торф и др.), которые постепенно разлагаются и усваиваются растениями. Органические удобрения положительно влияют на капусту, морковь, свеклу, петрушку, картофель, шпинат. Нерациональное, халатное использование химических удобрений, чрезмерные дозы их приводят к сильному накоплению нитратов, особенно в столовых корнеплодах. Содержание нитратов возрастает сильнее при использовании нитратных удобрений (KNO3, NaNO3, Ca(NO3)2 ), чем при употреблении аммонийных. За последние годы (со слов руководителя лаборатории пищевой токсикологии института питания Т.С.Хотимченко) произошло существенное снижение нитратов в продуктах отечественного растеневодства по причине меньшего использования химических удобрений в виду их дороговизны.
 Если в 1988-89 годах ПДК по нитратам превышал 15% у овощей, то теперь — не более 3%.
Если в 1988-89 годах ПДК по нитратам превышал 15% у овощей, то теперь — не более 3%. - 3. Накопление нитратов зависит и от факторов окружающей среды (температуры, влажности воздуха, почвы, интенсивности и продолжительности светового освещения):
- 4. чем длиннее световой день, тем меньше нитратов в растениях;
- 5. при влажном и холодном лете (1985г.) количество нитратов увеличилось в 2,5 раза.
- 6. при повышении температуры до 20°С количество нитратов снизилось в столовой свекле в 3 раза. Нормальная освещённость растений снижает содержание нитратов, поэтому в тепличных растениях нитратов больше (10)
Содержание нитратов в растениях зависит и от свойств почвы. Чем богаче гумусом и общим азотом почва, тем больше накапливаются нитраты в корнеплодах моркови. На содержание нитратов влияют и условия хранения растений. Установлено, что при хранении овощей в открытых ёмкостях вместе с гнилыми овощами увеличивается содержание нитратов в них, а также не следует перерабатывать корнеплоды моркови или плоды томатов, повреждённые гнилью. Лучше употреблять овощи своего сезона, т.е. когда овощи выросли под открытым небом, а не в теплице зимой. Овощи, богатые нитратами следует хранить в течении короткого времени и, желательно, в прохладном и тёмном месте. Нельзя хранить овощи битые, повреждённые. Овощи лучше собирать с огорода вечером.
Лучше употреблять овощи своего сезона, т.е. когда овощи выросли под открытым небом, а не в теплице зимой. Овощи, богатые нитратами следует хранить в течении короткого времени и, желательно, в прохладном и тёмном месте. Нельзя хранить овощи битые, повреждённые. Овощи лучше собирать с огорода вечером.
При употреблении фруктов в пищу мы должны внимательно следить за их качеством. Чтобы яблоки дольше хранились, их покрывают эмульсионным налётом и насыщают консервантами. Такие яблоки внешне очень привлекательны, но порой в них нет ни вкуса, ни запаха, ни живой сочности, а консерванты в них убивают в кишечнике человека его полезную микрофлору. Такие же консерванты используются и для хранения других продуктов (растительного масла, сосисок, колбас). Поэтому надо бдительно следить за сертификатами импортных продуктов.
Вопрос накопления нитратов в растениях нашей области стал изучаться СахНИИ с/х с 1989 года, сотрудники которого выяснили, что на Сахалине в связи с особыми агрометеорологическими условиями содержание нитратов в растениях увеличивается:
- 1.
 большое количество дней, частые туманы;
большое количество дней, частые туманы; - 2. заниженная солнечная радиация;
- 3. более низкие температуры воздуха и почвы;
- 4. сильные ветра.
Способы снижения вреда нитратов в растениях на организм человека.
Очень важно не только знать в каких растениях, в каких их органах и частях содержатся в основном нитраты, но и не менее важно надо знать, как уменьшить содержание этих ядовитых веществ для организма, поэтому предлагается ряд ценных советов:
- 5. Снижается количество нитратов при термической обработке овощей (13) (мойке, варке, жарке, тушении и бланшировке). Так, при вымачивании — на 20-30%, а при варке на 60-80%.
- § в капусте — на 58%;
- § в столовой свекле — на 20%;
- § в картофеле — на 40%.
При этом следует помнить, что при усиленной мойке и бланшировании (обваривании кипятком) овощей в воду уходят не только нитраты, но и ценные вещества: витамины, минеральные соли и др.
- 4. Чтобы снизить количество нитратов в старых клубнях картофеля, его клубни следует залить 1%-ным раствором поваренной соли.

- 5. У паттисонов, кабачков и баклажанов необходимо срезать верхнюю часть, которая примыкает к плодоножке.
- 6. Т.к. нитратов больше в кожуре овощей и плодов, то их (особенно огурцы и кабачки) надо очищать от кожуры, а у пряных трав надо выбрасывать их стебли и использовать только листья.
- 7. У огурцов, свеклы, редьки к тому же надо срезать оба конца, т.к. здесь самая высокая концентрация нитратов.
- 8. Хранить овощи и плоды надо в холодильнике, т.к. при температуре +2°С невозможно превращение нитратов в более ядовитые вещества — нитриты.
- 9. Чтобы уменьшить содержание нитритов в организме человека надо в достаточном количестве использовать в пищу витамин С (аскорбиновую кислоту) и витамин Е , т.к. они снижают вредное воздействие нитратов и нитритов (4).
- 10. Выяснено, что при консервировании уменьшается на 20-25% содержание нитратов в овощах, особенно при консервировании огурцов, капусты, т.к. нитраты уходят в рассол и маринад, которые поэтому надо выливать при употреблении консервированных овощей в пищу.

- 11. Салаты следует готовить непосредственно перед их употреблением и сразу съедать, на оставляя напотом.
Азот — это один из самых важнейших химических элементов в жизни растений, т.к. он необходим для синтеза аминокислот, из которых образуются белки. Азот получает растение из почвы в виде минеральных азотных солей (нитратных и аммиачных).
В растениях азот подвергается сложным превращениям.
Метаболизм азота в растениях — это сложный процесс, и нитраты занимают в нём промежуточное положение:
HNO 3 – HNO 2 – (HNO) 2 – NH 2 OH + NH 3
(нитрат) (нитрит) (гипонитрит) (гидроксиламин) (аммиак)
Нитраты в растениях восстанавливаются до нитритов. В этом процессе участвуют различные металлы (молибден, железо, медь, марганец), и при этом происходит интенсивная трата углеводов, т.к. на восстановление тратится энергия, источником которой являются углеводы. Нитриты могут накапливаться в растениях и этим подавлять их рост. Но основная часть нитритов, подвергаясь дальнейшим превращениям, даёт аммиак (Nh4).
Но основная часть нитритов, подвергаясь дальнейшим превращениям, даёт аммиак (Nh4).
Само по себе присутствие нитратов в растениях — нормальное явление, т.к. они являются источниками азота в этих организмах, но излишнее увеличение их крайне нежелательно, т.к. они обладают высокой токсичностью для человека сельско-хозяйственных животных.
Нитраты в основном скапливаются в корнях, корнеплодах, стеблях, черешках и крупных жилках листьев, значительно меньше их в плодах.
По способности накапливать нитраты овощи, плоды и фрукты делятся на 3 группы :
1)с высоким содержанием (до 5000мг/кг сырой массы): салат, шпинат, свекла, укроп, листовая капуста, редис, зелёный лук, дыни, арбузы.
2) со средним содержанием (300-600мг): цветная капуста, кабачки, тыквы, репа, редька, белокачанная капуста, хрен, морковь, огурцы.
3) с низким содержанием (10-80мг): брюссельская капуста, горох, щавель, фасоль, картофель, томаты, репчатый лук, фрукты и ягоды.
Нитраты и качество воды
Большое количество нитратов содержится в коллекторных и дренажных водах, дренирующих сельскохозяйственные территории, на которых применяются азотные удобрения и навоз. Концентрация нитратов в этих водах может превышать 120 мг/л. В естественных (природных) условиях количество их не превышает 9 мг/л. Наибольшее количество (свыше 200 мг/л) нитратов находится в бытовых стоках и в стоках животноводческих комплексов.
Грунтовые воды содержат, как правило, меньше нитратов, чем поверхностные, поскольку почва служит своего рода «фильтром» по пути передвижения нитратного азота. Чем глубже залегают грунтовые воды, тем меньше содержится в них нитратов.
Наиболее рациональный путь снижения концентрации нитратов в поверхностных и грунтовых водах заключается в уменьшении размеров высвобождения азота и его оксидов из природных и антропогенных источников и ограничения их миграции в агроландшафтах. В зонах интенсивного применения азотных удобрений необходимо создание охранных зон, предотвращающих поступление подвижных соединений азота в водоемы, воду которых используют как питьевую.
Нормы азотных удобрений должны быть экологически безопасными, сроки и способы их внесения определяются учетом почвенно-экологических условии агроландшафта и биологических особенностей реакции растений на режим азотного питания. Например, система применения азотных удобрений при выращивании риса на основе локального внесения туков в почву, благодаря чему снижается поступление нитратов в надпочвенный слой воды и исключается необходимость проведения подкормок в течение вегетации с самолета. Последний способ внесения азотных удобрений несет наибольшую угрозу качеству поверхностных вод.
При утилизации сточных вод животноводства рекомендуется ограничить использование их в неразбавленном виде. Наиболее приемлемым и целесообразным является обязательное разбавление стоков водой в 1,5 раза при обязательном внесении в почву фосфорных и калийных удобрений в дозах, необходимых для полною обеспечения растений в фосфоре и калии н сбалансированных к количеству азота, применяемого в сточных водах.
С целью предупреждения избыточной аккумуляции нитратов в природных подах, сохранения и прогнозирования изменения качества воды необходимо наладить региональный и местный контроль за их содержанием как в природных, так и в сбросных водах, установив при этом научно обоснованные нормативы предельно допустимых концентраций во всех видах вод.
Вредное воздействие нитратов на организм человека
Общеизвестно, что поступление в организм нитратов вредоносно для человека и сельско-хозяйственных животных. При этом следует помнить, особенно токсичны организму не сами нитраты, а нитриты, в которые они превращаются при определённых условиях:
1)Нитраты под воздействием фермента нитратредуктазы восстанавливаются до нитратов, которые взаимодействуют с гемоглобином крови и окисляют в нём 2-х валентное железо в 3-х валентное. В результате образуется вещество метгемоглобин, который уже не способен переносить кислород. Поэтому нарушается нормальное дыхание клеток и тканей организма (тканевая гипоксия), в результате чего накапливается молочная кислота, холестерин, и резко падает количество белка.
2)Особенно опасны нитраты для грудных детей, т.к. их ферментная основа несовершенна и восстановление метгемоглобина в гемоглобин идёт медленно.
3)Нитраты способствуют развитию патогенной (вредной) кишечной микрофлоры, которая выделяет в организм человека ядовитые вещества токсины, в результате чего идёт токсикация, т.е. отравление организма. Основными признаками нитратных отравлений у человека являются :
Синюшность ногтей, лица, губ и видимых слизистых оболочек;
Тошнота, рвота, боли в животе;
Понос, часто с кровью, увеличение печени, желтизна белков глаз;
Головные боли, повышенная усталость, сонливость, снижение работоспособности;
Одышка, усиленное сердцебиение, вплоть до потери сознания;
При выраженном отравлении — смерть.
4)Нитраты снижают содержание витаминов в пище, которые входят в состав многих ферментов, стимулируют действие горманов, а через них влияют на все виды обмена веществ.
5)У беременных женщин возникают выкидыши, а у мужчин — снижение потенции.
6)При длительном поступлении нитратов в организм человека (пусть даже в незначительных дозах) уменьшается количество йода, что приводит к увеличению щитовидной железы.
7)Установлено, что нитраты сильно влияют на возникновение раковых опухолей в желудочно-кишечном тракте у человека.
8)Нитраты способны вызывать резкое расширение сосудов, в результате чего понижается кровяное давление.
Допустимые нормы нитратов для человека
Для взрослого человека предельно допустимая норма нитратов 5мг на 1кг массы тела человека, т.е. 0,25г на человека весом в 60кг. Для ребёнка допустимая норма не более 50мг.
Сравнительно легко человек переносит дневную дозу нитратов в 15-200мг; 500мг — это предельно допустимая доза (600мг — уже токсичная доза для взрослого человека). Для отравления грудного малыша достаточно и 10мг нитратов.
ПДК нитратов в воде согласно СанПиН 2.1.4.1175-02 «Гигиенические требования к качеству воды нецентрализованного водоснабжения. Санитарная охрана источников» составляет 45 мг/дм 3
Санитарная охрана источников» составляет 45 мг/дм 3
В качестве очищения воды от нитратов используются обратный осмос и ионный обмен. В первом случае должно производиться обессоливание воды до такой степени, при которой концентрация нитратов будет соответствовать норме. Однако при обратном осмосе удаляются все солис малой селективностью и в результате получается обессоленная вода. Вопрос об полезности такой воды для организма и вкусовых качествах является дискуссионным. Стоимость такой обработки воды достаточно высока. При высоком содержании нитратов вполне возможно использовать малогабаритные установки обратного осмосадля приготовления воды только для питьевых нужд.
12. Нитраты в растениях
Среди многих причин, обусловливающих накопление нитратов в растении, следует выделить следующие; видовая и сортовая специфика накопления нитратов; условия минерального питания, почвенно-экологические факторы. Зачастую факторы, способствующие накоплению нитратов, воздействуют в комплексе , что осложняет прогнозирование уровня нитратов в продукции.
Видовые различия растений по накоплению нитратов зачастую обусловлены локализацией нитратов в отдельных органах растений. Выяснение особенностей локализации нитратов в разных органах и тканях представляется важным как для понимания механизмов перераспределения и запасания нитратов в ходе онтогенеза, так и диагностики качества продукции овощных и кормовых культур.
Распределение нитратов в растениях
Знание особенностей распределения нитратов в товарной части урожая продукции представляет особый интерес для потребителя, так как позволяет рационально использовать продукцию как на переработку (варка, приготовление соков, квашение, соление, консервирование), так и в пищу в свежем виде. Это, в свою очередь, обеспечивает снижение количества нитратов, поступающих в организм человека.
Распределение нитратов связано с физиологической специализацией и морфологическими особенностями отдельных органов возделываемых культур, типом и расположением листьев, размером листовых черешков и жилок, диаметром центрального цилиндра в корнеплодах. Распределение нитратов тесно связано с видом растения. Так, нитраты практически отсутствуют в зерне злаковых культур и в основном сосредоточены в стеблях и листьях. Зеленые культуры накапливают большое количество нитратов, как правило, в стеблях и черешках листьев. В листовой пластинке зеленых культур нитратов содержится в 4-10 раз меньше, чем в стеблях. Высокое содержание нитратов в стеблях и черешках вызвано тем, что они являются местом транспорта нитратов к другим органам растений, где они ассимилируются до органических соединении азота. Способность же ткани накапливать нитраты связана с целым комплексом факторов как внутренних, так и внешних. Наибольшее их количество находится в нижней 11 части листа, минимальное — в его верхушке.
Распределение нитратов тесно связано с видом растения. Так, нитраты практически отсутствуют в зерне злаковых культур и в основном сосредоточены в стеблях и листьях. Зеленые культуры накапливают большое количество нитратов, как правило, в стеблях и черешках листьев. В листовой пластинке зеленых культур нитратов содержится в 4-10 раз меньше, чем в стеблях. Высокое содержание нитратов в стеблях и черешках вызвано тем, что они являются местом транспорта нитратов к другим органам растений, где они ассимилируются до органических соединении азота. Способность же ткани накапливать нитраты связана с целым комплексом факторов как внутренних, так и внешних. Наибольшее их количество находится в нижней 11 части листа, минимальное — в его верхушке.
Накопление нитратов меняется в зависимости от типа органа растения. В клубнях картофеля низкий уровень нитратов обнаружен в мякоти клубня, тогда как в кожуре и сердцевине их содержание возрастало о 1,1-1.3 раза. Сердцевина, кончик и верхушка столовой свеклы отличаются от остальных его частей повышенным содержанием нитратов. Поэтому у столовой свеклы необходимо отрезать верхнюю и нижнюю части корнеплода.
Поэтому у столовой свеклы необходимо отрезать верхнюю и нижнюю части корнеплода.
В белокочанной капусте наибольшее количество нитратов находится в верхушке стебля (кочерыжке). Верхние листья кочана содержат их в 2 раза больше, чем внутренние. И так же как у зеленых овощей, черешки листьев капусты отличаются более высоким содержанием нитратного азота, чем листовые пластинки.
Само по себе присутствие нитратов в растениях — нормальное явление, т. к. они являются источниками азота в этих организмах, но излишнее увеличение их крайне нежелательно, т. к. они (как мы уже знаем) обладают высокой токсичностью для человека и домашних животных.
Нитраты в основном скапливаются в корнях, корнеплодах, стеблях, черешках и крупных жилках листьев, значительно меньше их в плодах.
Нитратов также больше в зеленых плодах, чем в спелых. Больше всего нитратов содержится в салате (особенно в тепличном), в редьке, петрушке, редисе, столовой свёкле, капусте, моркови, укропе:
в свекле и моркови больше нитратов в верхней части корнеплода, а в моркови также и в его сердцевине;
в
капусте — в кочерыжке, в толстых черешках
и в верхних листьях.
Выяснено также, что у всех овощей и плодов больше всего нитратов содержится в их кожице.
По способности накапливать нитраты овощи, плоды и фрукты делятся на 3 группы (2):
со средним содержанием (300 – 600 мг): цветная капуста, кабачки, тыквы, репа, редька, белокочанная капуста, хрен, морковь, огурцы;
С физиологической точки зрения количество нитратного азота в растениях определяется соотношением:
процессов поглощения;
транспорта;
ассимиляции;
распределения его в разных органах и частях растения.
И все эти процессы обусловлены совокупностью почвенно-экологических условий, агротехнических и генетических факторов.
Таким образом, накопление нитратов в растениях зависит от комплекса причин:
от биологических особенностей самих растений и их сортов. Выяснено, что больше всего нитратов содержится в редисе сорта “Красный великан” по сравнению с другими её сортами (“розовый с белым кончиком”, “жара” и др.).
от
возраста растений: в молодых органах
их больше (кроме шпината и овса). Меньше
накапливается нитратов в гибридных
растениях. Нитратов больше в ранних
овощах, чем в поздних.
Меньше
накапливается нитратов в гибридных
растениях. Нитратов больше в ранних
овощах, чем в поздних.
от режима минерального питания растений. Так, микроэлементы (особенно молибден) снижают содержание нитратов в редисе, редьке и цветной капусте; цинк и литий — в картофеле, огурцах и кукурузе. Уменьшается содержание нитратов в растениях и в результате замены минеральных удобрений на органические (навоз, торф и др.), которые постепенно разлагаются и усваиваются растениями. Органические удобрения положительно влияют на капусту, морковь, свеклу, петрушку, картофель, шпинат. Нерациональное, халатное использование химических удобрений, чрезмерные дозы их приводят к сильному накоплению нитратов, особенно в столовых корнеплодах.
Содержание
нитратов возрастает сильнее при
использовании нитратных удобрений
(KNO3, NaNO3, Ca(NO3)2), чем при употреблении
аммонийных. За последние годы (по словам
руководителя лаборатории пищевой
токсикологии института питания Т. С.
Хотимченко) произошло существенное
снижение нитратов в продуктах
отечественного растениеводства по
причине меньшего использования химических
удобрений в виду их дороговизны. Если
в 1988 – 89 годах ПДК по нитратам превышал
15% у овощей, то теперь — не более 3%.
Если
в 1988 – 89 годах ПДК по нитратам превышал
15% у овощей, то теперь — не более 3%.
от факторов окружающей среды (температуры, влажности воздуха, почвы, интенсивности и продолжительности светового освещения):
чем длиннее световой день, тем меньше нитратов в растениях;
при влажном и холодном лете количество нитратов увеличилось в 2,5 раза.
при повышении температуры до 20 °С количество нитратов снизилось в столовой свекле в 3 раза. Нормальная освещённость растений снижает содержание нитратов, поэтому в тепличных растениях нитратов больше.
При
употреблении фруктов в пищу мы должны
внимательно следить за их качеством.
Чтобы яблоки дольше хранились, их
покрывают эмульсионным налётом и
насыщают консервантами. Такие яблоки
внешне очень привлекательны, но порой
в них нет ни вкуса, ни запаха, ни живой
сочности, а консерванты в них убивают
в кишечнике человека полезную микрофлору.
Такие же консерванты используются и
для хранения других продуктов
(растительного масла, сосисок, колбас). Поэтому надо внимательно следить за
сертификатами импортных продуктов.
Поэтому надо внимательно следить за
сертификатами импортных продуктов.
Вопрос накопления нитратов в растениях нашей области стал изучаться СахНИИ с/х с 1989 года, сотрудники которого выяснили, что на Сахалине в связи с особыми агрометеорологическими условиями содержание нитратов в растениях увеличивается:
большое количество дней, частые туманы;
заниженная солнечная радиация;
более низкие температуры воздуха и почвы;
Нитраты в овощах и фруктах
Нитраты в овощах и фруктах
Категория: ПУБЛИКАЦИИ Опубликовано: 17.08.2018 09:56 Просмотров: 932Нитраты – это азотистые соединения, которые играют важную роль в развитии растений, участвуя в процессе формирования белка. Они содержатся в любой растительной пище, и в норме безвредны для здорового организма (при потреблении до 5 мг на 1 кг массы в сутки).
Нитраты становятся опасны, если их количество сильно превышает норму. Это происходит по разным причинам. Чаще всего вину возлагают на безответственных производителей, которые используют избыток азотных удобрений для быстрого созревания и повышения урожая в целом. Растения не могут полностью усвоить все нитраты и накапливают их сверх нормы.
Максимальное количество нитратов обычно содержится в овощах, которые растут в земле или близко к ней. Фрукты и ягоды (кроме арбуза) в этом смысле практически безвредны. Злаковые также вне подозрений: они накапливают нитраты только в стебле, но не в зерне.
Вред причиняют не нитраты как таковые, а их производные – нитриты и нитрозамины. Они образуются в кислой желудочной среде под действием ферментов организма.
Нитрозамины провоцируют возникновение раковых опухолей, нарушают эмбриональное развитие, ухудшают работу нервной и сердечно-сосудистой системы, наносят вред щитовидной железе и разрушают витамины A и B.
К сожалению, универсального и точного способа определить нитраты «на глаз» не существует. Вот наиболее общие признаки, которые могут указывать на избыток нитратов: слишком крупный размер и идеальная форма; чрезмерно насыщенный цвет; водянистость, рыхлость мякоти; неоднородный цвет в разрезе; наличие в мякоти белых или желтых прожилок.
Вот наиболее общие признаки, которые могут указывать на избыток нитратов: слишком крупный размер и идеальная форма; чрезмерно насыщенный цвет; водянистость, рыхлость мякоти; неоднородный цвет в разрезе; наличие в мякоти белых или желтых прожилок.
Если овощи подпорчены, скорее всего в них уже активно идет реакция преобразования нитратов в нитриты. Помните, что их повышенное содержание будет в первом весеннем сборе, недозрелых и тепличных овощах. Советуем по возможности выбирать полностью зрелые сезонные плоды среднего размера. Содержание нитратов будет сильно различаться также в зависимости от вида растения. «Рекордсменами» можно назвать свеклу, капусту, петрушку и укроп, все виды салата, редис, зеленый лук, сельдерей. Овощи с низким содержанием нитратов – это баклажаны, томат, репчатый лук, чеснок, фасоль, перец. Фрукты и ягоды относительно безопасны (если, конечно, вы не собираетесь есть дыню и арбуз с кожурой).
Существует несколько приемов для того, чтобы обезопасить себя и близких от отравления. Тщательно вымойте овощи под проточной водой. Обязательно нужно срезать верхушки и основания. В кабачках и огурцах больше всего нитратов скапливается у плодоножки и в кожуре, а у моркови, свеклы, редиса, репы, редьки – в кончике. У капусты снимают верхние листья и удаляют кочерыжку, а также вырезают крупные прожилки в листьях. Кабачки, тыкву, картофель (а также другие корнеплоды) нужно нарезать и подержать 15-20 минут в холодной воде. Зелень стоит вымачивать подольше: до 2 часов, желательно на солнце.
Тщательно вымойте овощи под проточной водой. Обязательно нужно срезать верхушки и основания. В кабачках и огурцах больше всего нитратов скапливается у плодоножки и в кожуре, а у моркови, свеклы, редиса, репы, редьки – в кончике. У капусты снимают верхние листья и удаляют кочерыжку, а также вырезают крупные прожилки в листьях. Кабачки, тыкву, картофель (а также другие корнеплоды) нужно нарезать и подержать 15-20 минут в холодной воде. Зелень стоит вымачивать подольше: до 2 часов, желательно на солнце.
Значительное количество нитратов уходит при варке овощей. Главное, сливайте отвар горячим, чтобы не допустить их «возвращения».
Эффективно снижают уровень нитратов квашение, соление и маринование. Нитраты выходят в рассол (маринад), поэтому его употреблять не стоит.
Ориентируйтесь на сезонность продуктов, не соблазняйтесь безупречным и ярким внешним видом. Не гонитесь за максимальной экономией. Составляйте сбалансированный рацион из растительной и животной пищи, чередуйте различные виды фруктов и овощей, мяса и злаков. Ешьте свежую пищу.
Ешьте свежую пищу.
В качестве дополнительной меры предосторожности постарайтесь включать в ежедневный рацион больше продуктов с повышенным содержанием витамина С (аскорбиновая кислота предотвращает преобразование нитратов в токсичные для нашего организма вещества).
А вообще, самые лучшие овощи и фрукты – те, которые выращены на собственном огороде (или на плантации, хозяев которых вы знаете лично и полностью им доверяете). Вы будете точно знать, какие удобрения были внесены в почву и в каком количестве, как производился уход за посадками.
А. ПЕТРОВ, Л. ПАЙЗЕРОВА, А. ПАВЛОВА,
специалисты Центра гигиены и эпидемиологии в Чувашской Республике.
Добавить комментарий
Технология выращивания овощей без нитратов
В погоне за хорошим урожаем и прибылью не нужно забывать о качестве и пользе получаемой овощной продукции. Нитраты сами по себе не несут никакой угрозы. Они содержатся в почве и являются источник азота для растений, участвуют в синтезе белков.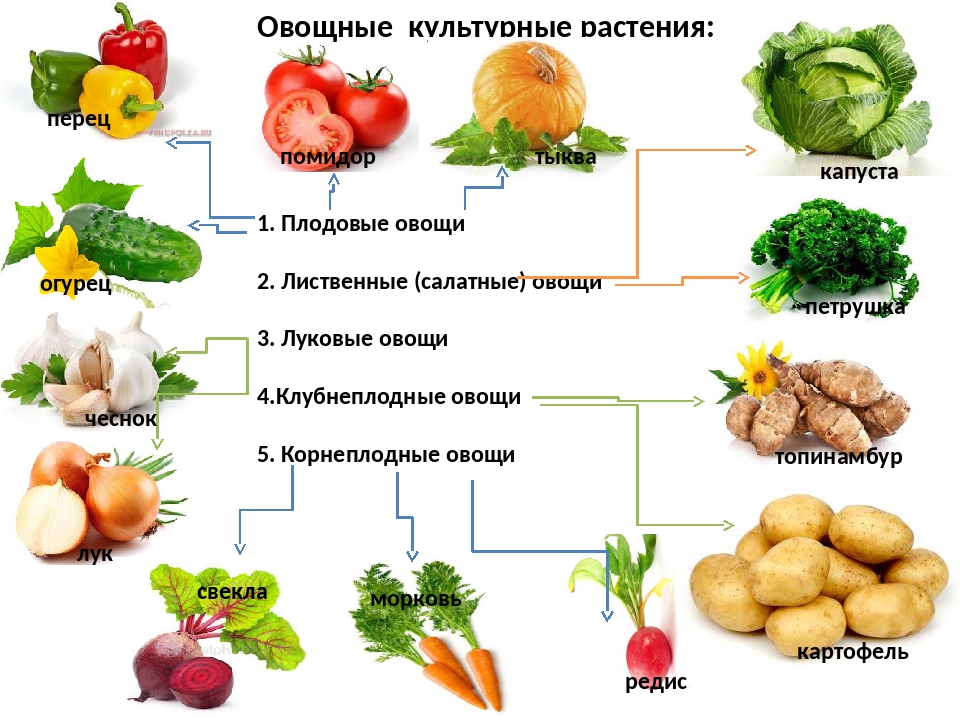 Образуются они благодаря жизнедеятельности нитрифицирующих бактерий, которые переводят азот из органических веществ и минеральных удобрений в соединения, доступные растениям. Сельскохозяйственные культуры усваивают нитраты, при их повышенной концентрации, накапливают. Местом хранения являются клеточные вакуоли. Но продовольственные органы растений, чрезмерно насыщенные этими веществами, представляют опасность для здоровья человека. Меньше всего нитраты концентрируются в плодах, затем по возрастания – в листовой пластинке, проводящей системе листьев, черешке, стебле, корнях. Плоды овощей, полученных на переудобренной почве, содержат нитраты в недопустимых концентрациях.
Образуются они благодаря жизнедеятельности нитрифицирующих бактерий, которые переводят азот из органических веществ и минеральных удобрений в соединения, доступные растениям. Сельскохозяйственные культуры усваивают нитраты, при их повышенной концентрации, накапливают. Местом хранения являются клеточные вакуоли. Но продовольственные органы растений, чрезмерно насыщенные этими веществами, представляют опасность для здоровья человека. Меньше всего нитраты концентрируются в плодах, затем по возрастания – в листовой пластинке, проводящей системе листьев, черешке, стебле, корнях. Плоды овощей, полученных на переудобренной почве, содержат нитраты в недопустимых концентрациях.
Корнеплоды склонны к заражению нитратами, в особенности репа, редис, свекла, редька (проводящая система не имеет локализации). В моркови ксенобиотики концентрируются в области расположения ксилемы и флоэмы, в сердцевине.
Самое маленькое количество опасных соединений отмечается в горохе, баклажане, луке репчатом, болгарском перце, помидоре и баклажане. Средняя концентрация отмечается в моркови, огурце, цветной и белокочанной капусте. Но самое большое количество в зеленых овощах (укроп, петрушка, шпинат, сельдерей).
Средняя концентрация отмечается в моркови, огурце, цветной и белокочанной капусте. Но самое большое количество в зеленых овощах (укроп, петрушка, шпинат, сельдерей).
Возможные колебания содержания нитратов в овощах
| Культура | NO3 мг/кг |
| Капуста белокочанная | 70-4712 |
| Морковь | 20-1843 |
| Свекла столовая | 120-3480 |
| Томат | 10-280 |
| Лук репчатый | 16-900 |
| Лук зеленый | 40-1400 |
| Редис | 200-2700 |
| Салат | 400-2900 |
| Шпинат | 600-4000 |
| Тыква | 29-1820 |
| Огурец | 30-560 |
| Кабачок | 147-1226 |
| Петрушка | 216-1017 |
| Сельдерей | 36-607 |
| Укроп | 400-2200 |
| Щавель | 240-400 |
Избыточное употребление в пищу нитратсодержащей овощной продукции может привести к отравлению. С одной стороны из нитратов в организме образуются канцерогенные вещества, нитрозамины. С другой стороны, формирование нитритов не менее опасно, так они приводят к повышению метагемоглобина в крови. Именно поэтому содержание рассматриваемых соединений не должно превышать допустимых уровней.
С одной стороны из нитратов в организме образуются канцерогенные вещества, нитрозамины. С другой стороны, формирование нитритов не менее опасно, так они приводят к повышению метагемоглобина в крови. Именно поэтому содержание рассматриваемых соединений не должно превышать допустимых уровней.
Предельно допустимый уровень содержание нитратов в овощах (Согласно санитарным правилам и нормам, установленным Министерством здравоохранения РБ)
| Культура | мг/кг |
| Свекла столовая | 1400 |
| Морковь | 200 |
| Капуста белокочанная | 400 |
| Томат | 100 |
| Лук репчатый | 80 |
| Лук перо | 400 |
| Редис | 1500 |
| Листовые овощи (салат, щавель, укроп, петрушка) | 1500 |
| Баклажан | 300 |
| Огурец | 150 |
| Кабачок | 400 |
| Картофель | 150 |
| Перец сладкий | 200 |
Норма нитратов в овощах поддерживается только в случае неукоснительного следования всем нормам и технологиям получения растениеводческой продукции. Грамотное применение агроприемов позволяет собирать богатые урожаи, свободные от ксенобиотиков. Накопление нитратов в овощах зависит от многочисленных параметров: типа почвы, сорта растения, организации севооборота, использования органоминеральных удобрений, обильности полива и т.д.
Грамотное применение агроприемов позволяет собирать богатые урожаи, свободные от ксенобиотиков. Накопление нитратов в овощах зависит от многочисленных параметров: типа почвы, сорта растения, организации севооборота, использования органоминеральных удобрений, обильности полива и т.д.
Факторы, влияющие на накопление нитратов:
Корнеплоды меньше концентрирует ксенобиотики на супесчаных почвах, с pH близкой к нейтральной, с гумусом около 2,03% ‑ 160 мг/кг NO3. Повышение содержание гумуса влечет за собой и увеличения нитратов в овощах.
- Температура и количество влаги.
Высокая влажность, повышенная температура катализируют процесс нитрификации азота в почве, который активно поглощается возделываемой культурой. Самые чистые овощи получаю в год с умеренными осадками и температурой. Опасно установление жаркой погоды в период созревания овощей и уборки. При определении сроков сбора урожая ориентируются на погодные условия.
Для моркови очень важно равномерное увлажнение почвы на протяжении всего вегетационного периода. В сентябре наилучшими условиями будут незначительные, но достаточные осадки, и температура, не превышающая норму. Свекла меньше всего концентрирует ксенобиотики при теплом июне, когда происходит образование вегетационный массы, и нежарком августе и сентябре (период накопления сахаров). Дождливое лето грозит избытком нитратов в корнеплоде. Капуста не склонна усваивать чрезмерное количество ксенобиотиков при средней температуре воздуха и умеренных дождях.
При нехватке осадков требуется проводить орошение, особенно в случае азотных подкормок. Опытным путем доказано, что при его наличии, по сравнению с его отсутствием, овощи накапливают значительно меньше NO3. Избыток полива вовсе вымывает почвенные нитраты.
- Освещенность, плотность посадки.
Плотные посадки, стремление получить как можно больше огурцов, моркови или свеклы с каждого м2 – опасно чрезмерным накоплением ксенобиотиков. Почему так происходит? Дело в том, что при недостатке света, загущенной посаде, что часто наблюдается в защищенном грунте, активность нитроредуктазы падает. Это фермент, с помощью которого происходит переход нитратов в используемую растениями для синтеза белков и других веществ форму.
Почему так происходит? Дело в том, что при недостатке света, загущенной посаде, что часто наблюдается в защищенном грунте, активность нитроредуктазы падает. Это фермент, с помощью которого происходит переход нитратов в используемую растениями для синтеза белков и других веществ форму.
Оптимальные предшественники
Если на поле выращивать одни и те же виды овощных культур, проверка каждого последующего урожая показывает, что концентрация нитратов возрастет. Но если в севооборот включить однолетние и многолетние травы, выращиваемые в качестве зеленого корма, качество продукции резко возрастает. Овощи с наименьшим содержанием нитратов получают в семипольном севообороте, с добавлением в него двух полей кормовых трав. Но не все растения оказывают положительное влияние на рассматриваемый вопрос. К выбору предшественника нужно подходить индивидуально, подбирая его к определенной культуре.
Применение двухлетнего пласта трав, состоящего и злаковых (тимофеевка, костер и овсяница), положительно влияет на качество томатов и моркови. Дополнительное применение пласта люцерны может привести к отсутствию какого-либо результата. Культура обогащает почву азотом, увеличивает объем урожая, но не способствует устранению ксенобиотиков.
Дополнительное применение пласта люцерны может привести к отсутствию какого-либо результата. Культура обогащает почву азотом, увеличивает объем урожая, но не способствует устранению ксенобиотиков.
При исследовании воздействия бобово-злаковых многолетников на морковь, капусту и свеклу получены интересные результаты. Оказывается, что их одногодичное применение в севообороте приводит к минимизации нитратов в корнеплодах (морковь, свекла), но увеличивает их содержание в капусте белокочанной. Объясняют это способностью бобовых фиксировать атмосферный азот.
Агротехнические приемы, снижающие концентрацию нитратов в овощах:
- Выбирать сорта, минимально поглощающие ксенобиотики.
- Включать в севооборот кормовые травы и сидераты.
- Соблюдать сроки сева, высадки рассады и уборки урожая. Незрелая овощная продукция характеризуется повышенным содержанием нитратов.
- Соблюдать схему посадки и норму высадки. Попытки загущения посадок с целью увеличения объемов с/х продукции приводят к затенению.
 Овощи такого качества могут не пройти проверку на ПДК нитратов. Слишком редкие посадки, приводят к получению крупных плодов, содержащих повышенное количество нитратов.
Овощи такого качества могут не пройти проверку на ПДК нитратов. Слишком редкие посадки, приводят к получению крупных плодов, содержащих повышенное количество нитратов. - Не допускать чрезмерного содержания в почве нитратного азота (более 30 мг NO3 на 100 г почвы). Для его связывания и замедления процессов нитрификации регулярно использовать соломистый навоз, соломенную резку, древесные опилки, растительные остатки, сидераты, другие органические отходы, богатые клетчаткой, которые замедляют высвобождение нитратного азота в почве за счет интенсивного размножения микроорганизмов, потребляющих нитраты.
- Общая доза азотных удобрений под капусту белокочанную и цветную не должна превышать 150 кг/га, под свеклу, кабачок, картофель, помидор, огурец, ‑ не более 120 кг/га, зеленные культуры и морковь, ‑ не более 90 кг/га.
- Подкормки азотными удобрениями допускаются лишь в 1-ую половину вегетации, и прекращаются за полтора месяца или месяц до уборки овощей.

- Чтобы азот не превалировал над калием во время созревания кочанов, плодов и корнеплодов, часть общей дозы калийных удобрений для подкормки вносят с поливной водой.
- Ускорение созревания, благодаря подкормки микроудобрениями, содержащими молибден и бор, не позволяет накопиться чрезмерному количеству нитратов в продуктовых органах.
- Контролировать азотное питание растений.
Agropk.by, мы работаем для вас
Чем опасны арбузы — Газета.Ru
Почему не надо бояться нитратов в арбузах, чем эта ягода действительно может быть опасна и кому не стоит ее есть, разбиралась «Газета.Ru».
С 3 августа в Москве откроются бахчевые развалы, где можно будет купить арбузы. Так ли страшны нитраты, которыми из года в год пугают потребителей производители нитратомеров и адепты «натуральных» продуктов, разбиралась «Газета.Ru».
Нитраты — это соли азотной кислоты.
Они применяются в сельском хозяйстве в качестве удобрений. Нитраты образуются и в человеческом организме, выполняя роль антимикробного агента в слюне, а также участвуя в работе сердечно-сосудистой системы, регулируя кровяное давление.
Нитраты образуются и в человеческом организме, выполняя роль антимикробного агента в слюне, а также участвуя в работе сердечно-сосудистой системы, регулируя кровяное давление.
Под воздействием ферментов организма и некоторых бактерий, обитающих в кишечнике и полости рта, излишек нитратов превращается в гораздо более токсичные нитриты. Попадая в кровь, они превращают гемоглобин в метгемоглобин, который не способен переносить кислород и углекислый газ. Когда его доля в крови доходит до 30%, появляются симптомы острого отравления, удушье, тахикардия, боль в затылке, слабость, снижается давление.
Дальнейший рост концентрации метгемоглобина в крови способен привести к смерти.
Кроме того, в кислой среде желудка из нитритов образовываются нитрозамины, способные привести к раку органов пищеварительной системы.
Интересно, что возможный вред нитритов для организма связан в первую очередь с их источником. Одно из крупнейших эпидемиологических исследований, охвативших данные за несколько десятилетий, показало, что опасны нитриты (и образующиеся из них в организме нитрозамины), поступающие из обработанных мясных продуктов, в которых они предотвращают рост бактерий. При их частом попадании в организм повышаются риски развития онкозаболеваний.
При их частом попадании в организм повышаются риски развития онкозаболеваний.
При этом нитриты, которые образовались из нитратов, поступивших из овощей и фруктов, наоборот, снижают риск развития рака желудка.
Лабораторные эксперименты показали, что образование опасных веществ ускоряется в присутствии компонентов мяса. В овощах и фруктах же содержатся антиоксиданты, которые блокируют такие реакции. Благодаря ним нитриты превращаются в оксид азота (II), которые способствует расширению кровеносных сосудов и нормализации кровяного давления.
Арбузы удобряют нитратами в период их созревания, пояснил «Роскачеству» старший научный сотрудник ВНИИ орошаемого овощеводства и бахчеводства Артем Соколов. При соблюдении агротехнологии арбуз возьмет ровно столько, сколько ему нужно для роста. К концу созревания в нем не должно быть нитратов – арбуз вырастет, питаясь ими. Поэтому тем, кто боится нитратов, стоит выбирать наиболее зрелые арбузы и не слишком активно вгрызаться в корки — в недостаточно зрелых ягодах нитраты будут содержаться преимущественно в них.
Кроме того, высокое содержание нитратов может быть в ранних поливных арбузах, которые везут в основном из Средней Азии или южных областей России начиная с конца июля. У поливных арбузов, в отличие от суходольных, плохо развиты корни, они не могут питаться самостоятельно, поэтому их нужно обильно удобрять. Суходольные арбузы ищут воду и питательные вещества сами, но и созревают позже.
Тем не менее, определенные риски для здоровья при потреблении арбузов все же есть.
В частности, на их кожуре могут остаться вещества, которыми растение обрабатывали для защиты от грибков и паразитов. До мякоти они не доходят, но могут сохраниться на поверхности и даже частично в нее впитаться. Поэтому перед употреблением арбуз необходимо тщательно вымыть и на всякий случай не вгрызаться в корку.
Кроме того, арбузы часто продаются у дорог, где на них оседает поднятая колесами пыль. Хотя, по словам специалистов, самые свежие и качественные арбузы можно купить именно на трассах неподалеку от места выращивания, отмывать их от осевшей на поверхности грязи стоит особенно тщательно, иначе последствия отравления затмят все удовольствие от поедания.
Также у арбуза высокий гликемический индекс — это значит, что его потребление приводит к резкому скачку глюкозы в крови. Поэтому людям с сахарным диабетом и предрасположенностью к нему стоит отнестись к арбузам с осторожностью.
Так как арбуз — сильное мочегонное средство, не стоит увлекаться его поеданием беременным женщинам и людям с заболеваниями почек.
Излишняя нагрузка на них может спровоцировать приступ мочекаменной болезни.
Специалисты не рекомендуют есть арбуз в качестве десерта после плотного приема пищи — обилие углеводов в его составе может вызвать тяжесть в желудке. Лучше съесть арбуз отдельно и желательно в первой половине дня. Поедание арбуза на ночь может привести к беспокойному сну из-за его мочегонных свойств и отекам на утро.
Как нейтрализовать химию в овощах?
Не всегда можно быть уверенным в экологической безопасности овощей, которые попадают к нам на стол.
Овощи – незаменимый компонент здорового питания.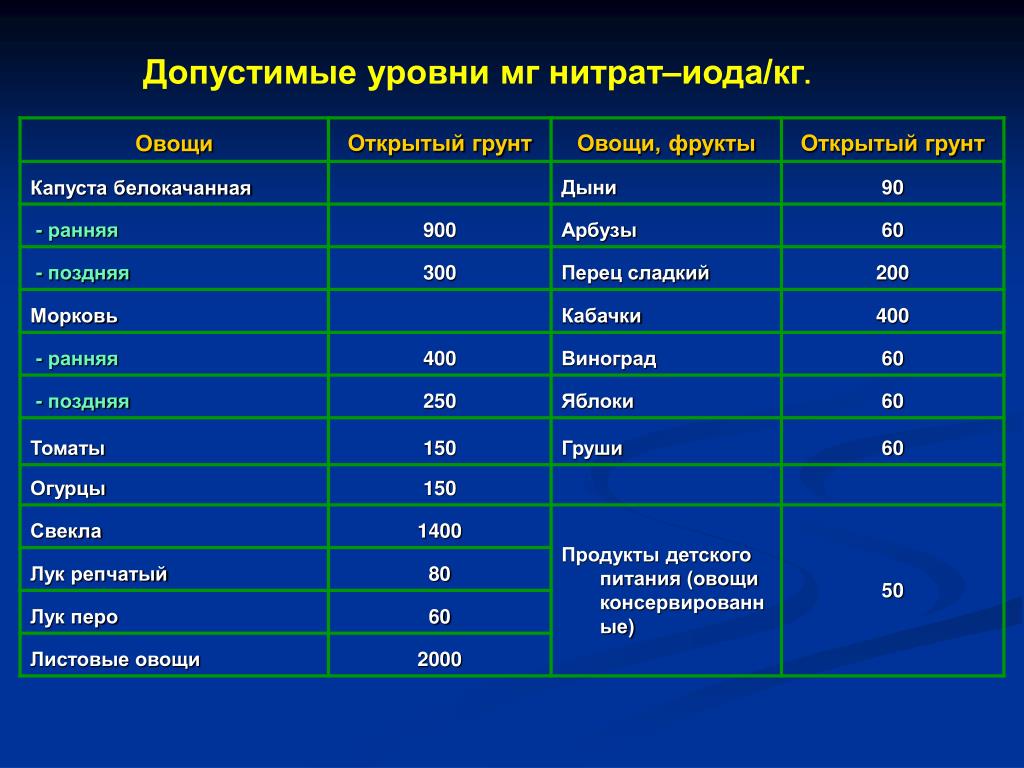 Они должны присутствовать в нашем рационе ежедневно, свежими или в составе блюд. Но не секрет, что вырастить хороший урожай без удобрений для почвы невозможно. В результате овощи накапливают нитраты и пестициды. Причем, химия попадает в овощи не только при обработке минеральными удобрениями, но из органики, если ее неправильно использовать. Особенно это касается ранних овощей. Есть и внешние причины, которые способствуют накоплению «лишних» нитратов в сельскохозяйственной продукции (климатические условия, болезни или вредители, сорняки и т.д.). Таким образом, даже урожай с собственного дачного участка может быть опасным для здоровья.
Они должны присутствовать в нашем рационе ежедневно, свежими или в составе блюд. Но не секрет, что вырастить хороший урожай без удобрений для почвы невозможно. В результате овощи накапливают нитраты и пестициды. Причем, химия попадает в овощи не только при обработке минеральными удобрениями, но из органики, если ее неправильно использовать. Особенно это касается ранних овощей. Есть и внешние причины, которые способствуют накоплению «лишних» нитратов в сельскохозяйственной продукции (климатические условия, болезни или вредители, сорняки и т.д.). Таким образом, даже урожай с собственного дачного участка может быть опасным для здоровья.
У нас возможности проверять каждый овощ в лаборатории на содержание вредных веществ. Отказываться от их употребления, включая ранние овощи, тоже не стоит. Узнайте, как избавиться от химии в овощах доступными методами.
Места накопления химии
Способность разных овощей накапливать нитраты отличается. Больше всего их накапливается в салате, листовой капусте, укропе, свекле, редисе, зеленом луке, шпинате. Меньше всего – в брюссельской капусте, фасоли, горохе, картофеле, сладком перце, томатах, репчатом луке. Правильная обработка помогает значительно снизить содержание нитратов и пестицидов в овощах. Для этого полезно знать места, в которых скапливается больше всего вредных веществ.
Меньше всего – в брюссельской капусте, фасоли, горохе, картофеле, сладком перце, томатах, репчатом луке. Правильная обработка помогает значительно снизить содержание нитратов и пестицидов в овощах. Для этого полезно знать места, в которых скапливается больше всего вредных веществ.
Картофель. Химия накапливается под кожурой картофеля и в сердцевине клубня. Рекомендуется сливать воду после того, как картошка закипела.
Капуста. Наибольшее количество нитратов содержится в верхних листах капусты и кочерыжке. Поэтому стоит их выбросить.
Огурцы, кабачки, баклажаны. Темно-зеленая кожура огурцов указывает на то, что их «перекормили» нитратами. В норме они должны быть нежно-травяного цвета. Самое большое количество нитратов в огурцах находится в кожуре и области плодоножки. У кабачков и баклажанов также нужно срезать части, примыкающие к плодоножке. Кроме того, очищайте от шкурки ранние кабачки и баклажаны.
Секла, морковь, редис. Наибольшая концентрация нитратов в этих корнеплодах — в верхушках и области плодоножки. Поэтому перед употреблением эти части нужно обрезать. Самой богатой нитратами считается свекла с закрученными хвостиками. У моркови нужно обрезать около 1 см хвостика и позеленевшую часть. В редисе нитраты накапливаются также в кожуре.
Поэтому перед употреблением эти части нужно обрезать. Самой богатой нитратами считается свекла с закрученными хвостиками. У моркови нужно обрезать около 1 см хвостика и позеленевшую часть. В редисе нитраты накапливаются также в кожуре.
Помидоры. Больше всего нитратов содержится в помидорах с толстой кожурой и в оранжево-красных помидорах. Перед покупкой посмотрите на овощ в разрезе. Белая мякоть и толстые прожилки – признак большого содержания химии. Если вам все же попались подозрительные томаты, подержите их в прохладной воде примерно час.
Традиционные компоненты салатов, овощных и других блюд — зелень, салат, укроп, петрушка. В этих растениях химия скапливается в прожилках и черенках. Поскольку зелень стремительно впитывает нитраты, то перед тем, как добавлять ее в блюда, вымочите в воде около часа.
Как избавиться от химии в овощах
Чтобы избавиться от химии в овощах, рекомендуем вам прислушаться к советам по их выбору и использованию.
Старайтесь покупать отечественные овощи. При их выращивании использовалось меньшее количеств удобрений, чем тех, что росли, например, в Голландии, Турции, Египте, Израиле. Почва в этих странах не позволяет дать богатый урожай без использования большого количества добавок.
При их выращивании использовалось меньшее количеств удобрений, чем тех, что росли, например, в Голландии, Турции, Египте, Израиле. Почва в этих странах не позволяет дать богатый урожай без использования большого количества добавок.
Отдавайте предпочтение сезонным овощам. Растения, выращенные вне своего сезона, нуждаются в большем количестве подкормки и обработки.
Избегайте слишком крупных и красивых овощей. Безупречный вид, обычно, — результат активного использования удобрений.
Тщательно мойте овощи. Мытье снижает содержание в них нитратов на 10-15%. Замачивание овощей на 30-60 минут – еще более эффективный метод уменьшить содержание химии. Свеклу, кабачки, морковь, тыкву, баклажаны можно нарезать небольшими кубиками и залить водой на 5-10 минут. Процедуру повторить еще 1-2 раза.
Чтобы удалить химические вещества с кожуры овощей или с зелени, замочите их на 5-10 минут в солевом растворе или слабом растворе уксуса, а затем промойте. Можно опустить их на 5 секунд в кипяток.
Варка – способ уменьшить содержание нитратов на 50-80%. В течение первых 30-40 минут варки нитраты активно уходят в отвар. Чтобы они не вернулись обратно овощи, отвар нужно слить горячим. Для лучшего испарения нитратов и их соединений готовьте овощи с открытой крышкой.
Чтобы частично нейтрализовать действие нитратов, добавляйте в овощное блюдо лимонный или гранатовый сок. Можно также сбрызгивать ими овощи перед приготовлением.
Не храните долго размороженные овощи и свежеприготовленные соки и салаты. Это способствует превращению нитратов в канцерогенные вещества. По той же причине не подвергайте продукты и блюда из них многократным изменениям температуры хранения.
Очищайте кожуру с овощей, особенно, если сомневаетесь в их качестве. В частности, нейтральный вкус овоща указывает на то, что их перекормили нитратами.
Чем опасны пестициды, нитраты и нитриты в овощах и фруктах?
Не так просто вырастить хороший урожай: атакуют вредители, овощи страдают от засухи и жары, да и хранить плоды – целая проблема. Сегодня производители широко применяют для своих целей пестициды, а также щедро «подкармливают» почвы нитратными удобрениями. Опасны ли они для человека, и как определить их наличие в овощах и фруктах, разбирается Passion.ru.
Сегодня производители широко применяют для своих целей пестициды, а также щедро «подкармливают» почвы нитратными удобрениями. Опасны ли они для человека, и как определить их наличие в овощах и фруктах, разбирается Passion.ru.
Что такое пестициды?
Пестицидами называют химические вещества, являющиеся ядами для вредителей, защитой от сорняков и различного рода болезней культурных растений. Их разделяют на группу инсектицидов, защищающих от вредных насекомых, фунгицидов — для защиты от грибковых поражений культурных растений, и гербицидов — для борьбы с сорняками.
Первыми пестицидами были растительные вещества по типу никотина, но сегодня применяют химические соединения различных групп. Самыми известными на сегодня пестицидами являются ДДТ, фосфорорганические соединения, пиретроиды и карбаматы.
В организм человека они могут проникать при употреблении плодов прямо с грядки, а также через употребление растений, накопивших в себе пестициды в процессе роста, если их применяли неумеренно. Такие продукты могут нарушать естественную защиту организма от рака, вызывая мутации клеток и опухоли.
Такие продукты могут нарушать естественную защиту организма от рака, вызывая мутации клеток и опухоли.
Кроме того, пестициды при попадании в организм могут вызвать отравления с тошнотой, рвотой и жидким стулом, поражением нервной системы и печени. Накопление их в организме медленно, но верно подрывает здоровье, сокращая продолжительность жизни и провоцируя эндокринные болезни, снижение иммунитета, проблемы легких и сердца.
Чтобы уменьшить вероятность встречи с ними, покупайте овощи и фрукты у проверенных производителей, сертифицированных продавцов, а перед едой тщательно промывайте фрукты и овощи в тазу с водой, морской солью и соком лимона либо в содовом растворе, а затем споласкивайте под проточной водой.
Что такое нитраты и нитриты?
Для повышения урожайности и для подкормки культурных растений, стимуляции их роста и плодовитости в сельском хозяйстве зачастую применяются химические удобрения, которые доставляют растениям калийные соли.
Дешевым и эффективным средством для их доставки являются азотная кислота – нитрат, в соединении с калием, кальцием или аммонием. Однако при регулярном их внесении в почву в большом объеме они имеют специфику накапливаться в определенных частях растений.
Сами по себе нитраты – соли не опасные и не токсичные, однако в организме или самих растениях в результате процессов метаболизма из них получаются нитрозосоединения, недоокисленные азотнокислые соли. Они имеют свойства свободных радикалов, повреждают клетки и ДНК, обладают мутагенным (вызывают мутации клеток) и канцерогенным (вызывают опухолевый рост) эффектами.
Кроме того, нитраты из овощей, фруктов либо зерновых в условиях влажности и тепла или в процессе пищеварения в кишечнике человека под действием микрофлоры толстой кишки превращаются в нитритные соединения. Эти вещества в большом количестве опасны для здоровья человека.
Нитриты достаточно широко используются в пищевой промышленности для производства колбас и мясных консервов, для взрослых они не опасны, но могут представлять реальную угрозу для детей. Поэтому детям нельзя потреблять богатые консервантами продукты, колбасу и мясные полуфабрикаты. Не стоит ими злоупотреблять и кормящей матери – нитраты и нитриты попадают в грудное молоко.
Поэтому детям нельзя потреблять богатые консервантами продукты, колбасу и мясные полуфабрикаты. Не стоит ими злоупотреблять и кормящей матери – нитраты и нитриты попадают в грудное молоко.
Опасность нитратов и нитритов
границ | Снижение содержания нитратов в овощах путем совместного регулирования распределения на короткие расстояния и перевозки на дальние расстояния
Введение
Азот (N) является важным элементом, влияющим на рост, урожайность и качество сельскохозяйственных культур (Peng et al., 2010). ; Джу и др., 2015). Он необходим для синтеза макромолекулярных соединений, таких как белки и нуклеиновые кислоты, которые играют важную роль в метаболизме и производстве энергии организмами (Li and Gong, 2011).Аммонийный азот (NH 4 + -N) и нитратный азот (NO 3 − -N) являются основными формами азота, поглощаемого и используемого сельскохозяйственными культурами, при этом последний является основным источником азота для культур засушливых земель. (Танг и др., 2013; Чжао и др., 2018). Экзогенные концентрации NO 3 − относятся к наиболее важным факторам, влияющим на накопление NO 3 − в растениях. Растения активно поглощают NO 3 − из окружающей среды посредством протонно-нитратного механизма (Wang et al., 2018). Несколько представителей семейства переносчиков NPF/пептидов (PTR) и переносчиков 2 (NRT2) NO 3 − в Arabidopsis участвуют в поглощении NO 3 − , включая компоненты системы высокоаффинного транспорта [HATS : NRT2.1, NRT2.2 (Filleur et al., 2001), NRT2.4 (Kiba et al., 2012) и NRT2.5 (Лежнева и др., 2014)] и низкоаффинной транспортной системы [LATS : NPF4.6 (Huang et al., 1999)]. Кроме того, известно, что NPF6.3 функционирует как переносчик NO 3 − с двойным сродством (Liu et al., 1999), сродство к NO 3 − которого определяется внешними концентрациями NO 3 − (Ho et al.
(Танг и др., 2013; Чжао и др., 2018). Экзогенные концентрации NO 3 − относятся к наиболее важным факторам, влияющим на накопление NO 3 − в растениях. Растения активно поглощают NO 3 − из окружающей среды посредством протонно-нитратного механизма (Wang et al., 2018). Несколько представителей семейства переносчиков NPF/пептидов (PTR) и переносчиков 2 (NRT2) NO 3 − в Arabidopsis участвуют в поглощении NO 3 − , включая компоненты системы высокоаффинного транспорта [HATS : NRT2.1, NRT2.2 (Filleur et al., 2001), NRT2.4 (Kiba et al., 2012) и NRT2.5 (Лежнева и др., 2014)] и низкоаффинной транспортной системы [LATS : NPF4.6 (Huang et al., 1999)]. Кроме того, известно, что NPF6.3 функционирует как переносчик NO 3 − с двойным сродством (Liu et al., 1999), сродство к NO 3 − которого определяется внешними концентрациями NO 3 − (Ho et al. , 2009). Предыдущие исследования показали, что различия в накоплении NO 3 − в разных сортах салата в значительной степени объясняются различиями в поглощении NO 3 − (Burns et al., 2011). В исследовании, посвященном изучению двух сортов пекинской капусты с высоким и низким накоплением NO 3 − , соответственно, более сильная поглощающая способность NO 3 − и более высокая экспрессия генов NPF и NRT2 были обнаружены у сорт с высоким NO 3 − – аккумулирующий сорт (Zhao et al., 2011). Поглощаемый растениями NO 3 − может быть непосредственно ассимилирован в аминокислоты под действием NO 3 − редуктазы (NR), нитритредуктазы (NiR), глутаминсинтетазы (GS) и глутаматсинтазы ( GOGAT) в цитозоле клетки (Williams et al., 1987). Было продемонстрировано, что дисбаланс в эффективности поглощения и снижения NO 3 − в овощах является важным фактором в определении накопления NO 3 − , а активность NR значительно отрицательно коррелирует.
, 2009). Предыдущие исследования показали, что различия в накоплении NO 3 − в разных сортах салата в значительной степени объясняются различиями в поглощении NO 3 − (Burns et al., 2011). В исследовании, посвященном изучению двух сортов пекинской капусты с высоким и низким накоплением NO 3 − , соответственно, более сильная поглощающая способность NO 3 − и более высокая экспрессия генов NPF и NRT2 были обнаружены у сорт с высоким NO 3 − – аккумулирующий сорт (Zhao et al., 2011). Поглощаемый растениями NO 3 − может быть непосредственно ассимилирован в аминокислоты под действием NO 3 − редуктазы (NR), нитритредуктазы (NiR), глутаминсинтетазы (GS) и глутаматсинтазы ( GOGAT) в цитозоле клетки (Williams et al., 1987). Было продемонстрировано, что дисбаланс в эффективности поглощения и снижения NO 3 − в овощах является важным фактором в определении накопления NO 3 − , а активность NR значительно отрицательно коррелирует. с содержанием NO 3 − в листьях пекинской капусты (Du et al., 2008). Более того, часть NO 3 − секретируется в ризосферу при посредничестве переносчика NO 3 − NPF2.7 (Wang et al., 2018).
с содержанием NO 3 − в листьях пекинской капусты (Du et al., 2008). Более того, часть NO 3 − секретируется в ризосферу при посредничестве переносчика NO 3 − NPF2.7 (Wang et al., 2018).
NO 3 − , который остается неиспользованным растениями, распространяется по всему заводу посредством распределения на короткие и дальние расстояния (Han et al., 2015; Zhang, 2017). Распределение NO 3 — на короткие расстояния происходит на субклеточном уровне и включает распределение NO 3 — между цитоплазмой и вакуолями, процесс, регулируемый членами семейства белков хлоридных каналов (CLC).Первоначально считалось, что белки CLC участвуют только в транспорте Cl –, функционируя как хлоридные каналы и антитранспортеры Cl –/H + . Однако в исследовании мутанта Arabidopsis clca De Angeli et al. (2006) продемонстрировали, что белки семейства CLC также могут транспортировать NO 3 — через тонопласт, действуя как антипортеры 2NO 3 — /H + . Было обнаружено, что по сравнению с растениями дикого типа мутант clca накапливает в вакуолях на 50 % меньше NO 3 − , что указывает на то, что AtCLCa играет ключевую роль в регуляции хранения вакуолей и распределения на короткие расстояния. NO 3 − в растениях (De Angeli et al., 2006).
Было обнаружено, что по сравнению с растениями дикого типа мутант clca накапливает в вакуолях на 50 % меньше NO 3 − , что указывает на то, что AtCLCa играет ключевую роль в регуляции хранения вакуолей и распределения на короткие расстояния. NO 3 − в растениях (De Angeli et al., 2006).
Транспорт NO 3 − на большие расстояния в основном зависит от координации белков NPF с низким сродством. AtNPF7.3 является рН-зависимым транспортным белком NO 3 − , расположенным в цитомембране и экспрессируемым в клетках перицикла вблизи ксилемы. Установлено, что у мутантов, лишенных AtNPF7.3 , содержание NO 3 − в ксилемном соке и побегах значительно снижено, что свидетельствует о том, что AtNPF7.3 играет важную роль в содействии переносу NO 3 − на большие расстояния от корней к надземным частям (Lin et al., 2008). Напротив, AtNPF7.2 в основном экспрессируется в клетках паренхимы вблизи ксилемы корня, где он участвует в выгрузке NO 3 − из ксилемы, регулируя коэффициент распределения NO 3 − между корнями. и побеги (Li et al., 2010). Таким образом, на концентрацию NO 3 − в растениях влияют многочисленные процессы, между которыми существует тесная взаимозависимость, которая способствует скоординированному регулированию накопления NO 3 − в растениях.
Напротив, AtNPF7.2 в основном экспрессируется в клетках паренхимы вблизи ксилемы корня, где он участвует в выгрузке NO 3 − из ксилемы, регулируя коэффициент распределения NO 3 − между корнями. и побеги (Li et al., 2010). Таким образом, на концентрацию NO 3 − в растениях влияют многочисленные процессы, между которыми существует тесная взаимозависимость, которая способствует скоординированному регулированию накопления NO 3 − в растениях.
Являясь важным источником неорганического азота, содержание NO 3 − в пищевых продуктах может поступать из почвы, водных ресурсов, химических удобрений или пищевых добавок, что, следовательно, влияет на пищевую цепь человека (Quijano et al., 2017 ). На сегодняшний день многочисленные исследования содержания NO 3 − в растениях выявили высокие концентрации NO 3 − в различных овощах (Bahadoran et al. , 2016), особенно в листовых овощах, которые являются наиболее важным источником NO 3 − в рационе человека, на долю которого приходится более 80% поступления NO 3 − (Anjana and Iqbal, 2007; Bondonno et al., 2018; Четти и др., 2018). Однако при хранении и обработке растений избыток NO 3 − , остающийся неусвоенным в тканях растений, может быть ферментативно преобразован в NO 2 − . NO 3 − , поступающий в организм человека, также может быть уменьшен до NO 2 − за счет активности кишечных микроорганизмов. NO 2 − является сильным канцерогеном и вызывает накопление метгемоглобина, соединения с потенциально токсичным действием на здоровье человека (Salehzadeh et al., 2020). Содержание NO 3 − в овощах зависит от его распространения и использования и зарекомендовало себя как один из показателей, используемых для оценки качества овощей и продуктов их переработки.
, 2016), особенно в листовых овощах, которые являются наиболее важным источником NO 3 − в рационе человека, на долю которого приходится более 80% поступления NO 3 − (Anjana and Iqbal, 2007; Bondonno et al., 2018; Четти и др., 2018). Однако при хранении и обработке растений избыток NO 3 − , остающийся неусвоенным в тканях растений, может быть ферментативно преобразован в NO 2 − . NO 3 − , поступающий в организм человека, также может быть уменьшен до NO 2 − за счет активности кишечных микроорганизмов. NO 2 − является сильным канцерогеном и вызывает накопление метгемоглобина, соединения с потенциально токсичным действием на здоровье человека (Salehzadeh et al., 2020). Содержание NO 3 − в овощах зависит от его распространения и использования и зарекомендовало себя как один из показателей, используемых для оценки качества овощей и продуктов их переработки. Следовательно, меры, которые могут быть использованы для снижения концентрации NO 3 − в листовых овощах путем регулирования его распределения и использования, имеют важное значение с точки зрения снижения загрязнения окружающей среды и обеспечения здорового питания.
Следовательно, меры, которые могут быть использованы для снижения концентрации NO 3 − в листовых овощах путем регулирования его распределения и использования, имеют важное значение с точки зрения снижения загрязнения окружающей среды и обеспечения здорового питания.
Короткий путь (от вакуоли до цитоплазмы) NO
3 − Распространение в овощах Эволюционный успех высших растений во многом объясняется их уникальной клеточной архитектурой (Kriegel et al., 2015). Вакуоли, как крупнейшие органеллы в клетках зрелых растений, составляют примерно 90% объема клетки и обычно используются для хранения питательных веществ (Liao et al., 2002; Shen et al., 2003; Krebs et al., 2010). ; Ляо и др., 2018). После поглощения растениями NO 3 − , важное питательное вещество для растений, распределяется в метаболический пул (цитоплазма) или в запасной пул (вакуоль) (Miller et al., 2007). Концентрации NO 3 — в вакуоли и цитоплазме обычно находятся в пределах от 30 до 50 моль м -3 и от 3 до 5 моль м -3 соответственно (Martinoia et al. , 2000). , а фракция, хранящаяся в вакуоли, не может быть метаболизирована растениями, если она первоначально не выделяется в окружающую цитоплазму. Соответственно, вакуоль является основным местом хранения NO 3 − , и поэтому роль этой вакуолярной фракции в распределении NO 3 − не следует упускать из виду при изучении содержания NO 3 − растений. (Мартинойя и др., 1981; Хуанг и др., 2012 г.; Хан и др., 2015).
, 2000). , а фракция, хранящаяся в вакуоли, не может быть метаболизирована растениями, если она первоначально не выделяется в окружающую цитоплазму. Соответственно, вакуоль является основным местом хранения NO 3 − , и поэтому роль этой вакуолярной фракции в распределении NO 3 − не следует упускать из виду при изучении содержания NO 3 − растений. (Мартинойя и др., 1981; Хуанг и др., 2012 г.; Хан и др., 2015).
В целом ассимиляционная способность цитоплазмы клеток листа достаточна для снижения концентрации NO 3 − . Пока NO 3 − остается распределенным вне вакуоли, он может быстро усваиваться, и поэтому содержание NO 3 − в растениях во многом определяется соотношением распределения NO 3 — внутри и снаружи вакуоли (Shen et al., 2003; Хуанг и др., 2012 г.; Хан и др., 2016). Изменения относительного размера этих двух резервуаров NO 3 — опосредованы обменным каналом 2NO 3 — /H + CLCa в тонопласте (Krebs et al. , 2010; Liao et al. , 2019) и зависит от активности вакуолярных протонных насосов H + -ATPase (V-ATPase) и вакуолярных H + -пирофосфатазы (V-PPase). Комбинированная активность этих вакуолярных протонных насосов, использующих MgATP и MgPPi в качестве субстратов, соответственно, создает электрохимический градиент H + в тонопласте, который управляет транспортом NO 3 — против его электрохимического потенциала (Martinoia et al., 2007; Лин и др., 2012) (рис. 1А).
, 2010; Liao et al. , 2019) и зависит от активности вакуолярных протонных насосов H + -ATPase (V-ATPase) и вакуолярных H + -пирофосфатазы (V-PPase). Комбинированная активность этих вакуолярных протонных насосов, использующих MgATP и MgPPi в качестве субстратов, соответственно, создает электрохимический градиент H + в тонопласте, который управляет транспортом NO 3 — против его электрохимического потенциала (Martinoia et al., 2007; Лин и др., 2012) (рис. 1А).
Рисунок 1 Модель распределения NO 3 − на дальние расстояния в растениях. Изменено из Чжан (2017). (A) Накопление NO 3 − в вакуоли регулируется хлоридными каналами (CLCa) и зависит от градиента H + , устанавливаемого V-ATPase и V-PPase. (B) Распространение NO 3 − на короткие расстояния и реакции, катализируемые NO 3 − редуктазы (NR), нитритредуктазы (NiR), глутаминсинтетазы (GS) и глутаматсинтазы (GOGAT) ) в побегах. (C) Транспорт NO 3 − на большие расстояния от корней к побегам в основном регулируется генами NPF7.3 , NPF7.2 и NPF2.9 .
(C) Транспорт NO 3 − на большие расстояния от корней к побегам в основном регулируется генами NPF7.3 , NPF7.2 и NPF2.9 .
Эти два протонных насоса входят в число наиболее распространенных белков тонопластов, что указывает на значительное количество энергии, затрачиваемой на вакуолярный транспорт (Carter et al., 2004; Jaquinod et al., 2007). V-АТФазы представляют собой высококонсервативные многосубъединичные протонные насосы, состоящие из двух субкомплексов: периферического комплекса V 1 и мембранно-интегрального комплекса V 0 .Периферический комплекс V 1 включает восемь субъединиц (от VHA-A до -H), которые экспонируются на цитоплазматической стороне вакуолярной мембраны и отвечают за гидролиз АТФ. Мембранно-интегральный комплекс V 0 , состоящий из шести субъединиц (VHA-а, -с, -с’, с’, -d и -е), встроен в мембрану и функционирует как канал для транслокации протонов из цитоплазмы в просвет компартментов эндомембраны, а также служит сайтом связывания для полимеризации и сборки субъединиц V 1 (Cipriano et al. , 2008; Луо, 2012). По сравнению с тонопластом H + -ATPase, протонная помпа H + -PPase, широко распространенная в растениях, некоторых водорослях, простейших и бактериях, имеет простую структуру, состоящую из олигопептидной цепи, и составляет примерно от 1 до 10% мембранных белков (Zhao, Liu, 1999; Maeshima, 2000).
, 2008; Луо, 2012). По сравнению с тонопластом H + -ATPase, протонная помпа H + -PPase, широко распространенная в растениях, некоторых водорослях, простейших и бактериях, имеет простую структуру, состоящую из олигопептидной цепи, и составляет примерно от 1 до 10% мембранных белков (Zhao, Liu, 1999; Maeshima, 2000).
V-АТФаза и V-ППаза не только служат ключевыми ферментами протонной помпы тонопластов, но также функционируют как детерминанты повторного использования NO 3 − (Shen et al., 2003). С точки зрения снижения накопления NO 3 − в вакуолях растений и дальнейшего повышения эффективности использования азота сельскохозяйственными культурами большое значение имеет выяснение механизма распространения NO 3 − на короткие расстояния, связанного с активность протонной помпы тонопласта (Han et al., 2014). В исследовании, посвященном изучению двух сортов проростков рапса с высокой и низкой эффективностью использования азота соответственно, Han et al. (2015) показали, что активность V-АТФазы и V-РРазы, а также скорость внутреннего потока NO 3 − в вакуоли у высокоэффективного сорта были ниже по сравнению с таковыми у сорта с низкой эффективностью использования азота.Это указывает на то, что в первом случае большее количество NO 3 − направляется в цитоплазму для последующего метаболизма, тем самым снижая вакуолярное содержание NO 3 − и, следовательно, повышая эффективность использования азота семенами рапса ( Хан и др., 2016). Результаты дальнейшего исследования показали, что емкость хранения для NO 3 − ограничена в отсутствие генов AtVHA-a2 и AtVHA-a3 с vha-a2 vha-a3 . двойной мутант содержал на 80% меньше NO 3 — , тогда как общая активность редуктазы NO 3 — увеличилась на 90 % (Krebs et al., 2010). Точно так же было замечено, что вакуоли мутантов atvha-a2 , atvha-a3 и atavp1 содержат меньше NO 3 − (Liao et al.
(2015) показали, что активность V-АТФазы и V-РРазы, а также скорость внутреннего потока NO 3 − в вакуоли у высокоэффективного сорта были ниже по сравнению с таковыми у сорта с низкой эффективностью использования азота.Это указывает на то, что в первом случае большее количество NO 3 − направляется в цитоплазму для последующего метаболизма, тем самым снижая вакуолярное содержание NO 3 − и, следовательно, повышая эффективность использования азота семенами рапса ( Хан и др., 2016). Результаты дальнейшего исследования показали, что емкость хранения для NO 3 − ограничена в отсутствие генов AtVHA-a2 и AtVHA-a3 с vha-a2 vha-a3 . двойной мутант содержал на 80% меньше NO 3 — , тогда как общая активность редуктазы NO 3 — увеличилась на 90 % (Krebs et al., 2010). Точно так же было замечено, что вакуоли мутантов atvha-a2 , atvha-a3 и atavp1 содержат меньше NO 3 − (Liao et al. , 2019).
, 2019).
Управляемый вакуолярными протонными насосами NO 3 − проникает в вакуоль через белки хлоридных каналов (Gaxiola et al., 2001; De Angeli et al., 2006; Brüx et al., 2008). Каналы хлорида и яблочной кислоты, два основных типа анионных каналов, являются внутренними выпрямляющими каналами, расположенными в тонопласте (Qu and Yu, 2008).Белки CLC облегчают поток анионов, таких как Cl — и NO 3 — , тогда как транспорт глутамата ограничен. Белки CLC активируются только в присутствии цитоплазматического Ca 2+ (Berechi et al., 1999). Этой активации способствует протеинкиназа домена кальмодулина (CDPK) в присутствии АТФ и ингибируется нифлумовой кислотой. В отличие от обычных анионных каналов, CLC не ингибируются 4,4′-динитростильбен-2,2′-дисульфоновой кислотой (White and Broadley, 2001; Yu and Liu, 2004; Qu et al., 2009).
В Arabidopsis , NRT2.7 и CLCa являются двумя переносчиками, которые облегчают перенос NO 3 − в вакуоль (Geelen et al.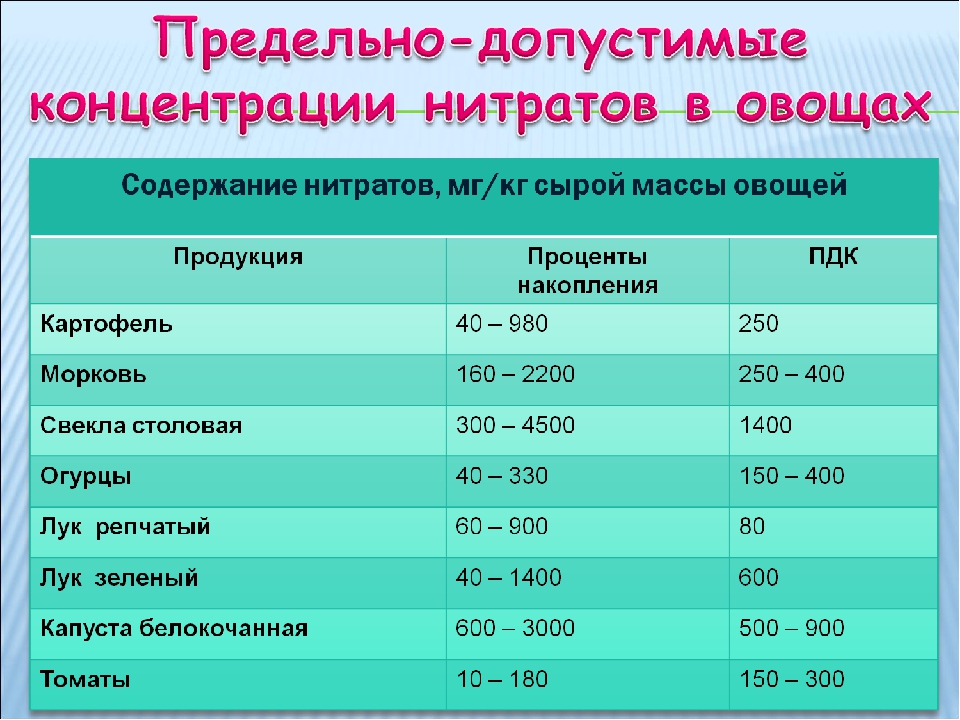 , 2000; Chopin et al., 2007). Другие транспортеры с потенциально сходными функциями включают CLCc и NPF6.2 (Chiu et al., 2004; Harada et al., 2004). Семь членов семейства CLC были идентифицированы у Arabidopsis thaliana , и De Angeli et al. (2006) были первыми, кто продемонстрировал, что AtCLCa является локализованным в тонопласте 2NO 3 − /H + антипортером, участвующим в регуляции NO 3 − секвестрация в вакуоли.Установлено, что накопление NO 3 − в вакуоли снижено примерно на 50 %, а содержание NO 3 − снижено как в побегах, так и в корнях у мутантных растений atclca ( Geelen et al., 2000; De Angeli et al., 2006; Monachello et al., 2009). Аналогичные результаты были получены в исследовании Liao et al. (2019). Предполагается, что AtCLCc также участвует в вакуолярном запасании NO 3 − , поскольку он локализован в тонопласте, а растения с мутацией в этом протоне характеризуются более низким содержанием NO 3 − (Harada et al.
, 2000; Chopin et al., 2007). Другие транспортеры с потенциально сходными функциями включают CLCc и NPF6.2 (Chiu et al., 2004; Harada et al., 2004). Семь членов семейства CLC были идентифицированы у Arabidopsis thaliana , и De Angeli et al. (2006) были первыми, кто продемонстрировал, что AtCLCa является локализованным в тонопласте 2NO 3 − /H + антипортером, участвующим в регуляции NO 3 − секвестрация в вакуоли.Установлено, что накопление NO 3 − в вакуоли снижено примерно на 50 %, а содержание NO 3 − снижено как в побегах, так и в корнях у мутантных растений atclca ( Geelen et al., 2000; De Angeli et al., 2006; Monachello et al., 2009). Аналогичные результаты были получены в исследовании Liao et al. (2019). Предполагается, что AtCLCc также участвует в вакуолярном запасании NO 3 − , поскольку он локализован в тонопласте, а растения с мутацией в этом протоне характеризуются более низким содержанием NO 3 − (Harada et al. , 2004). Среди белков NPF у Arabidopsis , AtNPF6.2 специфически экспрессируется в черешках, богатых NO 3 — , что указывает на то, что он может участвовать в накоплении NO 3 — в вакуолях клеток черешка. Однако функция AtNPF6.2 еще предстоит окончательно установить из-за отсутствия данных, указывающих, расположен ли этот белок в вакуолярной мембране (Chiu et al., 2004). AtNRT2.7, который находится в тонопласте и экспрессируется исключительно в семенах, на сегодняшний день является единственным белком в семействе NRT, участие которого в вакуолярном хранении NO 3 — подтверждено.Внутри семян этот белок отвечает за транспорт NO 3 − из цитоплазмы в вакуоль для хранения, тем самым способствуя накоплению азота в семенах (Chopin et al., 2007). По сравнению с белками семейства NPF и NRT2 белки CLC в первую очередь ответственны за вакуолярное накопление NO 3 − в процессе роста растений, и снижение их активности усиливает утилизацию NO 3 − , тем самым улучшая азот- эффективность использования сельскохозяйственных культур (Geelen et al.
, 2004). Среди белков NPF у Arabidopsis , AtNPF6.2 специфически экспрессируется в черешках, богатых NO 3 — , что указывает на то, что он может участвовать в накоплении NO 3 — в вакуолях клеток черешка. Однако функция AtNPF6.2 еще предстоит окончательно установить из-за отсутствия данных, указывающих, расположен ли этот белок в вакуолярной мембране (Chiu et al., 2004). AtNRT2.7, который находится в тонопласте и экспрессируется исключительно в семенах, на сегодняшний день является единственным белком в семействе NRT, участие которого в вакуолярном хранении NO 3 — подтверждено.Внутри семян этот белок отвечает за транспорт NO 3 − из цитоплазмы в вакуоль для хранения, тем самым способствуя накоплению азота в семенах (Chopin et al., 2007). По сравнению с белками семейства NPF и NRT2 белки CLC в первую очередь ответственны за вакуолярное накопление NO 3 − в процессе роста растений, и снижение их активности усиливает утилизацию NO 3 − , тем самым улучшая азот- эффективность использования сельскохозяйственных культур (Geelen et al. , 2000; Де Анджели и др., 2006 г.; Моначелло и др., 2009).
, 2000; Де Анджели и др., 2006 г.; Моначелло и др., 2009).
В отношении оттока NO 3 − из вакуолей установлено, что локализованные в тонопласте белки AtCLCb и OsNPF7.2 могут транспортировать NO 3 − , хотя прямых доказательств в настоящее время нет. чтобы указать, участвуют ли эти белки в вакуолярном притоке или оттоке NO 3 — (von der Fecht-Bartenbach et al., 2010; Hu et al., 2016). ВНПФ5.11, AtNPF5.12 и AtNPF5.16 регулируют перераспределение NO 3 — между корнями и побегами, опосредуя отток NO 3 — из вакуоли в цитозоль. У тройных мутантов, характеризующихся разрушением AtNPF5.11 , AtNPF5.12 и AtNPF5.16 , было обнаружено, что большие количества корневых 15 NO 3 − побеги (He et al., 2017). Более того, предполагается, что локализованный в тонопласте OsNPF7.2 может также участвовать в оттоке NO 3 − из вакуолей, а гетерологичная экспрессия в ооцитах Xenopus laevis показала, что он опосредует абсорбцию NO 3 − , хотя на сегодняшний день он еще не изучен. необходимо продемонстрировать, приводит ли функциональное нарушение OsNPF7.2 к накоплению NO 3 − в вакуолях (von der Fecht-Bartenbach et al., 2010; Hu et al., 2016). Кроме того, поступление NO 3 − оказывает значительное влияние на распределение NO 3 − как в метаболическом пуле, так и в запасном пуле листовых пластинок трех листовых овощей (рапс, пекинская капуста и шпинат) ( Чен и др., 2004).
необходимо продемонстрировать, приводит ли функциональное нарушение OsNPF7.2 к накоплению NO 3 − в вакуолях (von der Fecht-Bartenbach et al., 2010; Hu et al., 2016). Кроме того, поступление NO 3 − оказывает значительное влияние на распределение NO 3 − как в метаболическом пуле, так и в запасном пуле листовых пластинок трех листовых овощей (рапс, пекинская капуста и шпинат) ( Чен и др., 2004).
Антипортер 2NO 3 − /H + , расположенный в тонопласте, способствует переносу NO 3 − в вакуоль из цитоплазмы (De Angeli et al., 2006) ., 2010). С точки зрения эффективности использования азота роль вакуолярного NO 3 − в поддержании осмотического баланса внутри вакуоли считается расточительной (Shen et al., 2003). Однако можно ли заменить вакуолярный NO 3 − на Cl − для поддержания осмотического давления клетки в определенном диапазоне и тем самым снизить уровень накопленного в вакуоли NO 3 − , остается выяснить. 3 − Транспорт в овощах
3 − Транспорт в овощах
Часть NO 3 − , поглощаемая корнями растений, сохраняется в вакуолях или ассимилируется в органический азот через ряд реакции, катализируемые NO 3 − редуктазой, нитритредуктазой, глутаминсинтетазой и глутаматсинтазой (Williams et al., 1987) (рис. 1C). Однако большая часть NO 3 — , поглощенная корнями, транспортируется через ткани коры в каналы ксилемы для транспортировки на большие расстояния к различным тканям и органам побегов для последующей ассимиляции и использования в процессе роста и развития растений (Han et al., 2016; Чжан, 2017 г.) (рис. 1Б).
NO 3 − в основном транспортируется вверх по ксилеме и вниз по флоэме (Dechorgnat et al., 2011). Перенос на большие расстояния и распределение NO 3 − между корнями и побегами у Arabidopsis в основном совместно регулируются NPF7.3 и NPF7. 2 , двумя членами семейства PTR, выражение из которых сильно индуцируется NO 3 − (Lin et al., 2008; Ли и др., 2010; Чен и др., 2012; Леран и др., 2014 г.; Zhang Z.H. et al., 2014) (рис. 1C). AtNPF7.3 преимущественно экспрессируется в столбчатых клетках оболочки, окружающих протоксилему в корне, и отвечает за загрузку NO 3 — из цитоплазмы корня в ксилему для транспорта к побегам (Lin et al. , 2008). AtNPF7.2 экспрессируется в клетках паренхимы ксилемы и влияет на транспорт NO 3 − от корней к побегам, регулируя выгрузку NO 3 − из ксилемы (Li et al., 2010). Таким образом, хотя они и играют противоположные роли в загрузке и выгрузке NO 3 − в ксилему и из нее, AtNPF7.3 и AtNPF7.2 , соответственно, совместно способствуют переносу NO на большие расстояния. 3 − от корней к побегам. Кроме того, было показано, что OsNPF2.
2 , двумя членами семейства PTR, выражение из которых сильно индуцируется NO 3 − (Lin et al., 2008; Ли и др., 2010; Чен и др., 2012; Леран и др., 2014 г.; Zhang Z.H. et al., 2014) (рис. 1C). AtNPF7.3 преимущественно экспрессируется в столбчатых клетках оболочки, окружающих протоксилему в корне, и отвечает за загрузку NO 3 — из цитоплазмы корня в ксилему для транспорта к побегам (Lin et al. , 2008). AtNPF7.2 экспрессируется в клетках паренхимы ксилемы и влияет на транспорт NO 3 − от корней к побегам, регулируя выгрузку NO 3 − из ксилемы (Li et al., 2010). Таким образом, хотя они и играют противоположные роли в загрузке и выгрузке NO 3 − в ксилему и из нее, AtNPF7.3 и AtNPF7.2 , соответственно, совместно способствуют переносу NO на большие расстояния. 3 − от корней к побегам. Кроме того, было показано, что OsNPF2. 2 участвует в выгрузке NO 3 — из ксилемы, тем самым способствуя переходу от корня к побегу NO 3 — и развитию растений.Было обнаружено, что мутантные растения osnpf2.2 поддерживают высокие уровни NO 3 − в корнях и имеют низкое соотношение побег:корень NO 3 − (Li et al., 2015). Более того, было замечено, что AtNPF2.3 играет важную роль в транслокации NO 3 — от корня к побегу у растений, находящихся в условиях засоления (Taochy et al., 2015).
2 участвует в выгрузке NO 3 — из ксилемы, тем самым способствуя переходу от корня к побегу NO 3 — и развитию растений.Было обнаружено, что мутантные растения osnpf2.2 поддерживают высокие уровни NO 3 − в корнях и имеют низкое соотношение побег:корень NO 3 − (Li et al., 2015). Более того, было замечено, что AtNPF2.3 играет важную роль в транслокации NO 3 — от корня к побегу у растений, находящихся в условиях засоления (Taochy et al., 2015).
В настоящее время AtNPF2.9 является единственным геном, который, как было подтверждено, играет роль в загрузке NO 3 − во флоэму корня и негативно регулирует транспорт NO от корня к побегу 3 − (Фан и др., 2009; Ван и Цай, 2011). Также было установлено, что AtNPF5.11 , AtNPF5.12 и AtNPF5.16 играют роль в поглощении NO 3 − из вакуоли в цитоплазму у Arabidopsis соотношение побег:корень, а у тройного мутанта по этим генам было обнаружено, что большее количество NO 3 − перемещается в побеги (He et al. , 2017). В Arabidopsis , AtNPF2.9, AtNPF7.2, и AtNPF7.3 являются основными переносчиками NO 3 − , участвующими в регуляции дальнего транспорта и перераспределения NO 3 − от корней к побегам (рис. 1В). В связи с этим следует отметить, что концентрация NO 3 − , транспортируемых в ксилеме, как правило, в несколько десятков и сотен раз выше, чем во флоэме, что, соответственно, объясняет, почему исследования NO 3 − Распространение в побегах и корнях в основном сосредоточено на переносе NO 3 − в ксилему, а не во флоэму (Lin et al., 2008; Ли и др., 2010; Ван и Цай, 2011). На сегодняшний день исследования взаимоотношений между генами NPF и переносом на большие расстояния NO 3 − у сельскохозяйственных культур проводились в основном на пшенице, рисе и рапсе. Однако у пшеницы были изучены только реакции генов NPF7.3 и NPF7.2 на азотный стресс (Xuan et al.
, 2017). В Arabidopsis , AtNPF2.9, AtNPF7.2, и AtNPF7.3 являются основными переносчиками NO 3 − , участвующими в регуляции дальнего транспорта и перераспределения NO 3 − от корней к побегам (рис. 1В). В связи с этим следует отметить, что концентрация NO 3 − , транспортируемых в ксилеме, как правило, в несколько десятков и сотен раз выше, чем во флоэме, что, соответственно, объясняет, почему исследования NO 3 − Распространение в побегах и корнях в основном сосредоточено на переносе NO 3 − в ксилему, а не во флоэму (Lin et al., 2008; Ли и др., 2010; Ван и Цай, 2011). На сегодняшний день исследования взаимоотношений между генами NPF и переносом на большие расстояния NO 3 − у сельскохозяйственных культур проводились в основном на пшенице, рисе и рапсе. Однако у пшеницы были изучены только реакции генов NPF7.3 и NPF7.2 на азотный стресс (Xuan et al. , 2014), тогда как физиологические характеристики азота были проанализированы у линий риса, сверхэкспрессирующих OsNPF7. .3 (март 2011 г.).В наших исследованиях мы проанализировали ответ NPF7.3 и NPF7.2 на дефицит NO 3 − и построили сеть коэкспрессии для идентификации ключевых генов, участвующих в NO 3 − . транспорт от корня к побегу у проростков рапса (Hua et al., 2018; Liang et al., 2019). Свидетельства, накопленные к настоящему времени, по существу подтверждают, что NPF7.3 и NPF7.2 регулируют перенос и распространение NO 3 − в ряде сельскохозяйственных культур, в которых они играют роли, аналогичные наблюдаемым в A. .талиана . Таким образом, мы полагаем, что отношения между NO 3 — дальним транспортом и генами NPF, описанные в Arabidopsis , также могут быть применимы к культурным культурам или овощам.
, 2014), тогда как физиологические характеристики азота были проанализированы у линий риса, сверхэкспрессирующих OsNPF7. .3 (март 2011 г.).В наших исследованиях мы проанализировали ответ NPF7.3 и NPF7.2 на дефицит NO 3 − и построили сеть коэкспрессии для идентификации ключевых генов, участвующих в NO 3 − . транспорт от корня к побегу у проростков рапса (Hua et al., 2018; Liang et al., 2019). Свидетельства, накопленные к настоящему времени, по существу подтверждают, что NPF7.3 и NPF7.2 регулируют перенос и распространение NO 3 − в ряде сельскохозяйственных культур, в которых они играют роли, аналогичные наблюдаемым в A. .талиана . Таким образом, мы полагаем, что отношения между NO 3 — дальним транспортом и генами NPF, описанные в Arabidopsis , также могут быть применимы к культурным культурам или овощам.
Известно, что поток ксилемы находится под сильным влиянием транспирации, которая, в свою очередь, оказывает значительное влияние на перенос NO на большие расстояния 3 − . NO 3 − , загруженный в ксилему, непрерывно транспортируется в надземные части растений, опосредованно влиянием транспирации, тем самым способствуя транспорту NO 3 − от корней к побегам ( Ли и др., 2010; Чен и др., 2012). Последовательно было продемонстрировано, что ингибирование транспирации снижает транспорт NO 3 − к побегам растений гороха, что приводит к увеличению накопления NO − в корнях и снижению содержания в съедобных частях растений (Hernandez et al., 1997). Дальний транспорт NO 3 — не только определяет распределение и ассимиляцию в различных тканях, но также представляет собой важный физиологический механизм, с помощью которого растения реагируют на изменение окружающей среды (Zhang G.Б. и др., 2014). Чен и др. (2012) и Li et al. (2010) показали, что транспирация регулирует транспорт питательных элементов от корней к побегам в нормальных условиях, тогда как накопление NO 3 − в корнях также опосредовано AtNPF7.
NO 3 − , загруженный в ксилему, непрерывно транспортируется в надземные части растений, опосредованно влиянием транспирации, тем самым способствуя транспорту NO 3 − от корней к побегам ( Ли и др., 2010; Чен и др., 2012). Последовательно было продемонстрировано, что ингибирование транспирации снижает транспорт NO 3 − к побегам растений гороха, что приводит к увеличению накопления NO − в корнях и снижению содержания в съедобных частях растений (Hernandez et al., 1997). Дальний транспорт NO 3 — не только определяет распределение и ассимиляцию в различных тканях, но также представляет собой важный физиологический механизм, с помощью которого растения реагируют на изменение окружающей среды (Zhang G.Б. и др., 2014). Чен и др. (2012) и Li et al. (2010) показали, что транспирация регулирует транспорт питательных элементов от корней к побегам в нормальных условиях, тогда как накопление NO 3 − в корнях также опосредовано AtNPF7. 3 и AtNPF7.2 , может быть доминирующим регулирующим фактором в распространении NO 3 − в растениях, подвергшихся стрессу. Например, в условиях кадмиевого стресса было замечено, что растения дикого типа Arabidopsis сохраняют более высокое отношение корня к побегу NO 3 — , чем atnpf7.2 мутантных растений, что указывает на то, что это соотношение активно регулируется NPF7.2 и другими переносчиками, а не пассивно транспирацией (Li et al., 2010). Таким образом, ингибируя экспрессию гена NPF7.3 и усиливая экспрессию гена NPF7.2 в растениях, возможно контролировать транспорт NO 3 − на большие расстояния от корней к побегам. который представляет собой полезный подход к снижению содержания NO 3 − в листовых овощах.
3 и AtNPF7.2 , может быть доминирующим регулирующим фактором в распространении NO 3 − в растениях, подвергшихся стрессу. Например, в условиях кадмиевого стресса было замечено, что растения дикого типа Arabidopsis сохраняют более высокое отношение корня к побегу NO 3 — , чем atnpf7.2 мутантных растений, что указывает на то, что это соотношение активно регулируется NPF7.2 и другими переносчиками, а не пассивно транспирацией (Li et al., 2010). Таким образом, ингибируя экспрессию гена NPF7.3 и усиливая экспрессию гена NPF7.2 в растениях, возможно контролировать транспорт NO 3 − на большие расстояния от корней к побегам. который представляет собой полезный подход к снижению содержания NO 3 − в листовых овощах.
Выводы и будущие разработки
В растениях накопление NO 3 − зависит от его абсорбции и метаболизма. Растения активно поглощают NO 3 − из окружающей среды посредством протонно-нитратного механизма (Wang et al., 2018). Поглощенный растениями NO 3 − может непосредственно усваиваться в органический азот, секретироваться в ризосферу, накапливаться в вакуоли или транспортироваться от корней к побегам (Zhang, 2017).Таким образом, на концентрацию NO 3 − в растениях влияют многочисленные процессы, между которыми существует тесная взаимозависимость, которая способствует скоординированному регулированию накопления NO 3 − в растениях.
Растения активно поглощают NO 3 − из окружающей среды посредством протонно-нитратного механизма (Wang et al., 2018). Поглощенный растениями NO 3 − может непосредственно усваиваться в органический азот, секретироваться в ризосферу, накапливаться в вакуоли или транспортироваться от корней к побегам (Zhang, 2017).Таким образом, на концентрацию NO 3 − в растениях влияют многочисленные процессы, между которыми существует тесная взаимозависимость, которая способствует скоординированному регулированию накопления NO 3 − в растениях.
Vacuolar NO 3 − накопление и высвобождение играют важную роль в регулировании концентрации и перераспределения NO 3 − . На приток вакуолярного NO 3 − в основном влияют локализованные в тонопласте белки, такие как AtCLCa, AtCLCc, AtNPF6.2, и AtNRT2.7, в то время как AtCLCb и OsNPF7.
 3 − содержание овощей.
3 − содержание овощей.
Вакуолярно-цитоплазматическое распределение NO 3 − влияет не только на распределение и утилизацию NO 3 − (Gaxiola et al., 2001; Brüx et al., 2008; Krebs et al., 2010), но также влияет на экспрессию и функцию генов, индуцированных NO 3 − (Glass et al., 2002; Huang et al., 2013). NPF2.9 , NPF7.3 и NPF7.2 , которые отвечают за NO 3 − загрузку во флоэму, загрузку в ксилему и выгрузку из ксилемы, соответственно, являются главные регуляторы дальнего следования НО 3 − транспорта.Однако флоэма в первую очередь участвует в транспорте органического азота, тогда как концентрация неорганического азота, переносимого флоэмой, обычно в десятки-сотни раз меньше, чем в ксилеме (Lin et al., 2008; Fan и др., 2009; Ли и др., 2010; Ван и Цай, 2011). Таким образом, НПФ7.3 и НПФ7.2 являются основными регуляторами дальних перевозок NO 3 − . Повышение активности белка NPF7.2 в сочетании со снижением активности NPF7.3 будет способствовать благоприятному регулированию транспорта NO 3 − на большие расстояния, тем самым снижая транспорт NO 3 − от корней к побегам и, таким образом, содержание NO 3 − в листовых овощах.
Повышение активности белка NPF7.2 в сочетании со снижением активности NPF7.3 будет способствовать благоприятному регулированию транспорта NO 3 − на большие расстояния, тем самым снижая транспорт NO 3 − от корней к побегам и, таким образом, содержание NO 3 − в листовых овощах.
Исследование механизмов, лежащих в основе переноса NO 3 − на короткие и большие расстояния, требует дальнейшего расширения для решения следующих вопросов (Li et al., 2010; Schroeder et al., 2013). (1) В дополнение к регуляции осмотических функций, как хранение NO 3 — в вакуолях влияет на экспрессию и функцию его индуцируемых генов? 2. Чем отличается вклад хлоридных каналов (ХЛК) и протонных насосов в распределение NO 3 − в вакуолях? (3) Учитывая, что транспорт NO 3 − из цитоплазмы в вакуоли в первую очередь регулируется CLCa, как этот процесс влияет на дальнейшую ассимиляцию NO 3 − ? На основании результатов предыдущих исследований вакуолярная система распределения NO 3 − , играющая важную роль в коротком расстоянии NO 3 − , и система транспортировки сосудистых пучков на большие расстояния , который важен при транспортировке NO 3 − на большие расстояния, определены в качестве основных целей для дальнейших исследований механизмов, лежащих в основе распространения NO 3 − на большие расстояния. Лучшее понимание этих механизмов будет способствовать более эффективному контролю содержания NO 3 − в растениях и даст важные рекомендации по селекции и выращиванию листовых овощей с низкими концентрациями NO 3 − .
Лучшее понимание этих механизмов будет способствовать более эффективному контролю содержания NO 3 − в растениях и даст важные рекомендации по селекции и выращиванию листовых овощей с низкими концентрациями NO 3 − .
Вклад авторов
GL организовал и написал оригинальную рукопись. GL и ZZ обсудили и отредактировали рукопись и утвердили окончательную версию.
Финансирование
Эта работа частично финансировалась Национальной ключевой программой исследований и разработок Китая (2017YFD0200100 и 2017YFD0200103), Программой найма иностранных экспертов провинции Хунань, Национальной системой технологий производства масличного рапса Китая, «План 2011» Министерством образования Китая, а также Проект строительства двойного первого класса Хунаньского сельскохозяйственного университета (kxk201801005).
Конфликт интересов
Авторы заявляют, что исследование проводилось при отсутствии каких-либо коммерческих или финансовых отношений, которые могли бы быть истолкованы как потенциальный конфликт интересов.
Ссылки
Анджана С.У., Икбал М. (2007). Накопление нитратов в растениях, факторы, влияющие на этот процесс, и последствия для здоровья человека. Агрон. Поддерживать Дев. 27, 45–57. doi: 10.1051/agro:2006021
CrossRef Полный текст | Google Scholar
Бахадоран З., Мирмиран П., Джедди С., Азизи Ф., Гасеми А., Хадаэг Ф. (2016). Содержание нитратов и нитритов в овощах, фруктах, злаках, бобовых, молочных продуктах, мясе и мясных продуктах. J. Food Compos. Анальный. 51, 93–105. doi: 10.1016/j.jfca.2016.06.006
CrossRef Full Text | Google Scholar
Беречи Г., Варга З., Ван Ирен Ф., Ван Дуйн Б. (1999). Анионные каналы в мембране харакориллинового тонопласта: кальциевая зависимость и ректификация. J. Член. биол. 172, 159–168.doi: 10.1007/s0023293
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Bondonno, C.P., Blekkenhorst, L.C., Liu, A.H., Bondonno, N.P., Ward, N.C., Croft, K.D., et al.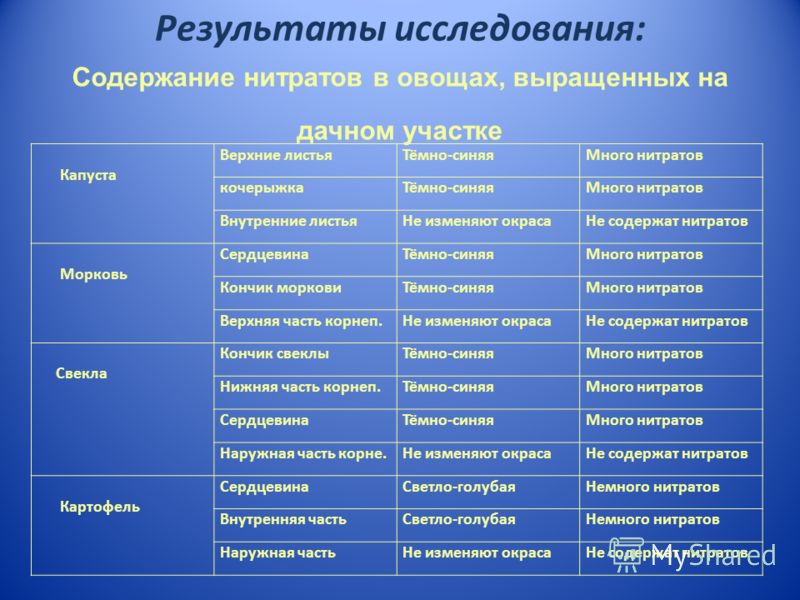 (2018). Биоактивные нитраты растительного происхождения и здоровье сердечно-сосудистой системы. Мол. Асп. Мед. 61, 83–91. doi: 10.1016/j.mam.2017.08.001
(2018). Биоактивные нитраты растительного происхождения и здоровье сердечно-сосудистой системы. Мол. Асп. Мед. 61, 83–91. doi: 10.1016/j.mam.2017.08.001
Полный текст CrossRef | Google Scholar
Брюкс А., Лю Т. Ю., Кребс М., Штирхоф Ю. Д., Ломанн Дж. У., Мирш О. и др. (2008).Снижение активности V-ATPPase в сети trans-Golgi вызывает оксилипин-зависимое ингибирование роста гипокотиля у Arabidopsis . Растительная клетка 20, 1088–1100. doi: 10.1105/tpc.108.058362
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Бернс И. Г., Чжан К., Тернер М. К., Мичем М., Аль-Редхиман К., Линн Дж. и др. (2011). Скрининг влияния генотипа и окружающей среды на накопление нитратов у 24 видов молодого салата. J. Sci. Фуд Агрик. 91, 553–562. doi: 10.1002/jsfa.4220
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Картер К., Пан С., Зухар Дж., Авила Э. Л., Гирке Т., Райхель Н. В. (2004). Протеом вегетативной вакуоли Arabidopsis thaliana обнаруживает предсказанные и неожиданные белки.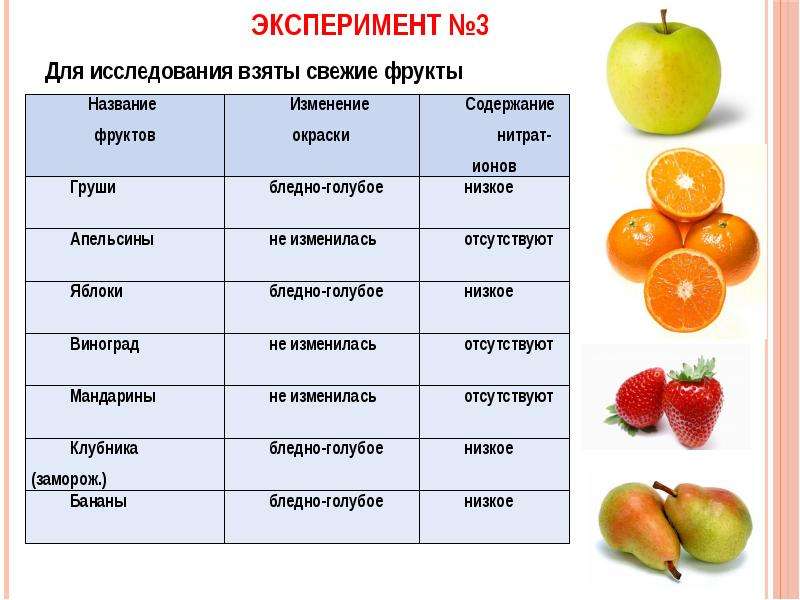 Растительная клетка 16, 3285–3303. doi: 10.1105/tpc.104.027078
Растительная клетка 16, 3285–3303. doi: 10.1105/tpc.104.027078
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Чен Б. М., Ван З. Х., Ли С. Х., Wang, G.X., Song, H.X., Wang, X.N. (2004). Влияние поступления нитратов на рост растений, накопление нитратов, метаболическую концентрацию нитратов и активность нитратредуктазы в трех листовых овощах. Растениевод. 167, 635–643. doi: 10.1016/j.plantsci.2004.05.015
CrossRef Полный текст | Google Scholar
Chen, CZ, Lv, XF, Li, JY, Yi, HY, Gong, JM (2012). Arabidopsis NRT1.5 является еще одним важным компонентом в регуляции перераспределения нитратов и стрессоустойчивости. Завод физиол. 159, 1582–1590. doi: 10.1104/pp.112.199257
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Четти, А. А., Прасад, С., Пиньо, О. К., де Мораис, К. М. (2018). Оценочное потребление нитратов и нитритов из мяса, потребляемого на Фиджи. Пищевая хим. 278, 630–635. doi: 10.1016/j.foodchem.2018.11.081
278, 630–635. doi: 10.1016/j.foodchem.2018.11.081
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Чиу, К.С., Линь, К.С., Ся, А.П., Су, Р.К., Лин, Х.Л., Цай, Ю. Ф. (2004). Мутация переносчика нитратов AtNRT1.4 приводит к снижению содержания нитратов в черешках и изменению развития листьев. Физиология клеток растений. 45, 1139–1148. doi: 10.1093/pcp/pch243
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Шопен Ф., Орсель М., Дорбе М. Ф., Шардон Ф., Труонг Х. Н., Миллер А. Дж. и др. (2007). Транспортер нитратов Arabidopsis ATNRT2.7 контролирует содержание нитратов в семенах. Растительная клетка 19, 1590–1602.doi: 10.1105/tpc.107.050542
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Cipriano, D. J., Wang, Y., Bond, S., Hinton, A., Jefferies, K. C., Qi, J., et al. (2008). Структура и регуляция вакуолярной АТФазы. Биохим. Биофиз. Acta 1777, 599–604.
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Де Анджели А., Моначелло Д., Эфритихин Г., Фрашисс Ж. М., Томин С., Гамбаль Ф., и другие. (2006). Нитрат/протонный антипортер AtCLCa опосредует накопление нитратов в вакуолях растений. Природа 442, 939–942. doi: 10.1038/nature05013
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Дечоргнат Дж., Нгуен С. Т., Арменго П., Жосье М., Дятлофф Э., Филлер С. и др. (2011). Из почвы в семена: долгий путь нитратов в растениях. Дж. Экспл. Бот. 62, 1349–1359. doi: 10.1093/jxb/erq409
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Ду, С.Т., Ли, Л.Л., Чжан, Ю.С., Линь, X.Ю. (2008). Различия в накоплении нитратов и выбор сорта у разных генотипов пекинской капусты ( Brassica chinensis L.). J. Питательные вещества для растений. 14, 969–975. doi: 10.11674/zwyf.2008.0524
Полный текст CrossRef | Google Scholar
Fan, S. C., Lin, C.S., Hsu, P.K., Lin, S.H., Tasy, YF (2009). Транспортер нитратов Arabidopsis NRT1.7, экспрессируемый во флоэме, отвечает за ремобилизацию нитратов от источника к приемнику. Растительная клетка 21, 2750–2761. doi: 10.1105/tpc.109.067603
C., Lin, C.S., Hsu, P.K., Lin, S.H., Tasy, YF (2009). Транспортер нитратов Arabidopsis NRT1.7, экспрессируемый во флоэме, отвечает за ремобилизацию нитратов от источника к приемнику. Растительная клетка 21, 2750–2761. doi: 10.1105/tpc.109.067603
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Filleur, S., Dorbe, M. F., Cerezo, M., Orsel, M., Granier, F., Gojon, A., et al. (2001). У мутанта Т-ДНК Arabidopsis , затронутого генами NRT2 , нарушено поглощение нитратов. ФЭБС Письмо. 489, 220–224. doi: 10.1016/S0014-5793(01)02096-8
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Гаксиола, Р.A., Li, J., Undurraga, S., Dang, L.M., Allen, G.J., Alper, S.L., et al. (2001). Засухоустойчивые и солеустойчивые растения являются результатом чрезмерной экспрессии насоса AVP1 H + . Проц. Натл. акад. науч. США 98, 11444–11449. doi: 10.1073/pnas.1
398PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Geelen, D. , Lurin, C., Bouchez, D., Frachisse, J.M., Lelièvre, F., Courtial, B., et al. (2000). Нарушение предполагаемого гена анионного канала AtCLC-a у Arabidopsis предполагает роль в регуляции содержания нитратов. Завод J. 21, 259–267. doi: 10.1046/j.1365-313x.2000.00680.x
, Lurin, C., Bouchez, D., Frachisse, J.M., Lelièvre, F., Courtial, B., et al. (2000). Нарушение предполагаемого гена анионного канала AtCLC-a у Arabidopsis предполагает роль в регуляции содержания нитратов. Завод J. 21, 259–267. doi: 10.1046/j.1365-313x.2000.00680.x
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Гласс, А. Д., Бритто, Д. Т., Кайзер, Б. Н., Кингхорн, Дж. Р., Кронцукер, Х. Дж., Кумар, А., и др. (2002). Регуляция транспортных систем нитратов и аммония в растениях. Дж. Экспл. Бот. 53, 855–864. doi: 10.1093/jexbot/53.370.855
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Хан Ю. Л., Лю Кью., Gu, J.D., Gong, J.M., Guan, C.Y., Lepo, J.E., et al. (2014). V-АТФаза и V-ППаза при воздействии на тонопласт NO 3 – Содержание в Brassica napus путем контроля распределения NO 3 – Между цитоплазмой и вакуолью. J. Регулирование роста растений. 34, 22–34. doi: 10.1007/s00344-014-9439-8
CrossRef Full Text | Google Scholar
Han, Y.L., Liao, Q., Yu, Y., Song, H.X., Liu, Q., Rong, X.M., et al. (2015).Механизмы реутилизации нитратов в тонопласте двух генотипов Brassica napus с разной эффективностью использования азота. Acta Physiol. Planturum 37, 42. doi: 10.1007/s11738-014-1744-0
CrossRef Полный текст | Google Scholar
Хань Ю. Л., Сун Х. Х., Ляо К., Ю Ю., Цзянь С. Ф., Лепо Дж. Э. и др. (2016). Эффективность использования азота опосредована вакуолярной способностью связывать нитраты в корнях Brassica napus . Завод физиол. 170, 1684–1698. doi: 10.1104/pp.15.01377
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Харада Х., Куромори Т., Хираяма Т., Шинозаки К., Ли Р. А. (2004). Количественный анализ локусов признаков накопления нитратов у Arabidopsis привел к исследованию вклада гена анионного канала AtCLC-c в изменение уровня нитратов. Дж. Экспл. Бот. 55, 2005–2014 гг. doi: 10.1093/jxb/erh324
Дж. Экспл. Бот. 55, 2005–2014 гг. doi: 10.1093/jxb/erh324
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Он, Ю.N., Peng, J.S., Cai, Y., Liu, D.F., Guan, Y., Yi, H.Y., et al. (2017). Локализованные в тонопласте транспортеры поглощения нитратов, участвующие в вакуолярном оттоке и перераспределении нитратов у Arabidopsis . науч. Rep. 7, 6417. doi: 10.1038/s41598-017-06744-5
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Эрнандес, Л. Э., Гарате, А., Карпена Руис, Р. (1997). Влияние кадмия на поглощение, распределение и усвоение нитратов в Pisum sativum . Почва для растений 189, 97–106. doi: 10.1023/A:1004252816355
Полный текст CrossRef | Google Scholar
Hu, R., Qiu, D., Chen, Y., Miller, A.J., Fan, X., Pan, X., et al. (2016). Нокдаун локализованного в тонопласте низкоаффинного переносчика нитратов OsNPF7.2 влияет на рост риса в условиях высокого содержания нитратов. Фронт. Растениевод. 7, 1529. doi: 10.3389/fpls.2016.01529
Фронт. Растениевод. 7, 1529. doi: 10.3389/fpls.2016.01529
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Хуа Ю. П., Чжоу Т., Ляо, К., Сонг, Х. Х., Гуань, К. Ю., Чжан, З. Х. (2018). Геномная идентификация и характеристика генетических вариантов, лежащих в основе дифференциальной эффективности использования азота в аллотетраплоидных генотипах рапса. G3 8, 2757–2771. doi: 10.1534/g3.118.200481
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Хуанг, Северная Каролина, Лю, К. Х., Ло, Х. Дж., Цай, Ю. Ф. (1999). Клонирование и функциональная характеристика гена переносчика нитратов Arabidopsis , который кодирует конститутивный компонент низкоаффинного поглощения. Растительная клетка 11, 1381–1392. doi: 10.1105/tpc.11.8.1381
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Huang, HT, Zhang, ZH, Song, HX (2012). Реутилизация нитратного азота на основе протонного насоса мембраны вакуоли. Подбородок. Дж. Эко. 31, 731–737. doi: 10.13292/j.1000-4890.2012.0142
Подбородок. Дж. Эко. 31, 731–737. doi: 10.13292/j.1000-4890.2012.0142
CrossRef Полный текст | Google Scholar
Huang, H. T., Rong, X. M., Song, H. X., Liu, Q., Liao, Q., Luo, J. P., et al. (2013). Влияние ингибитора нитратредуктазы (NR) на активность NR в масличном рапсе и его связь с содержанием нитратов. Акта Агро. Грех. 39, 1668–1673. doi: 10.3724/SP.J.1006.2013.01668
CrossRef Full Text | Google Scholar
Жакино, М., Вильерс, Ф., Киффер-Жахино, С., Хьювьё, В., Брюлей, К., Гарин, Дж., и др. (2007). Протеомное вскрытие вакуолей Arabidopsis thaliana , выделенных из клеточной культуры. Мол. Клеточная протеомика 6, 394–412. doi: 10.1074/mcp.M600250-MCP200
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Ю, К.X., Буреш, Р.Дж., Ван, З.К., Чжан, Х., Лю, Л.Дж., Ян, Дж.К., и соавт. (2015). Признаки корнеплодов и побегов сортов риса с более высокой урожайностью зерна и более высокой эффективностью использования азота при более низких нормах внесения азота. Полевые культуры Res. 175, 47–55. doi: 10.1016/j.fcr.2015.02.007
Полевые культуры Res. 175, 47–55. doi: 10.1016/j.fcr.2015.02.007
CrossRef Полный текст | Google Scholar
Киба Т., Фериа-Буррелье А. Б., Лафуж Ф., Лежнева Л., Буте-Мерси С., Орсель М. и др. (2012). Переносчик нитратов Arabidopsis NRT2.4 играет двойную роль в корнях и побегах растений, нуждающихся в азоте. Растительная клетка 24, 245–258. doi: 10.1105/tpc.111.092221
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Кребс М., Бейхл Д., Гёрлих Э., Аль-Рашейд К. А., Мартен И., Штирхоф Ю. Д. и др. (2010). Arabidopsis Активность V-АТФазы в тонопласте необходима для эффективного хранения питательных веществ, но не для накопления натрия. Проц. Натл. акад. науч. США 107, 3251–3256.doi: 10.1073/pnas.05107
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Кригель А., Андрес З., Медзиградский А., Крюгер Ф., Шолль С., Деланг С. и др. (2015). Разделение работы в эндомембранной системе: для вакуолярного закисления требуется комбинированная активность V-АТФазы и V-РРазы. Растительная клетка 27, 3383–3396. doi: 10.1105/tpc.15.00733
Растительная клетка 27, 3383–3396. doi: 10.1105/tpc.15.00733
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Леран С., Варала К., Бойер Дж.К., Чиурацци М., Кроупорд Н., Даниэль-Веделе Ф. и соавт. (2014). Единая номенклатура членов семейства транспортеров нитратов 1/пептидов у растений. Trends Plant Sci. 19, 5–9. doi: 10.1016/j.tplants.2013.08.008
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Лежнева Л., Киба Т., Фериа-Буррелье А. Б., Лафуж Ф., Буте-Мерси С., Зуфан П. и др. (2014). Переносчик нитратов Arabidopsis NRT2.5 играет роль в приобретении и ремобилизации нитратов у растений, испытывающих недостаток азота. Завод J. 80, 230–241. doi: 10.1111/tpj.12626
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Li, JY, Gong, JM (2011). Восприятие и трансдукция сигналов нитратов у высших растений. Завод физиол. Дж. 47, 111–118.
Google Scholar
Li, J. Y., Fu, Y.L., Pike, S.M., Bao, J., Tian, W., Zhang, Y., et al. (2010). Транспортер нитратов Arabidopsis NRT1.8 участвует в удалении нитратов из ксилемного сока и опосредует толерантность к кадмию. Растительная клетка 22, 1633–1646. doi: 10.1105/tpc.110.075242
Y., Fu, Y.L., Pike, S.M., Bao, J., Tian, W., Zhang, Y., et al. (2010). Транспортер нитратов Arabidopsis NRT1.8 участвует в удалении нитратов из ксилемного сока и опосредует толерантность к кадмию. Растительная клетка 22, 1633–1646. doi: 10.1105/tpc.110.075242
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Li, Y., Ouyang, J., Wang, Y.Y., Hu, R., Xia, K., Duan, J., et al. (2015). Нарушение транспортера нитратов риса OsNPF2.2 препятствует транспорту нитратов от корней к побегам и развитию сосудов. науч. Rep. 5, 9635. doi: 10.1038/srep09635
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Лян Г. Х., Хуа Ю.П., Чжоу Т., Ляо К., Сун Х. Х., Чжан З. Х. (2019). Биоинформатический анализ и ответ на нитратно-кадмиевый стресс генов семейства NRT1.5 и NRT1.8 в Brassica napus . Акта Агро. Грех. 45, 365–380. doi: 10.3724/SP.J.1006.2019.84099
CrossRef Full Text | Google Scholar
Ляо, С. Р., Чен, Т., Лю, С. Л. (2002). Образование и функции вакуолей растений. Подбородок. Дж. Клеточная биология. 24, 95–101. doi: 10.3969/j.issn.1674-7666.2002.02.010
Р., Чен, Т., Лю, С. Л. (2002). Образование и функции вакуолей растений. Подбородок. Дж. Клеточная биология. 24, 95–101. doi: 10.3969/j.issn.1674-7666.2002.02.010
CrossRef Full Text | Google Scholar
Ляо, К., Чжоу, Т., Яо, Дж. Ю., Хан, К. Ф., Сонг, Х. Х., Гуань, С. Ю., и др. (2018). Геномная характеристика генов вакуольного переносчика нитратов хлоридных каналов (CLC) и их транскрипционных ответов на различные питательные стрессы в аллотетраплоидных семенах рапса. PLoS Один. 13, e0208648. doi: 10.1371/journal.pone.0208648
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Ляо, К., Jian, S.F., Song, H.X., Guan, C.Y., Lepo, J.E., Ismail, A.M., et al. (2019). Баланс между эффективностью использования азота и устойчивостью к кадмию у сортов Brassica napus и Arabidopsis thaliana . Растениевод. 284, 57–66. doi: 10.1016/j.plantsci.2019.04.003
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Лин С. Х., Куо Х. Ф., Канивенс Г., Лин К. С., Лепетит М., Хсу П. К. и др. (2008). Мутация Arabidopsis NRT1.5 переносчик нитратов вызывает нарушение транспорта нитратов от корней к побегам. Растительная клетка 20, 2514–2528. doi: 10.1105/tpc.108.060244
Х., Куо Х. Ф., Канивенс Г., Лин К. С., Лепетит М., Хсу П. К. и др. (2008). Мутация Arabidopsis NRT1.5 переносчик нитратов вызывает нарушение транспорта нитратов от корней к побегам. Растительная клетка 20, 2514–2528. doi: 10.1105/tpc.108.060244
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Лин, С. М., Цай, Дж. Ю., Сяо, К. Д., Хуан, Ю. Т., Чиу, К. Л., Лю, М. Х., и др. (2012). Кристаллическая структура встроенной в мембрану H + -транслоцирующей пирофосфатазы. Природа 484, 399–403. doi: 10.1038/nature10963
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Лю, К.Х., Хуанг, С.Ю., Цай, Ю.Ф. (1999). CHL1 является переносчиком нитратов Arabidopsis с двойным сродством, участвующим в нескольких фазах поглощения нитратов. Растительная клетка 11, 865–874. doi: 10.1105/tpc.11.5.865
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Луо, Ю. С. (2012). Ход исследований активности Н + -АТФазы в плазматической мембране и вакуолярной мембране растений при солевом стрессе. J. Аньхой Агрик. науч. 40, 1263–1265, 1280. doi: 10.13989/j.cnki.0517-6611.2012.03.001
С. (2012). Ход исследований активности Н + -АТФазы в плазматической мембране и вакуолярной мембране растений при солевом стрессе. J. Аньхой Агрик. науч. 40, 1263–1265, 1280. doi: 10.13989/j.cnki.0517-6611.2012.03.001
CrossRef Полный текст | Google Scholar
млн лет назад, К. (2011). Характеристики сверхэкспрессии генов переносчиков нитратов OsNRT1.2 и OsNRT1.5 в рисе. Нанкин: магистерская диссертация Nanjing Agric. ун-т
Google Scholar
Martinoia, E., Heck, U., Wiemken, A. (1981). Вакуоли как хранилища нитратов в листьях ячменя. Природа 289, 292–294. doi: 10.1038/289292a0
CrossRef Полный текст | Google Scholar
Martinoia, E., Массонно, А., Франгн, Н. (2000). Транспортные процессы растворенных веществ через вакуолярную мембрану высших растений. Физиология клеток растений. 41, 1175–1186. doi: 10.1093/pcp/pcd059
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Миллер А. Дж., Фан X., Орсел М., Смит С. Дж., Велл Д. М. (2007). Нитратный транспорт и сигнализация. Дж. Экспл. Бот. 58, 2297–2306. doi: 10.1093/jxb/erm066
Дж., Фан X., Орсел М., Смит С. Дж., Велл Д. М. (2007). Нитратный транспорт и сигнализация. Дж. Экспл. Бот. 58, 2297–2306. doi: 10.1093/jxb/erm066
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Моначелло, Д., Allot, M., Oliva, S., Krapp, A., Daniel-Vedele, F., Barbier-Brygoo, H., et al. (2009). Два переносчика анионов AtClCa и AtClCe выполняют взаимосвязанные, но не дублирующие роли в путях ассимиляции нитратов. Новый Фитол. 183, 88–94. doi: 10.1111/j.1469-8137.2009.02837.x
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Пэн С., Буреш Р. Дж., Хуанг Дж., Хуанг Дж., Чжун С., Цзоу Ю. и др. (2010). Улучшение азотных удобрений риса за счет управления азотом на конкретном участке. Агро. Поддерживать. Дев. 30, 649–656. doi: 10.1051/agro/2010002
CrossRef Полный текст | Google Scholar
Qu, YN, Yu, BJ (2008). Влияние блокаторов хлорных каналов на содержание ионов и другие физиологические показатели проростков глициновой сои и глицинемакса при стрессе NaCl. Дж. Нанкин Агрик. ун-т 31, 17–21. doi: 10.3321/j.issn:1000-2030.2008.02.004
Дж. Нанкин Агрик. ун-т 31, 17–21. doi: 10.3321/j.issn:1000-2030.2008.02.004
Полный текст CrossRef | Google Scholar
Qu, YN, Zhou, Q., Yu, BJ (2009).Влияние Zn 2+ и нуфлумовой кислоты на фотосинтез проростков Glycine soja и Glycine max в условиях стресса NaCl. Окружающая среда. Эксп. Бот. 65, 304–309. doi: 10.1016/j.envexpbot.2008.11.005
CrossRef Полный текст | Google Scholar
Quijano, L., Yusà, V., Font, G., McAllister, C., Torres, C., Pardo, O. (2017). Программа оценки риска и мониторинга содержания нитратов в овощах в регионе Валенсия (Испания). Пищевая хим. Токсикол. 100, 42–49.doi: 10.1016/j.fct.2016.12.010
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Салехзаде Х., Малеки А., Резаи Р., Шахморади Б., Поннет К. (2020). Содержание нитратов в свежих и вареных овощах и связанные с ними риски для здоровья. PLoS One 15, e0227551. doi: 10.1371/journal.pone.0227551
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Шредер Дж. Л., Делхайз Э., Фроммер В. Б., Герино М. Л., Харрисон М. Дж., Herrera-Estrella, L., et al. (2013). Использование мембранных транспортеров для улучшения урожая для устойчивого производства продуктов питания. Природа 497, 60–66. doi: 10.1038/nature11909
Л., Делхайз Э., Фроммер В. Б., Герино М. Л., Харрисон М. Дж., Herrera-Estrella, L., et al. (2013). Использование мембранных транспортеров для улучшения урожая для устойчивого производства продуктов питания. Природа 497, 60–66. doi: 10.1038/nature11909
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Shen, QR, Tang, L., Xu, YC (2003). Обзор поведения нитратов в вакуолях растений. Акта Педол. Грех. 40, 465–470. doi: 10.3321/j.issn:0564-3929.2003.03.022
Полный текст CrossRef | Google Scholar
Танг Ю., Sun, X., Hu, C., Tan, Q., Zhao, X. (2013). Генотипические различия в поглощении, транслокации и ассимиляции нитратов у двух сортов пекинской капусты [ Brassica campestris L. ssp. Chinesnsis (L.)]. Завод физиол. Биохим. 70, 14–20. doi: 10.1016/j.plaphy.2013.04.027
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Taochy, C., Gaillard, I., Ipotesi, E., Oomen, R.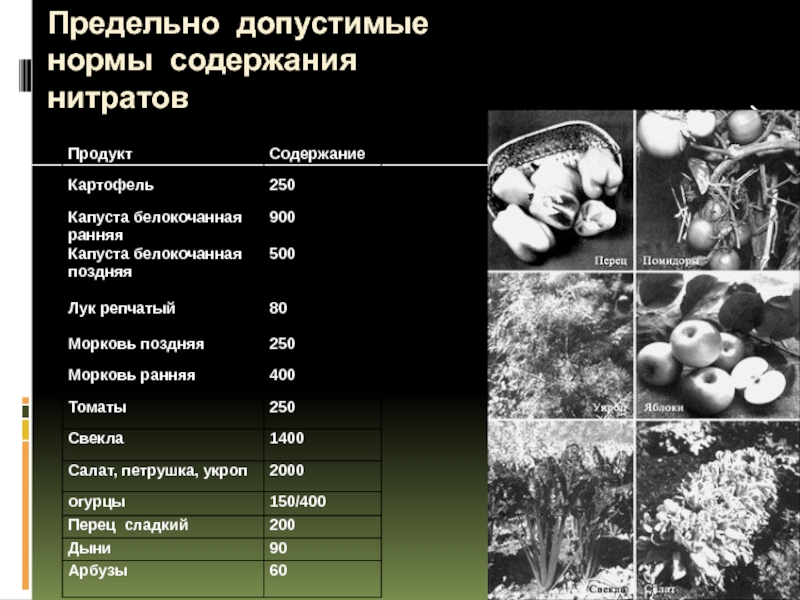 , Leonhardt, N., Zimmermann, S., et al. (2015). Транспортер корневой стелы Arabidopsis NPF2.3 способствует транслокации нитратов к побегам в условиях солевого стресса. Завод J. 83, 466–479. doi: 10.1111/tpj.12901
, Leonhardt, N., Zimmermann, S., et al. (2015). Транспортер корневой стелы Arabidopsis NPF2.3 способствует транслокации нитратов к побегам в условиях солевого стресса. Завод J. 83, 466–479. doi: 10.1111/tpj.12901
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
фон дер Фехт-Бартенбах Дж., Богнер М., Дыновски М., Людевиг У. (2010). CLC-b-опосредованный обмен NO 3 — /H + в тонопласте вакуолей Arabidopsis . Физиология клеток растений. 51, 960–968. doi: 10.1093/pcp/pcq062
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Ван Ю.Ю., Ченг, Ю. Х., Чен, К. Э., Цай, Ю. Ф. (2018). Транспорт нитратов, передача сигналов и эффективность использования. год. Преподобный завод биол. 69, 85–122. doi: 10.1146/annurev-arplant-042817-040056
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Уайт, П.Дж., Бродли, М.Р. (2001). Хлор в почвах, его поглощение и перемещение внутри растения: обзор. Энн. Бот. 88, 967–988. doi: 10.1006/anbo.2001.1540
Хлор в почвах, его поглощение и перемещение внутри растения: обзор. Энн. Бот. 88, 967–988. doi: 10.1006/anbo.2001.1540
CrossRef Полный текст | Google Scholar
Уильямс, К., Персиваль Ф., Мерино Дж., Муни Х.А. (1987). Оценка стоимости конструкции ткани по теплоте сгорания и содержанию органического азота. Окружающая среда растительных клеток. 10, 725–734. doi: 10.1111/1365-3040.ep11604754
CrossRef Full Text | Google Scholar
Сюань, Х.М., Ван, Ю.Х., Вэй, Л.Т. (2014). Анализ транскрипции генов, кодирующих переносчики нитратов семейств NRT1 и NRT2, в ответ на азотное голодание в листьях проростков пшеницы. J. Triticeae Crops 34, 1019–1028.doi: 10.7606/j.issn.1009-1041.2014.08.01
CrossRef Full Text | Google Scholar
Ю, Б. Дж., Лю, Ю. Л. (2004). Хлор, хлоридный канал и толерантность к хлоридам в растениях. Подбородок. Бык. Бот. 21, 402–410. doi: 10.3969/j.issn.1674-3466.2004.04.003
Полный текст CrossRef | Google Scholar
Zhang, G. B., Yi, HY, Gong, JM (2014). Сигнальный модуль Arabidopsis этилен/жасмоновая кислота-NRT координирует перераспределение нитратов и компромисс между ростом и адаптацией к окружающей среде. Растительная клетка 26, 3984–3998. doi: 10.1105/tpc.114.129296
B., Yi, HY, Gong, JM (2014). Сигнальный модуль Arabidopsis этилен/жасмоновая кислота-NRT координирует перераспределение нитратов и компромисс между ростом и адаптацией к окружающей среде. Растительная клетка 26, 3984–3998. doi: 10.1105/tpc.114.129296
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Zhang, ZH, Song, HX, Liu, Q. (2014). Характер распределения абсорбционного азота в масличном рапсе ( Brassica napus L.) на разных стадиях роста. J. Питательные вещества для растений. 37, 1648–1660. doi: 10.1080/017.2014.888747
CrossRef Полный текст | Google Scholar
Чжан, З. Х. (2017). Взаимосвязь между транспортом нитратов и их использованием культурой и эффективностью использования азота. J. Питательные вещества для растений. 23, 217–223. doi: 10.11674/zwyf.15357
CrossRef Full Text | Google Scholar
Чжао, Л. Х., Лю, Ю. Л. (1999). Тонопласт Н + -пирофосфатаза и ее реакция на стрессы. Завод физиол. J. 35, 441–445. doi: 10.13592/j.cnki.ppj.1999.06.001
Завод физиол. J. 35, 441–445. doi: 10.13592/j.cnki.ppj.1999.06.001
CrossRef Full Text | Google Scholar
Чжао, С.П., Чжан, Р.Л., Сюй, М.Ф., Чжэн, Дж. К. (2011). Влияние различных соотношений NH 4 + /NO 3 — на накопление нитратов у разных генотипов китайской капусты. Почвы 43, 32–38. doi: 10.13758/j.cnki.tr.2011.01.024
CrossRef Полный текст | Google Scholar
Чжао Л., Лю Ф., Кроуфорд Н. М., Ван Ю. (2018). Молекулярная регуляция реакции растений на нитраты. Междунар. Дж. Мол. науч. 19, 2039. doi: 10.3390/ijms139
CrossRef Full Text | Google Scholar
Вносимый в корни глицинбетаин снижает накопление нитратов и улучшает качество салата, выращенного на гидропонике
https://doi.org/10.1016/j.foodchem.2021.130558Получить права и содержаниеОсновные моменты
- •
Нитраты в листьях салата часто связаны с вредным воздействием на здоровье человека.
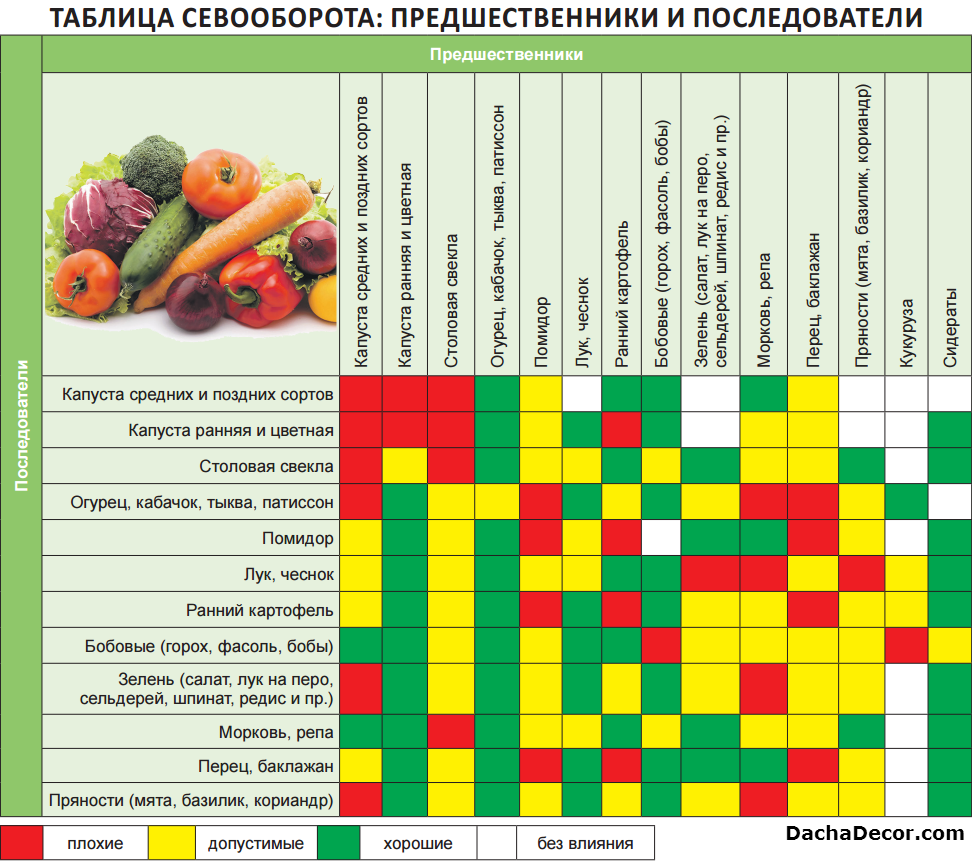
- •
Глицинбетаин (GB) в растворе для фертигации поглощался и перемещался в листьях.
- •
Содержание нитратов в салате снижалось с помощью GB в зависимости от концентрации.
- •
RU Добавка для гидропоники увеличивает содержание сухого вещества в листьях салата.
- •
GB обогащение повысило пищевую и питательную ценность салата.
Abstract
Листовые овощи, такие как салат ( Lactuca sativa L.), естественно, имеют высокое содержание нитратов, и Европейская комиссия установила максимальный уровень содержания нитратов в салате. Глицинбетаин является органическим осмолитом, облегчающим стресс растений, но его роль в накоплении нитратов в листьях остается неизвестной. Было исследовано поглощение глицинебетаина корнями салата и его способность регулировать содержание нитратов в салате и улучшать качество растений.Были проведены два гидропонных эксперимента с салатом с разными дозами внесения глицинебетаина (Exp1: 0, 1, 7,5 и 15 мМ; Exp2: 0, 1 + 1 + 1, 1 + 10 и 4 мМ). Растения анализировали в разные моменты времени. Применение корней привело к поглощению глицинбетаина и его перемещению в листья. Концентрации глицинбетаина > 7,5 мМ снижали содержание нитратов в листьях до 40 % и повышали содержание сухого вещества в листьях. Глицинбетаин положительно влияет на минеральный и аминокислотный состав листьев. Таким образом, глицинбетаин может стать новой стратегией снижения содержания нитратов в гидропонном салате.
Растения анализировали в разные моменты времени. Применение корней привело к поглощению глицинбетаина и его перемещению в листья. Концентрации глицинбетаина > 7,5 мМ снижали содержание нитратов в листьях до 40 % и повышали содержание сухого вещества в листьях. Глицинбетаин положительно влияет на минеральный и аминокислотный состав листьев. Таким образом, глицинбетаин может стать новой стратегией снижения содержания нитратов в гидропонном салате.
Ключевые слова
Аминокислота
Рост
Lactuca sativa
Минералы
Технология питательных пленок
Опубликовано Elsevier Ltd.
Рекомендованные статьи
Ссылки на статьи
Культуры, такие как овсяное сено, сорго, кукуруза, суданская трава, джонсинская трава, свекла, асковидные сорняки марь, русский чертополох и паслен являются примерами растений, накапливающих нитраты.Есть много других. Растения, содержащие более 1,5% нитратов (в виде KNO3) в сухом виде, могут быть смертельными для домашнего скота. Растения различаются по способности накапливать нитраты. Тип почвы, доступность и форма азота, присутствующего в почве, различные факторы окружающей среды и химические или физические повреждения растений влияют на количество нитратов во многих из этих растений.Например, засуха, заморозки или обработка растений, накапливающих нитраты, 2,4-D могут вызвать чрезмерное накопление нитратов растениями. Нитрат накапливается преимущественно в вегетативной ткани растений, в то время как семена остаются в сохранности. Где и когда происходит отравление нитратами Как это влияет на домашний скот Количество растительного материала, необходимого для отравления животного, зависит от количества нитратов в растении и, в меньшей степени, от скорости поедания растения. На токсичность влияют многие факторы, но в целом около 0,05% нитратов от веса животного является минимальной смертельной дозой.Отравление происходит в основном у жвачных животных. Знаки и поражения отравления
Как Сокращение потерь |
Отравление нитратами | Сельское хозяйство Манитобы
Токсичные уровни нитратов в кормах всегда возможны, когда нормальный рост растений нарушается из-за града, засухи, снегопада или заморозков.Процент животных, пострадавших от острого отравления нитратами в Манитобе, как правило, невелик. Однако когда смертельные потери все же случаются, они происходят внезапно и могут быть разрушительными. Высокий уровень нитратов не должен быть проблемой, если программа кормления осуществляется правильно.
Что такое нитраты?
При благоприятных условиях растения поглощают азот в основном в виде нитратов. Нитрат быстро превращается в аммиак, который включается в растительный белок.
Нитрат быстро превращается в аммиак, который включается в растительный белок.
Неблагоприятные условия выращивания могут препятствовать использованию нитратов и вызывать их накопление в растении.
В нормальных условиях крупный рогатый скот преобразует нитраты корма в нитриты. Затем он превращается в аммиак и используется микробами рубца для производства белка. Проблема возникает, когда нитраты превращаются в нитриты быстрее, чем нитриты превращаются в аммиак.
Когда это происходит, нитрит накапливается и всасывается в кровоток, где он связывается с гемоглобином, снижая тем самым способность крови переносить кислород. Животные могут погибнуть от удушья.
Факторы, влияющие на накопление нитратов
Тип корма
В одних растениях нитраты накапливаются больше, чем в других.Зерновые культуры и сорняки более склонны накапливать нитраты, чем бобовые и травы. Хотя это и известно, очень небольшой процент сена из бобовых и злаков будет содержать заметное количество нитратов.
Уровень оплодотворения
Высокий уровень нитратов в почве в результате внесения азотных удобрений, внесения навоза, вспахивания бобовых или летнего пара может привести к высокому уровню нитратов в кормах. Например, было обнаружено, что марь редкорная из свинарника содержит более 3% нитратов, что в семь раз больше, чем содержание того же сорняка, собранного на соседнем поле.
Стадия развития корма
Ранние фуражные корма (стадия от начала доения) обычно содержат более высокие уровни нитратов, чем те же фуражные корма, когда они почти созрели (стадия теста).
Интенсивность света и температура
Плохая интенсивность света (тень) и высокие температуры приводят к высокому уровню нитратов в растениях. Нитраты накапливаются ночью и быстро рассеиваются в яркие солнечные дни при умеренных температурах.
Посевы, поврежденные заморозками
Уровень нитратов будет самым высоким непосредственно перед восходом солнца.Если наступают ранние заморозки, то обычно это происходит незадолго до восхода солнца, когда содержание нитратов в растении достигает своего пика. Любые уцелевшие листья, вероятно, будут затенены поврежденными морозом листьями выше, поэтому потенциал снижения содержания нитратов ограничен.
Любые уцелевшие листья, вероятно, будут затенены поврежденными морозом листьями выше, поэтому потенциал снижения содержания нитратов ограничен.
Посевы, поврежденные градом
Сразу после града можно ожидать, что содержание нитратов будет довольно низким, поскольку град обычно возникает после жаркого, яркого, солнечного дня. Однако затем нитраты могут накапливаться в течение ночи и оставаться на высоком уровне, поскольку потеря листьев снижает вероятность превращения нитратов в белок.Степень потери листьев определяет степень снижения уровня нитратов.
Засуха
Если условия улучшатся и растение начнет активно расти, часть накопленных нитратов может быть израсходована за несколько дней. Обычно это происходит только на верхних листьях, которые подвергаются воздействию солнечного света. Нижние листья, которые затемнены, могут содержать высокий уровень нитратов.
Уменьшится ли количество нитратов после сбора урожая?
Если сено в валке остается влажным в течение нескольких дней или попадает под дождь, уровень нитратов снизится. Быстро высушенное сено потеряет очень мало нитратов. Концентрация нитратов в тюках сена со временем заметно не меняется.
Быстро высушенное сено потеряет очень мало нитратов. Концентрация нитратов в тюках сена со временем заметно не меняется.
Силосование приводит к снижению уровня нитратов на 40-60%.
Как проверить корм на нитраты
Нитраты в кормах можно обнаружить только химическим анализом. Если вы подозреваете наличие проблемы, отнесите репрезентативную пробу корма местному представителю сельского хозяйства для выборочной проверки. Это определит наличие нитратов. Лаборатории по тестированию кормов могут определить фактический уровень нитратов.
Кормление кормами с высоким содержанием нитратов
Животные не должны потреблять корм, содержащий более 0,5% нитрата (0,8% нитрата калия). Корма с высоким содержанием нитратов следует физически смешивать с кормами с низким содержанием нитратов, поэтому
общий уровень нитратов составляет менее 0,5%. Выкладывание одного тюка корма с высоким содержанием нитратов вместе с одним или несколькими тюками корма с низким содержанием нитратов недопустимо. Кормление с адекватным уровнем энергии и витамина А снижает риск токсичности. Переходите на сомнительный корм в течение 1-2 недель и не переводите скот на корма с высоким содержанием нитратов и обратно.
Симптомы отравления
Симптомы смертельного отравления нитратами включают затрудненное дыхание, пену изо рта, учащенный пульс, слабость, диарею, частое мочеиспускание, нарушение координации и судороги. Смерть может наступить через три-четыре часа. Вскрытие показало темную кровь шоколадного цвета. Метиленовым синим лечат отравления нитратами.
Сублетальные дозы могут привести к потере аппетита, снижению молочной продуктивности, замедлению роста и аборту.
Подготовлено сельским хозяйством Манитобы.
Потенциальная опасность отравления нитратами и отравления силосным газом
Потенциальная опасность нитратов Отравление и отравление силосным газом
Что такое нитраты?
Нитраты встречаются в природе во многих растениях, но их можно найти в более высоких концентрациях в кукурузе и некоторых сорняках, таких как баранина и марь.Нитраты накапливаются в растениях кукурузы при большое количество почвенных нитратов и недостаток влаги, что мешает при нормальном росте растений. Накопление нитратов часто бывает максимальным. после дождя, завершившего длительный засушливый период.
Какие уровни считаются опасными?
Концентрация нитратов, измеренная в частях на миллион (ppm) должно быть менее 1000 ppm для скармливания мясному скоту без риска.Уровни выше 4000 частей на миллион не должны подаваться. Корм с нитратов между этими двумя уровнями связано с относительным риском от количества корма и вида скота. Требуется тщательное управление.
Как узнать, в порядке ли моя кукуруза?
Уровни нитратов могут колебаться ежедневно в пределах завода, с концентрацией выше в нижней части растения по сравнению с теми, которые находятся вблизи верхняя.Растения кукурузы обычно содержат значительно более высокие уровни нитратов сразу после дождя, который следует за продолжительным период засушливой погоды. Риск отравления нитратами на зеленом измельчение или выпас этой кукурузы намного выше в течение 5-7 дней после дождя, чем в реальный период засушливой погоды.
Тестирование при сборе урожая даст общее представление об относительном уровень нитратов, но не концентрация нитратов в силосе кормят.Лучшее время для проверки концентрации нитратов – после ферментация завершена. Получите репрезентативную выборку. Держать образцы охлаждают и отправляют в лабораторию как можно быстрее. Если сообщается о высоких уровнях, вода и другие корма также должны быть проверено.
Что такое силосный газ?
Повышенный нитратный потенциал увеличивает риск силосного газа. Двуокись азота, NO2, является опасным химическим удушающим средством и производится практически сразу после помещения растительного материала в силос.Даже кратковременное воздействие на человека может привести к серьезным травмам. легочной ткани и внезапная смерть. Имеет характерный отбеливатель запах и может быть виден в виде красновато-коричневого дымка. Это тяжелее чем воздух, поэтому он будет располагаться чуть выше силоса поверхность. Он также может стекать по силосным желобам и в кормовые помещения. Соблюдайте меры предосторожности и процедуры по работе с бункерным газом, изложенные в информационном бюллетене OMAFRA . Опасные газы на Сельскохозяйственные операции, приказ №14-017. Обратитесь в Онтарио Информационный бюллетень Ассоциации безопасности ферм Опасности силосного газа.
Для получения дополнительной информации об отравлении нитратами и других неблагоприятных погодных условиях. связанные темы, проконсультируйтесь с OMAFRA на странице неблагоприятной погоды или позвоните в Сельскохозяйственную информацию Контактный центр: 1-877-424-1300.
Влияние сульфат-анионов на накопление нитратов и общее содержание азота Кьельдаля в растениях салата, выращиваемых на торфо-перлитовой смеси
АвторыГл.Карипидис, Д. Дума, П. Ифанти, К. Зисис, Г. Патакиутас
АбстрактныйИнтенсивное земледелие характеризуется повышенным использованием синтетических азотных удобрений. При избыточном внесении азотных удобрений многие овощи, особенно листовые, накапливают большое количество нитратов. Повышенное содержание нитратов в овощах связано с возможными последствиями для здоровья, поскольку метаболиты нитратов могут вызывать канцерогенез, детскую метгемоглобинемию и, возможно, даже тератогенез.Целью настоящего исследования было изучение влияния сульфат-ионов на накопление нитратов и общее содержание азота Кьельдаля (TKN) в листьях салата ( Lactuca sativa var. crispa ‘Lollo Bionda’) в качестве попытки предложить возможные способы для снижения уровня нитратов. Растения выращивали на торфо-перлитовой смеси и удобряли питательными растворами в тепличных условиях. Три уровня концентрации азота (100, 200 и 400 мг л ‑1 N) применялись в сочетании с тремя уровнями сульфат-анионов (15, 150 и 300 мг л ‑1 S в виде SO 4 2 — ).На стадии уборки определяли сырую массу листьев, накопление нитратов, концентрацию общей серы и содержание тканей ТКН. Как и ожидалось, лиственная биомасса, накопление нитратов и содержание ТКН увеличивались при повышении концентрации азота. Однако повышенный уровень сульфатов (150 и 300 мг л ‑1 S) не влиял на массу растений, тогда как при увеличении количества сульфатных удобрений наблюдалось снижение накопления нитратов. Более того, концентрация 150 мг л ‑1 S вызывала увеличение ТКН, тогда как концентрация 300 мг л ‑1 S вызывала обратный эффект.Результаты настоящего исследования показывают, что повышенные концентрации сульфатов привели к снижению накопления нитратов в листьях салата. Это может быть связано с вмешательством в поглощение нитратов ионами сульфатов и может быть предложено в качестве возможного способа снижения содержания нитратов в салате, что обеспечивает безопасность потребителей.
Механизм накопления нитратов у пакхои [Brassica campestris L.ssp. Chinensis (L.)] на JSTOR
АбстрактныйУменьшение содержания нитратов в овощах может повысить эффективность использования азота растениями и снизить риск для здоровья человека, вызванный преобразованием нитратов в нитриты в овощах.В данной работе изучались механизмы различий в накоплении и распределении нитратов в органах двух сортов пакхои (Brassica campestris L.ssp. Chinensis (L.), ранее скринированных в гидропонных экспериментах, из 12 сортов, широко выращиваемых в настоящее время в Китае. Два типичных сорта В этом эксперименте использовались сорта Shanghaiqing с низким накоплением нитратов и Liangbaiye 1 с высоким накоплением нитратов.Не было существенной разницы в общем поглощении нитратов, но между двумя сортами существовала значительная разница в содержании нитратов.По сравнению с Liangbaiye 1, Shanghaiqing показал значительно более высокую скорость фотосинтеза и активность нитратредуктазы. Определение концентрации (активности) нитратов в вакуолях с помощью двуствольных нитрат-селективных микроэлектродов показало, что Shanghaiqing имеет более низкую вакуолярную нитратную активность, чем Liangbaiye 1. Два предполагаемых гена нитратредуктазы, nia1 и nia2, были амплифицированы из листовых пластинок этих двух сортов. Фрагменты мРНК Nia 1 (887 п.н., регистрационные номера DQ082868 и DQ082869) амплифицировали с использованием вырожденного праймера, а фрагмент мРНК nia2 амплифицировали с использованием одной пары генерирующих праймеров, разработанных в соответствии с DQ001901.Анализ последовательностей DQ082868 и DQ082869 показал 97% и 87% сходства с двумя последовательностями мРНК нитратредуктазы Brassica napus, регистрационные номера D38219 и D38220 соответственно. Результаты ПЦР в реальном времени для сравнения относительной экспрессии предполагаемых генов нитратредуктазы (nia1 и nia2) показали, что Shanghaiqing имел значительно более высокий уровень экспрессии, чем Liangbaiye 1, а nia2 был значительно выше, чем nia1, в листовой пластинке и черешке. Как активность нитратредуктазы, так и относительный уровень экспрессии nia1 находились в порядке листовая пластинка > корень > черешок, тогда как у nia2 листовая пластинка > черешок > корень.Не было статистически значимой разницы в активности нитратов, хранящихся в вакуолях, между различными органами двух сортов. Можно сделать вывод, что Shanghaiqing поглощал немного меньше нитратов, но имел значительно более высокую активность нитратредуктазы в цитозоле и имел более высокую относительную экспрессию предполагаемых генов нитратредуктазы, чем Liangbaiye 1; это приводит к тому, что Shanghaiqing имеет более низкое содержание нитратов, чем Liangbaiye 1.
Информация о журналеPlant and Soil публикует оригинальные статьи и обзорные статьи, исследующие взаимодействие биологии растений и наук о почве и предлагающие четкий механистический компонент.Сюда входят как фундаментальные, так и прикладные аспекты минерального питания, отношений растений и воды, симбиотических и патогенных взаимодействий растений и микробов, анатомии и морфологии корней, биологии почв, экологии, агрохимии и агрофизики. Статьи, посвященные основным молекулярным или математическим компонентам, также входят в сферу охвата журнала.
Информация об издателеSpringer — одно из ведущих международных научных издательств, выпускающее более 1200 журналов и более 3000 новых книг ежегодно, охватывающих широкий круг предметов, включая биомедицину и науки о жизни, клиническую медицину, физика, инженерия, математика, информатика и экономика.
.
 Сублетальные эффекты могут возникнуть у домашнего скота при употреблении корма, содержащего от 0,5 до 1,5% нитратов. Отравление нитратами может возникнуть и у животных, употребляющих в пищу нитратные удобрения, машинное масло и некоторые природные воды из колодцев и прудов.
Сублетальные эффекты могут возникнуть у домашнего скота при употреблении корма, содержащего от 0,5 до 1,5% нитратов. Отравление нитратами может возникнуть и у животных, употребляющих в пищу нитратные удобрения, машинное масло и некоторые природные воды из колодцев и прудов. Собранные и хранящиеся корма продолжают быть токсичными.
Собранные и хранящиеся корма продолжают быть токсичными. Корма с высоким содержанием нитратов следует разбавлять кормами с низким содержанием нитратов, чтобы уменьшить потребление нитратов, или, если есть признаки токсичности нитратов, кормление кормами, накапливающими нитраты, следует прекратить. Признаки дефицита витамина А были связаны с кормлением низким уровнем нитратов, что позволяет предположить, что витаминные добавки могут быть полезными.
Корма с высоким содержанием нитратов следует разбавлять кормами с низким содержанием нитратов, чтобы уменьшить потребление нитратов, или, если есть признаки токсичности нитратов, кормление кормами, накапливающими нитраты, следует прекратить. Признаки дефицита витамина А были связаны с кормлением низким уровнем нитратов, что позволяет предположить, что витаминные добавки могут быть полезными.