фото и видео, условия и оборудование камер для разведения вешенок
Способов выращивания грибов вешенок несколько: самый приемлемый из них – на пнях на дачном участке. Воспользовавшись таким методом разведения вешенок, вы сможете обеспечить вкусными грибами свою семью. Но если вы подумываете над тем, как выращивать вешенки для продажи, придется обзавестись теплицей или специальным помещением. Ну а для начала, конечно, изучить технологию процесса.
Технология выращивания вешенок экстенсивным способом: разведение на пнях
Для выращивания вешенок на пнях чурбаны, зараженные грибами, можно живописно установить или вкопать на садовом участке. Первые плоды на толстых бревнах можно ожидать не ранее чем через год. Толщина чурбанов для разведения вешенок на пнях должна быть не меньше 10 см, а длина от 40 см. На отрезках толстых бревен плодоношение продолжается 5-7 лет.
Перед тем как выращивать грибы вешенки, нужно заготовить чурбаны.
При подготовке к выращиванию вешенок экстенсивным способом в пнях сверлят отверстия по кругу. Если пень спилен у самой земли, сверлят отверстия с торца наискосок, начиная сверление недалеко от коры. Грибница распространяется быстро вдоль древесных волокон, а в других направлениях — медленно.
Другой вариант технологии выращивания вешенок на пнях — сразу вкопать чурбан в землю. Грибы на вкопанных бревнах лучше переносят периоды без дождей. Выбирают место, с трех сторон затененное растениями и открытое с запада или востока. Лучше выбрать место в овражке, низине, где влажность земли и воздуха выше. При необходимости сажают дополнительные растения, которые обеспечат защиту от ветра.
Из всех вешенок, которые растут в России в лиственных лесах на широте южнее Москвы, самая вкусная — вешенка обыкновенная. Природные формы этого гриба требуют холодового шока для плодоношения.
Для украшения сада при выращивании грибов вешенок на пнях можно поселить на чурбанах или пнях экзотические сорта: лимонно-желтую (Pleurotus citrinopileatus) и розовую (Pleurotus djamor). Они очень красивы, но менее вкусны.
Как подготовить грибные блоки для выращивания вешенок на даче на пнях
Для приготовления одного субстратного блока для выращивания вешенок объемом 6 л возьмите 6 л щепы из перемолотых свежих веток или сушеной щепы. Вместо щепы можно взять 6-7 л измельченной соломы или лузги от семян подсолнечника. Добавьте 200 г ячменя, овса или перловой крупы. Водой доведите массу субстрата до 3000 г. Добавьте в субстрат чайную ложку гашеной извести — Са(ОН)г.
Добавьте 200 г ячменя, овса или перловой крупы. Водой доведите массу субстрата до 3000 г. Добавьте в субстрат чайную ложку гашеной извести — Са(ОН)г.Для изготовления маленьких блоков объемом 3 л при выращивании вешенок на даче надо уменьшить количество всех ингредиентов в 2 раза.
Перед тем как выращивать вешенки из грибных блоков массой 10-20 кг, после тщательного перемешивания набейте субстрат в полипропиленовые пакеты объемом 8 л или 4 литра. Затем вставьте в горло пакета и обвяжите бечевкой изготовленные из ваты или из чистого синтепона пробки диаметром 2-3 см.
Стерилизуйте или пастеризуйте субстрат прямо в пакете одним из способов. Затем, убедившись, что субстрат остыл до температуры ниже +30 °С, насыпьте в горлышко пакета от 50 до 100 г зернового мицелия вешенки. Разместите пакеты вертикально пробкой вверх в помещении с температурой от +16 °С до +26 °С для инкубации мицелия в субстрате. Спустя 3-4 недели субстрат зарастет мицелием и станет белым. Время зарастания зависит от температуры: при +24 ?С оно минимально, а при +16 °С оно может существенно увеличиться.
Можно подготовить субстрат для вешенок более экономным, так называемым «китайским» способом. Для блока массой 1,5 кг возьмите 3 л основы субстрата, добавьте 100 г зерна или крупы. Водой доведите массу субстрата до 1500 г. Добавьте в субстрат чайную ложку гашеной извести -Са(ОН)2. Набейте субстрат в полипропиленовый мешок объемом 4 л. Стерилизуйте или пастеризуйте субстрат прямо в незакрытом пакете одним из способов. После охлаждения субстрата ниже +30 °С завяжите пакет бечевкой совершенно герметично. На чистом столе чистыми руками разомните зерновой мицелий.
Сделайте стамеской или ножом 6 вертикальных равноотстоящих друг от друга прорезей размером 4 см в боковой поверхности мешка с субстратом. Вложите в каждую прорезь по 1 чайной ложке зернового мицелия. Заклейте герметично прорези в мешке скотчем. Для инкубации мицелия в субстрате разместите пакеты вертикально при комнатной температуре 16-26 °С. Спустя 4-7 дней убедитесь, что мицелий образовал белые пятна зарастания вокруг заклеенных прорезей. После этого сделайте крестовые прорези в скотче размером 2 х 2 см, на том же месте, где они были, и поставьте мешки обратно в комнату инкубации. Спустя 20-40 дней, в зависимости от количества внесенного мицелия и от температуры воздуха, субстратный блок для грибов вешенок станет белым и будет готов к плодоношению.
Как выращивать вешенки из грибных блоков и видео выгонки
Перед тем как выращивать вешенки, пакеты поставьте на полки или на землю в саду вертикально. Плодовые тела грибов будут плодоносить из надрезов в боковой поверхности. Оптимальная температура воздуха в этот период +13…+17 °С, влажность воздуха 70-90%. Такие условия в природе бывают только осенью или дождливым летом. Особенно мало влаги содержится в воздухе зимой в помещении с отоплением. Для увеличения влажности воздуха грибные блоки для выращивания вешенок нельзя просто накрыть пакетом: из-за высокой концентрации углекислого газа под пакетом вырастет гриб неправильной формы. Можно сделать из полиэтилена небольшую культивационную камеру с вентиляцией. Имеющиеся в продаже ультразвуковые увлажнители воздуха («холодный пар») могут подавать своим вентилятором свежий влажный воздух в камеру плодоношения. Надо приобрести также электротаймер, который будет включать увлажнитель на 5 мин каждый час. При наличии такого увлажнителя в осенне-зимний период можно вырастить хорошую вешенку на застекленной лоджии.
Можно сделать из полиэтилена небольшую культивационную камеру с вентиляцией. Имеющиеся в продаже ультразвуковые увлажнители воздуха («холодный пар») могут подавать своим вентилятором свежий влажный воздух в камеру плодоношения. Надо приобрести также электротаймер, который будет включать увлажнитель на 5 мин каждый час. При наличии такого увлажнителя в осенне-зимний период можно вырастить хорошую вешенку на застекленной лоджии.
Летом при повышенной температуре появление зачатков плодовых тел при разведении грибов вешенок экстенсивным способом может задержаться. В этом случае надо устроить для мицелия «холодный шок». Поместить пакет с мицелием на 3 дня в холодильник или в погреб с температурой от 0 до +10 °С, а потом вернуть субстратные блоки на место их будущего плодоношения. Скорее всего, там быстро появятся многочисленные зачатки плодовых тел внутри перфорированного пакета. Теперь главное условие выращивания вешенок — высокая влажность воздуха при низкой концентрации углекислого газа. Такой микроклимат бывает среди густой растительности в тени. Для плодоношения вешенки надо выбрать место, защищенное от ветра и от прямых солнечных лучей. Для увеличения влажности воздуха можно поливать окружающие растения и почву. А после появления плодовых тел нужен полив по грибам.
Такой микроклимат бывает среди густой растительности в тени. Для плодоношения вешенки надо выбрать место, защищенное от ветра и от прямых солнечных лучей. Для увеличения влажности воздуха можно поливать окружающие растения и почву. А после появления плодовых тел нужен полив по грибам.
В саду можно поместить мицелий в затененную с южной стороны теплицу и увлажнять воздух регулярными поливами. Если в теплице есть зеленые растения, а субстратных блоков с вешенкой немного, будут расти высококачественные грибы. При большом количестве блоков выделяется много углекислого газа, и грибы будут некрасивыми, вялыми, с вытянутой ножкой. Для создания нужных условий выращивания грибов вешенок нужно удалять из помещения углекислый газ, я для этого регулярно проветривать помещение или установить вентиляционную систему.
Собирайте урожай по мере их появления, пока еще края шляпки загнуты вниз, не распрямились полностью. Грибы аккуратно выламывайте из прорезей субстратного блока, раскачивая их вниз и вверх.
Посмотрите видео «Условия выращивания вешенок и выгонка грибных блоков», чтобы лучше понять технологию процесса:
Как выращивать грибы вешенки из блоков по нестерильной технологии
Вешенка обладает набором активных ферментов, который позволяет ей захватить субстрат в пакете и создать там высокую концентрацию углекислого газа до того, как там появятся плесени и анаэробные бактерии. Нестерильную технологию можно реализовать, если субстрат не сильно заражен плесенью. Таким субстратом могут быть перемолотые свежие ветки ивы или березы.
Технология выращивания вешенки нестерильным способом довольно проста. Поместите в таз 6 л щепы из свежих, перемолотых в садовом измельчителе веток ивы. Разбросайте по щепе гашеную известь (1 чайная ложка). Используя этот способ выращивания вешенок, измельчите в руках 200 г зернового мицелия и внесите его в щепу при помешивании.
Приготовьте пакет из полиэтилена, рассчитанный на 7 л содержимого. Сделайте для него синтепоновую пробку. Пробки нужны для защиты мицелия от грибных комариков и для того, чтобы вешенка не начала плодоносить раньше, чем вы этого захотите.
Для изготовления синтепоновой пробки достаточно отрезать кусок синтепона и скрутить его в виде цилиндрика диаметром 4 см и длиной 6 см. Для придания пробке из синтепона цилиндрической формы обмотайте его нитками так, как мотают клубок для вязания.
Набейте полученную смесь в полиэтиленовый пакет. Лучше, если высота пакета будет больше его ширины. Опустите пробку так, чтобы пакет был плотно набит субстратом. Горло пакета стяните бечевкой.
Как видно на фото, при выращивании вешенок нужно придать субстратному блоку прямоугольную форму, приклеив скотчем «уши» пакета к его дну, так чтобы он прочно стоял на полке пробкой вверх:
Для инкубации поставьте блок в помещение с температурой +20…+24 °С. Спустя неделю внутри пакета появятся белые звездочки грибницы, которая растет вблизи частиц зернового мицелия. Сначала в верхней части блока, где больше кислорода, а затем в нижней появятся белые пятна. Через 3-4 недели весь субстратный блок станет белым. С этого момента можно считать, что субстратный блок освоен мицелием и что сам субстрат уже превратился в полноценный субстратный мицелий. Его можно использовать для выгонки грибов или для засева новых партий субстрата.
Спустя неделю внутри пакета появятся белые звездочки грибницы, которая растет вблизи частиц зернового мицелия. Сначала в верхней части блока, где больше кислорода, а затем в нижней появятся белые пятна. Через 3-4 недели весь субстратный блок станет белым. С этого момента можно считать, что субстратный блок освоен мицелием и что сам субстрат уже превратился в полноценный субстратный мицелий. Его можно использовать для выгонки грибов или для засева новых партий субстрата.
Для выращивания грибов вешенок из полученных блоков с мицелием надо сделать в боковой стенке пакета шесть вертикальных 3-сантиметровых разрезов ножом и поставить блок в тенистое место сада для плодоношения. Грибы будут расти из этих разрезов.
Можно поступить проще — срезать горло мешочка вместе с пробкой, тогда грибы вырастут сверху. Пакеты поставьте на полки или на землю в саду вертикально. Оптимальные условия для этой стадии культивирования грибов — температура воздуха +13…+17 °С, влажность воздуха 70-90%.
А теперь посмотрите видео «Выращивание вешенок по нестерильной технологии»:
Выгонка мицелия вешенки при выращивании грибов
Мицелий для выращивания вешенок в количестве от 2 до 5% от массы субстрата вносят в субстрат в чистом помещении: насыпают в полиэтиленовые мешки и уплотняют. Оптимальная плотность субстрата 0,4-0,5 кг/л. Можно использовать полиэтиленовые мешки, заранее перфорированные круглыми отверстиями. Оптимальная масса субстратного блока 15 кг. Мешок крепко завязывают сверху шпагатом. Подготовленные субстратные блоки размещают на транспортных тележках и небольшими партиями перевозят к месту инкубации.
При многокамерной системе выращивания вешенки все фазы развития происходят в камерах с регулируемым климатом. Первые 20 суток в камере с оборудованием для выращивания вешенок держат температуру воздуха +24 °С, оптимальную для инкубации мицелия в субстрате, а вентиляцию свежим воздухом выключают. Затем резко понижают температуру воздуха до +15 °С и подают свежий воздух в полном объеме, чтобы инициировать начало плодоношения. Спустя 10 дней собирают грибы первой волны плодоношения, затем регулируют условия, так чтобы ускорить появление второй волны. Для того чтобы грибы вырастали равномерно по дням недели, камер должно быть много.
Затем резко понижают температуру воздуха до +15 °С и подают свежий воздух в полном объеме, чтобы инициировать начало плодоношения. Спустя 10 дней собирают грибы первой волны плодоношения, затем регулируют условия, так чтобы ускорить появление второй волны. Для того чтобы грибы вырастали равномерно по дням недели, камер должно быть много.
Большее распространение получила двухзональная, или двухкамерная система выращивания. Одну треть культивационной площади отводят под камеру инкубации, где мицелий осваивает субстрат. Остальную площадь — под камеру плодоношения, куда подают свежий воздух и где постоянно поддерживается температура +15 °С и относительная влажность воздуха 80%, оптимальные для плодоношения вешенки.
После инокуляции и изготовления субстратных блоков их перемещают в камеру инкубации. Вертикальное размещение блоков обеспечивает лучшую конвекцию воздуха внутри блока, но чаще их располагают горизонтально для экономии места. Для стартового ускорения освоения субстрата мицелием иногда блоки перфорируют стамеской лишь через 2-3 дня после их размещения в камере инкубации. Этот прием позволяет повысить содержание углекислого газа в субстрате в начале инкубации.
Этот прием позволяет повысить содержание углекислого газа в субстрате в начале инкубации.
Оптимальная температура субстрата в центре субстратного блока при инкубации составляет +25…+27 °С. Предельные значения от +16 до +35 °С. Температура воздуха +20…+24 °С.
В зависимости от выбранной технология выращивания грибов вешенок относительная влажность воздуха должна быть 70-95% , концентрация углекислого газа высокая (более 2000 ppm). В фазе инкубации свежий воздух в культивационную камеру не подают. Необходимо такое размещение субстратных блоков, чтобы все они находились в одинаковых условиях и могли свободно отдавать свое биологическое тепло, чтобы избежать перегрева субстрата. При многоярусном размещении блоков для их охлаждения может потребоваться система обдува блоков рециркуляционными воздушными потоками. Свет не требуется, но допустим. После появления зачатков грибов на некоторых блоках с одинаковой датой изготовления всю партию блоков переносят в камеру плодоношения.
Выращивание грибов вешенок в помещении с ламинарным потоком воздуха
При выращивании вешенок в помещении с ламинарным потоком воздуха стеллажи для размещения блоков надо сделать так, чтобы блоки стояли вертикально в один ряд в виде одной сплошной стенки. Расстояние между стенками 1 м. Расстояние между ярусами по высоте составляет 70 см. Для предотвращения выпадения блоков в сторону прохода на уровне середины блоков кладется на крючки съемный арматурный пруток. Вертикальные стойки нужно установить через каждые полтора метра по длине стеллажа. Каждый стеллаж при выращивании грибов вешенок в помещении с ламинарным потоком воздуха крепится не менее чем двумя металлическими дюбелями к полу и двумя к потолку. С одной стороны стеллажа арматурные прутки приваривают к опорам, с другой их кладут на приваренные к опорам крючки. На время размещения субстратных блоков соответствующий пруток снимается и кладется временно на другой ярус.
Расстояние между стенками 1 м. Расстояние между ярусами по высоте составляет 70 см. Для предотвращения выпадения блоков в сторону прохода на уровне середины блоков кладется на крючки съемный арматурный пруток. Вертикальные стойки нужно установить через каждые полтора метра по длине стеллажа. Каждый стеллаж при выращивании грибов вешенок в помещении с ламинарным потоком воздуха крепится не менее чем двумя металлическими дюбелями к полу и двумя к потолку. С одной стороны стеллажа арматурные прутки приваривают к опорам, с другой их кладут на приваренные к опорам крючки. На время размещения субстратных блоков соответствующий пруток снимается и кладется временно на другой ярус.
Для постоянного удаления углекислого газа от сростков вешенки и для активизации испарения воды с поверхности плодовых тел нужно обеспечить движение воздуха вблизи плодовых тел со скоростью не менее 0,05 м/с. При условии высокой относительной влажности воздуха допустима большая скорость обдува грибов (до 5 м/с).
Для получения высококачественных плодовых тел в камеру культивации постоянно должно подаваться не менее 200 м3/ч свежего воздуха в расчете на одну тонну субстрата в камере. Зимой воздух с улицы должен быть нагрет и увлажнен, что требует больших затрат тепловой энергии. Нагрев с помощью электричества обходится особенно дорого.
Качество грибов и урожай зависят также от способа обдува грибов воздухом в камере, от способа рециркуляции воздуха. Самое плохое решение — это подача в камеру нагретого и увлажненного воздуха, который после однократного прохода через камеру удаляется в выхлопное окно с помощью вытяжного вентилятора. Надо, чтобы воздух сначала многократно прошел сквозь зону роста грибов и только после этого, «собрав» с грибов и с блоков углекислый газ, вышел на улицу.
Одна из таких систем рециркуляции воздуха — это обдув грибов ламинарным потоком воздуха.
Стенки с блоками располагают вдоль длинной стороны камеры на расстоянии 1 м одна от другой. Оставляют незанятый грибами коридор (проход) параллельный стойкам с грибами и отгороженный от них легкой перегородкой. В коридоре устанавливают осевые вентиляторы большой производительности, нагреватели и увлажнители воздуха. Такой коридор называют «климатическим коридором». Туда же подают свежий воздух. Воздух камеры прогоняется вентиляторами по коридору, там увлажняется и нагревается, а возвращается через зону размещения стенок с субстратными блоками. Воздух многократно циркулирует, обдувая грибы. Лишь насытившись углекислым газом, он удаляется в выхлопное окно под действием давления, создаваемого приточным вентилятором свежего воздуха, производительность которого много меньше, чем осевых вентиляторов в коридоре.
Оставляют незанятый грибами коридор (проход) параллельный стойкам с грибами и отгороженный от них легкой перегородкой. В коридоре устанавливают осевые вентиляторы большой производительности, нагреватели и увлажнители воздуха. Такой коридор называют «климатическим коридором». Туда же подают свежий воздух. Воздух камеры прогоняется вентиляторами по коридору, там увлажняется и нагревается, а возвращается через зону размещения стенок с субстратными блоками. Воздух многократно циркулирует, обдувая грибы. Лишь насытившись углекислым газом, он удаляется в выхлопное окно под действием давления, создаваемого приточным вентилятором свежего воздуха, производительность которого много меньше, чем осевых вентиляторов в коридоре.
Здесь вы можете посмотреть видео выращивания грибов вешенок в помещении с ламинарным потоком воздуха:
Выращивание вешенок в помещении с вихревой системой рециркуляции воздуха
Мешки с субстратом в камере размещают в виде высоких вертикальных сплошных стенок, перпендикулярных к длинной стороне камеры культивации. Расстояние между соседними стеллажами составляет 1 м. Зона с грибами отделена от стен со всех сторон проходами. Ширина одного прохода 2 м, остальных трех — 1 м. Климатическим коридором служит продольный двухметровый проход, не отгороженный от зоны с грибами. В нем устанавливают струйный вентилятор. Над струей воздуха, создаваемой струйным вентилятором, подвешивают нужное количество мелкодисперсных увлажнителей (аэрозольные генераторы типа АГ-1). Свежий воздух подается в камеру через окно. Он вытесняет отработанный воздух вместе с выделенным грибами углекислым газом через выхлопное окно в потолке камеры. При умеренных температурах наружного воздуха его можно подавать отдельным вентилятором непосредственно с улицы. Но зимой воздух должен быть предварительно нагрет. Система предварительной подготовки свежего воздуха включает в себя радиальный вентилятор среднего давления в количестве не менее 200 м3/ч в расчете на каждую тонну субстрата.
Расстояние между соседними стеллажами составляет 1 м. Зона с грибами отделена от стен со всех сторон проходами. Ширина одного прохода 2 м, остальных трех — 1 м. Климатическим коридором служит продольный двухметровый проход, не отгороженный от зоны с грибами. В нем устанавливают струйный вентилятор. Над струей воздуха, создаваемой струйным вентилятором, подвешивают нужное количество мелкодисперсных увлажнителей (аэрозольные генераторы типа АГ-1). Свежий воздух подается в камеру через окно. Он вытесняет отработанный воздух вместе с выделенным грибами углекислым газом через выхлопное окно в потолке камеры. При умеренных температурах наружного воздуха его можно подавать отдельным вентилятором непосредственно с улицы. Но зимой воздух должен быть предварительно нагрет. Система предварительной подготовки свежего воздуха включает в себя радиальный вентилятор среднего давления в количестве не менее 200 м3/ч в расчете на каждую тонну субстрата.
Воздух забирается с улицы через противомоскитную сетку, проходит через предварительный нагреватель воздуха до достижения положительных температур, затем поступает в смесительный короб, где может смешиваться с воздухом камеры. Клапан регулировки в смесительном коробе позволяет регулировать количество воздуха по отношению к воздуху из камеры. Между смесительным коробом и вентилятором устанавливают основной электронагреватель воздуха или нагревательный теплообменник. В системе вентиляции свежий воздух нагревается до нужной температуры и поступает в «климатический коридор» через окно. Суммарную тепловую мощность двух нагревателей можно примерно оценить из расчета 2-3 кВт на каждые 200 м3/ч подаваемого свежего воздуха. Нагрев свежего воздуха и время включения аэрозольных генераторов регулируются так, чтобы температура воздуха в камере была +15 °С при влажности 80%. При отсутствии охладителей наружного воздуха летом свежий воздух может иметь более высокую температуру, но аэрозольные генераторы уменьшают ее на несколько градусов.
Клапан регулировки в смесительном коробе позволяет регулировать количество воздуха по отношению к воздуху из камеры. Между смесительным коробом и вентилятором устанавливают основной электронагреватель воздуха или нагревательный теплообменник. В системе вентиляции свежий воздух нагревается до нужной температуры и поступает в «климатический коридор» через окно. Суммарную тепловую мощность двух нагревателей можно примерно оценить из расчета 2-3 кВт на каждые 200 м3/ч подаваемого свежего воздуха. Нагрев свежего воздуха и время включения аэрозольных генераторов регулируются так, чтобы температура воздуха в камере была +15 °С при влажности 80%. При отсутствии охладителей наружного воздуха летом свежий воздух может иметь более высокую температуру, но аэрозольные генераторы уменьшают ее на несколько градусов.
Мощная и узкая струя воздуха, создаваемая струйным вентилятором, организует циркулярное движение воздуха вокруг стеллажей с грибами. Сама струя и эти потоки в соответствии с законом Бернулли создают в камере градиент давления, который обеспечивает движение воздуха по проходам между стеллажами, омывающее грибы. В ближних к вентилятору проходах воздух движется к «климатическому коридору», а в дальних — от него.
В ближних к вентилятору проходах воздух движется к «климатическому коридору», а в дальних — от него.
Циркулярное движение воздуха вокруг стеллажей с грибами приводит также к циркуляциям воздуха вблизи грибов. Такая вихревая система рециркуляции воздуха улучшает удаление углекислого газа от грибов и от прорезей в мешках.
Струя воздуха в центральном проходе выполняет также функцию хорошего перемешивания воздуха камеры с теплым воздухом из вентилятора, с паром и с водным аэрозолем.
Посмотрите видео, как выращивать вешенки в помещении с вихревой системой рециркуляции воздуха:
Выращивание вешенок на субстратных брикетах
На крупных производствах используется оборудование для выращивания вешенок в виде автоматических брикетировщиков итальянского производства с производительностью порядка 360 брикетов в час. После охлаждения субстрата в тоннеле его выгружают электролебедкой на транспортерную ленту брикетировщика, где установлен дозатор мицелия и происходит посев субстрата. Затем инокулированный субстрат попадает в камеру пресса, где брикет формируется и упаковывается в перфорированную пленку.
После охлаждения субстрата в тоннеле его выгружают электролебедкой на транспортерную ленту брикетировщика, где установлен дозатор мицелия и происходит посев субстрата. Затем инокулированный субстрат попадает в камеру пресса, где брикет формируется и упаковывается в перфорированную пленку.
Параметры готового субстрата для грибов вешенок: влажность = 70-74%, pH =7,5-8,5, азот общий (11общ) = 0,7-1,0%, Окраска равномерно коричневая, плотность субстрата 0,45-0,50 кг/л. Габаритные размеры брикетов субстрата вешенки 35 х 55 х 22 см, масса 20-22 кг.
Ниже приведен пример простого, реализованного на практике варианта выгонки грибов из брикетов. Субстрат в брикетах размещают на четырех четырехъярусных стеллажах. В камере размещается 20 т субстрата. Удельная нагрузка субстрата составляет 180 кг на 1 м2 пола камеры. Зимой воздух подогревается батареями парового отопления. Свежий воздух поступает в камеру плодоношения через форточки. Объем поступления свежего воздуха и температуру воздуха регулируют степенью открытия форточек. Поток воздуха проходит через стеллажи с грибами и удаляется вытяжным вентилятором. Воздух в камере увлажняется одним аэрозольным генератором типа АГ-1, который подвешен под потолком камеры в центральном проходе. Перед аэрозольным генератором подвешен осевой вентилятор производительностью 1700 м3/ч. Он создает струю воздуха, которая захватывает «туман» от генератора и перемешивает воздух в камере. Мелкодисперсный распылитель АГ-1 и вентилятор включаются вместе по таймеру.
Поток воздуха проходит через стеллажи с грибами и удаляется вытяжным вентилятором. Воздух в камере увлажняется одним аэрозольным генератором типа АГ-1, который подвешен под потолком камеры в центральном проходе. Перед аэрозольным генератором подвешен осевой вентилятор производительностью 1700 м3/ч. Он создает струю воздуха, которая захватывает «туман» от генератора и перемешивает воздух в камере. Мелкодисперсный распылитель АГ-1 и вентилятор включаются вместе по таймеру.
Вытяжной вентилятор производительностью 5000 м3/ч вмонтирован в противоположную от окна стену камеры. Вентиляторы включаются по таймеру каждые полчаса на 5 мин. В летний период система отлично работает и позволяет получать грибы хорошего качества. В зимний период приходится ограничивать подачу воздуха из-за недостаточной мощности отопительной системы. Зимой во время работы вытяжных вентиляторов морозный свежий воздух заходит через форточку. Однако грибы не успевают замерзнуть и достаточно хорошо растут. Во время инкубации мицелия окна закрыты, вытяжные вентиляторы не работают. Приоткрывают окна и включают ненадолго вытяжные вентиляторы лишь в случае, если температура в центре блока поднимается выше +35 °С. После этого температура в камере поддерживается от +13 до +20 °С. Урожайность за две волны плодоношения достигает 20% от массы субстрата.
Приоткрывают окна и включают ненадолго вытяжные вентиляторы лишь в случае, если температура в центре блока поднимается выше +35 °С. После этого температура в камере поддерживается от +13 до +20 °С. Урожайность за две волны плодоношения достигает 20% от массы субстрата.
Подготовка субстрата для выращивания грибов вешенок в тоннеле
В шампиньонных комплексах в огромном количестве производят субстрат для вешенки в тех же тоннелях, что и шампиньонный компост. Хорошее качество субстрата для вешенки, сделанного в тоннеле на ферме, где делают шампиньонный компост, объясняется использованием оборотной воды из шампиньонного цеха с аэробными микроорганизмами. На фермах, где не производят шампиньоны, улучшают субстрат для вешенки добавкой в оборотную воду навоза в количестве до 10 кг на тонну соломы.
Стандартная технология подготовки субстрата для выращивания вешенок начинается с измельчения соломы. Измельчение соломы до частиц размером 3-8 см нужно для того, чтобы в дальнейшем было проще набивать субстрат в мешки. Солому увлажняют оборотной водой на бетонной площадке 1-5 дней, периодически переворачивая. Влажность соломы при загрузке тоннеля должна быть на уровне 78%. Тоннель заполняют соломой слоем до 2,5 м, так чтобы его поверхность была ровной. После пастеризации слой соломы существенно оседает. Для размещения 1 т соломы субстрата требуется около 1,5 м2 площади пола тоннеля.
Солому увлажняют оборотной водой на бетонной площадке 1-5 дней, периодически переворачивая. Влажность соломы при загрузке тоннеля должна быть на уровне 78%. Тоннель заполняют соломой слоем до 2,5 м, так чтобы его поверхность была ровной. После пастеризации слой соломы существенно оседает. Для размещения 1 т соломы субстрата требуется около 1,5 м2 площади пола тоннеля.
После загрузки тоннель закрывают и включают рециркуляционную вентиляцию для выравнивания температуры в массе субстрата. Затем начинают добавлять 1% свежего воздуха. Зимой для начального разогрева субстрата для выращивания вешенок снизу вместе с воздухом подают пар. Через некоторое время в субстрате начинается подъем микробиологической активности. Субстрат начинает разогреваться сам, и для поддержания температуры пастеризации требуется все меньше пара и все больше (до 5%) свежего воздуха. Температуру повышают медленно, разогрев субстрата занимает 12 ч летом и до 24 ч зимой. Парогенератор должен обеспечивать подачу 25 кг пара в час на каждую тонну субстрата.
По достижении температуры +65 °С начинается процесс пастеризации. Во время пастеризации объем подачи свежего воздуха составляет 5% от общего объема рециркуляции, или 10 м3/ч на 1 т субстрата. После двенадцатичасовой пастеризации для последующей ферментации субстрат охлаждают до +50 °С (в течение 8-10 ч) за счет увеличения объема свежего наружного воздуха до 30%. Затем проводят ферментацию субстрата при +45…+50 °С от 24 до 48 ч при подаче большого объема свежего воздуха (20%). По окончании пастеризации или ферментации массу субстрата стараются быстро охладить свежим воздухом, который в этот момент впускают в объеме до 100%. При подготовке субстрата для вешенок его охлаждают до +28 °С зимой, а летом до +24 °С. Процесс охлаждения занимает от 12 до 24 ч в зависимости от сезона и температуры окружающего воздуха.
При приготовлении субстрата для вешенок его выгружают конвейером, лебедкой с системой подвижных полов (сеток), другими механизмами или вручную. Мицелий вносят в субстрат в пропорции от 2 до 5% от массы субстрата. Инокуляцию проводят в чистом помещении, расположенном рядом с камерой термообработки. Мицелий равномерно распределяют в субстрате и полученную смесь фасуют в полиэтиленовые мешки.
Инокуляцию проводят в чистом помещении, расположенном рядом с камерой термообработки. Мицелий равномерно распределяют в субстрате и полученную смесь фасуют в полиэтиленовые мешки.
Как сделать субстрат для вешенок по гидротермической технологии
Наиболее доступная для малообъемного производства вешенки технология термообработки субстрата — это замачивание субстрата в мешках в горячей воде. Емкость для гидротермической обработки представляет собой металлический бак с электронагревателями воды в нижней части и с горизонтальной решеткой над нагревателями.
Перед тем как приготовить субстрат для вешенок по гидротермической технологии, измельченную солому в сухом виде загружают в новые или использованные плетеные полипропиленовые мешки, в которые обычно фасуют сахар. Можно также сделать субстрат из подсолнечной лузги без добавок или из равных частей древесной щепы и хлопковых очесов. Мешки с субстратом ставят вертикально, закрывают сверху распорами от всплывания и накрывают крышкой. Бак заполняют водой. Субстрат в мешках должен быть 96 полностью покрыт водой. Нагрев продолжается 12-13 ч. Температура воды не должна подниматься выше 82-85 °С. После того как температура будет достигнута, выключают нагреватели и выдерживают субстрат в воде в течение 4 ч. Затем воду сливают. А можно горячие мешки выгрузить из бака на решетчатый пол, где оставить на ночь. Утром начинают инокуляцию субстрата мицелием в отдельном чистом помещении. Субстрат забирают из бокса отдельными мешками и вытряхивают на инокуляционный стол. Температура субстрата при инокуляции не должна превышать +
Бак заполняют водой. Субстрат в мешках должен быть 96 полностью покрыт водой. Нагрев продолжается 12-13 ч. Температура воды не должна подниматься выше 82-85 °С. После того как температура будет достигнута, выключают нагреватели и выдерживают субстрат в воде в течение 4 ч. Затем воду сливают. А можно горячие мешки выгрузить из бака на решетчатый пол, где оставить на ночь. Утром начинают инокуляцию субстрата мицелием в отдельном чистом помещении. Субстрат забирают из бокса отдельными мешками и вытряхивают на инокуляционный стол. Температура субстрата при инокуляции не должна превышать +
30 °С.
Наряду с описанным выше есть другой вариант гидротермической обработки субстрата. Сухую солому или лузгу подсолнечника предварительно закладывают в емкость и накрывают тяжелым щитом, который не даст ей всплыть. Нагретую бойлерами или в специальных баках до температуры +80 °С воду наливают в емкость, так чтобы полностью закрыть субстрат. Температура воды после теплообмена с субстратом +70 °С. Субстрат оставляют под водой на ночь. Утром воду сливают. Спустя несколько часов начинают инокуляцию и изготовление субстратных блоков.
Субстрат оставляют под водой на ночь. Утром воду сливают. Спустя несколько часов начинают инокуляцию и изготовление субстратных блоков.
Субстрат из лузги подсолнечника допускает ускоренную гидротермическую обработку путем кипячения в воде. Лузгу подсолнечника фасуют в плетеные полипропиленовые мешки, выдерживают 4 ч в баке с теплой водой при температуре около +30 °С. Затем привязывают к мешкам веревку достаточной длины и погружают в бак с кипящей водой. Через 30 мин мешки вынимают из кипятка и подвешивают на веревках. С мешков стекает вода, и они просушиваются до следующего утра. После того как субстрат остынет до +30 °С, производят инокуляцию мицелием. Через одну порцию воды можно пропустить до5 порций субстрата.
Основным недостатком гидротермической технологии является сильное переувлажнение субстрата. При избытке воды в субстрате возникают анаэробные зоны. На субстратном блоке появляются темные пятна, развиваются плесени, в нижней части мешка скапливается вода, быстрее разводятся грибные мухи.
Наименьшее увлажнение дает варка субстрата с последующей просушкой мешков в подвешенном состоянии. Следует заметить, что избыточное переувлажнение субстрата меньше себя проявляет при использовании в качестве основы хлопковых очесов.
Приготовление и обработка субстрата для вешенок водяным паром
Субстрат сначала увлажняют тем или иным способом до нужной влажности (W = 60%) затем его кладут на сетки в бак и под негерметичной крышкой обрабатывают паром 4 ч, считая с момента разогрева субстрата до +90 °С. Подачу пара прекращают и оставляют субстрат остывать на ночь. Утром переносят субстрат в чистое помещение для инокуляции. Эта технология хорошо себя зарекомендовала при обработке субстрата с хлопковыми очесами. Удобно использовать небольшой бак с внутренними размерами 1,0 х 1,0 х 1,0 м, который имеет штуцер для слива воды и систему подачи пара под субстрат. Внутри бачка приварены уголки, на которые устанавливают армированные уголком сетки для субстрата. Сетки с ручками размером 100 х 33 см устанавливают по три на каждый этаж. На сетку раскладывают предварительно замоченный субстрат слоем 20 см. На каждой сетке лежит вес 30-35 кг. После термообработки такую сетку два работника легко поднимают и относят на стол для инокуляции.
Сетки с ручками размером 100 х 33 см устанавливают по три на каждый этаж. На сетку раскладывают предварительно замоченный субстрат слоем 20 см. На каждой сетке лежит вес 30-35 кг. После термообработки такую сетку два работника легко поднимают и относят на стол для инокуляции.
В средней климатической полосе России рациональнее использовать березовые и осиновые дрова. На грибной ферме в Волоколамском районе успешно выращивают вешенку на щепе осины, обработанной паром. Древесные стволы диаметром не более 20 см измельчают в дробилке до мелкой щепы размером 10-30 мм. Более толстые дрова приходится рубить на несколько частей перед перемалыванием. Естественная влажность дров составляет 40-50%. Содержание азота в древесине всего около 0,1%. Поэтому в субстрат дополнительно добавляют зерно овса или ячменя в количестве 20% от массы древесины. Термообработку и перемешивание делают в субстратной машине, которая представляет собой вращающуюся на оси бочку. В нее можно удобно загрузить щепу и зерно, залить воду, подать пар и все перемешать.
Древесную щепу загружают пневматически пылевым вентилятором в субстратную машину. Поскольку щепа довольно тяжелая, загрузка происходит быстро. Затем добавляют зерно овса или ячменя из расчета 20% от массы щепы и воду. Количество воды рассчитывают, исходя из исходной и нужной влажности субстрата. Оптимальная влажность субстратной смеси от 65 до 70% — в этом случае в субстрате не будет свободной воды. Затем, перемешивая эту смесь, подают пар для нагревания. Смесь нагревают до +90°С и выдерживают при этой температуре 2 ч. Подача пара не сильно увеличивает влажность субстрата, но все же при отработке технологии надо измерить влажность готового субстрата и скорректировать количество добавляемой воды.
Вместо субстратной машины можно использовать пропарочный бак, но в таком случае щепу предварительно перемешивают с зерном и необходимым количеством воды на чистом бетонном полу.
После охлаждения в субстрат добавляют мицелий, тщательно перемешивают и фасуют. Масса мешка составляет 16-18 кг.
Длительность инкубации при обработке субстрата для вешенок на смешанном с зерном древесном субстрате составляет 25 дней. Урожайность грибов на первой волне составляет от 15 до 18% от массы блока. Вешенки получаются красивыми, плотными и ароматными.
Как подготовить субстрат для вешенок экономичными способами
Чтобы сделать субстрат для вешенок, можно использовать один из предложенных ниже экономичных способов.
Ксеротермическая обработка субстрата. При применении этой технологии расходуется меньше энергии на нагрев пара, поскольку теплоемкость сухой соломы меньше теплоемкости влажной. Паром обрабатывается сухая солома, затем в субстрат на чистом полу добавляется холодная чистая вода. Измельченная солома поступает по транспортеру или пневмотранспортеру в бункер термообработки, где ее температура доводится паром до +95…+100 °С. Обработка при этой температуре продолжается 1-2 ч. Солома для ксеротермической технологии должна быть без плесени. После ксеротермической обработки всегда остаются сухие участки соломин, а для уничтожения сухих спор плесеней нужна температура +160 °С.
После ксеротермической обработки всегда остаются сухие участки соломин, а для уничтожения сухих спор плесеней нужна температура +160 °С.
Анаэробная ферментация субстрата в воде — это выдерживание субстрата в воде без доступа воздуха при температурах от комнатной до +60 °С. Субстрат выдерживают до трех суток. При этом вырабатывается его защита от плесеней. Качественными показателями готовности субстрата являются неприятный запах анаэробных процессов и наличие бактериальной пленки на поверхности воды. Снижение температуры до +30…+40 °С приводит к тому, что запах становится непереносимым и ухудшаются свойства субстрата. При низких температурах ферментация занимает от одной до двух недель, но низкотемпературная анаэробная обработка, несмотря на свою экономичность, широкого распространения не получила. Все недостатки гидротермии характерны и для анаэробной ферментации (кроме большого энергопотребления).
Как ещё можно приготовить субстрат для вешенок
Ещё можно подготовить субстрат для вешенок путем обработки в герметичных бочках без доступа воздуха и без термической обработки.
Обработка субстрата в герметичных бочках без доступа воздуха. Замоченный до нужной влажности субстрат обрабатывается в воздушной среде, но без доступа свежего воздуха во время термообработки. Пастеризация без доступа воздуха проводится при температуре +60…+70 °С в герметичных емкостях. Отличие от гидротермии и от анаэробной ферментации заключается в отсутствии свободной воды в промежутках между частицами субстрата. Субстрат обрабатывается в термокамере в герметично закрытых бочках. Кислород воздуха расходуется полезной микрофлорой субстрата, поэтому крышки бочек присасываются к бочкам за счет разности давлений. Результат технологии достаточно хорош при влажности субстрата 65%. Нужен точный расчет количества добавляемой воды.
Изготовление субстрата без термической обработки. Лузга подсолнечника, прогретая на маслобойном заводе, не бывшая под дождем, может дать хороший результат без термической обработки. Лузгу замачивают 2 суток при комнатной температуре в воде с гашеной известью, которая не растворяется и в основном остается на дне емкости. Затем ее оставляют на ночь на сетке для стекания воды. Утром добавляют мицелий в количестве 1-3% и засыпают в перфорированные полиэтиленовые мешки, рассчитанные на 10 кг субстрата. Урожай на первой волне достигает 18% от влажной массы.
Затем ее оставляют на ночь на сетке для стекания воды. Утром добавляют мицелий в количестве 1-3% и засыпают в перфорированные полиэтиленовые мешки, рассчитанные на 10 кг субстрата. Урожай на первой волне достигает 18% от влажной массы.
Выращивание грибов вешенок на стеллажах
В некоторых хозяйствах, предназначавшихся для выращивания шампиньонов, успешно выращивают вешенку на стеллажах. Засеянные мицелием субстратные брикеты плотно укладывают на стеллажи шириной 140 см в виде грядки толщиной 20 см. Перфорацию делают только сверху. При использовании насыпного, засеянного мицелием вешенки субстрата его насыпают на стеллаж ровным слоем, уплотняют и накрывают сверху перфорированной полиэтиленовой пленкой. При выращивании вешенок на стеллажах грибы буду расти вертикально вверх, а их форма будет почти симметричной, как у грибов, растущих на земле.
Параметрами климата в камере управляют в соответствии с заданным графиком культивирования. Рассмотрим для примера типичный вариант шампиньонной камеры. Ширина камеры со стеллажами для вешенок составляет 6,0 м. При высоте камеры 2,8 м в ней можно разместить 4-ярус-ные стеллажи. Ширина среднего прохода точно 1 м. Длина стеллажей 17,5 м, ширина 140 см. Расстояние от пола до полки 1-го яруса 20 см, между полками (по высоте яруса) 60 см. Для насыпного субстрата нужна полка в виде корыта с бортиками 20 см. На полке субстрат толщиной 20 см, над ним воздушный промежуток 35-40 см. Субстратные брикеты кладут вплотную в виде четырех линий шириной 35 см. Получается ширина грядки 140 см. Полная загрузка камеры — 20 т субстрата. Для нормального развития грибов вешенки в период плодоношения вентиляция свежим воздухом должна быть не меньше, чем 200 м3/ч на тонну субстрата. Для продавливания воздуха, через систему кондиционирования с полиэтиленовым воздуховодом потребуется давление 400 Па. В данном случае требуется радиальный
Ширина камеры со стеллажами для вешенок составляет 6,0 м. При высоте камеры 2,8 м в ней можно разместить 4-ярус-ные стеллажи. Ширина среднего прохода точно 1 м. Длина стеллажей 17,5 м, ширина 140 см. Расстояние от пола до полки 1-го яруса 20 см, между полками (по высоте яруса) 60 см. Для насыпного субстрата нужна полка в виде корыта с бортиками 20 см. На полке субстрат толщиной 20 см, над ним воздушный промежуток 35-40 см. Субстратные брикеты кладут вплотную в виде четырех линий шириной 35 см. Получается ширина грядки 140 см. Полная загрузка камеры — 20 т субстрата. Для нормального развития грибов вешенки в период плодоношения вентиляция свежим воздухом должна быть не меньше, чем 200 м3/ч на тонну субстрата. Для продавливания воздуха, через систему кондиционирования с полиэтиленовым воздуховодом потребуется давление 400 Па. В данном случае требуется радиальный
вентилятор производительностью 4000 м3/ч при рабочем давлении 400 Па. Полиэтиленовый воздуховод в камере представляет собой надутый воздухом полиэтиленовый рукав диаметром около 50 см, снабженный направленными вниз форсунками диаметром 6 см. Воздуховод подвешивается под потолком посередине центрального прохода, так чтобы поток воздуха из форсунок был направлен вертикально вниз. Длина воздуховода 17 м. Дальний от кондиционера конец воздуховода заглушается. Воздуховод изготавливается из полиэтиленового рукава шириной 80см при толщине пленки 100 мкм. Расстояние между отверстиями-форсунками 50см, а число форсунок в воздуховоде 33.
Воздуховод подвешивается под потолком посередине центрального прохода, так чтобы поток воздуха из форсунок был направлен вертикально вниз. Длина воздуховода 17 м. Дальний от кондиционера конец воздуховода заглушается. Воздуховод изготавливается из полиэтиленового рукава шириной 80см при толщине пленки 100 мкм. Расстояние между отверстиями-форсунками 50см, а число форсунок в воздуховоде 33.
При достаточно большой скорости истечения воздуха из форсунок начинается циркулярное движение воздуха вокруг стеллажей — воздух опускается в проходе с воздуховодом и поднимается в проходах, где воздуховодов нет. При выращивании грибов вешенок на стеллажах струи воздуха из форсунок создают в верхней половине прохода пониженное давление, в нижней половине — повышенное. Разность давлений заставляет двигаться воздух над поверхностью грядок. Такая система распределения воздуха хорошо перемешивает воздух камеры и выравнивает температуру воздуха по объему помещения. Урожайность вешенки — около 20% по отношению к массе субстрата. Вырастают плотные, тяжелые грибы отличного качества.
Вырастают плотные, тяжелые грибы отличного качества.
Технология выращивания вешенок: как вырастить грибы в мешках в теплицах
Существует ещё одна технология выращивания вешенок – в мешках, размещенных в теплицах. Она применяется в некоторых хозяйствах в осенне-зимний период, в перерывах между оборотами овощных культур. Агрокомбинат «Московский» долгое время успешно практиковал выращивание вешеноки в теплицах, свободных от овощей в зимнее время. Пустые стеклянные теплицы не могут держать снег на крыше, поэтому воздух в них подогревают всю зиму. Тепло для выращивания грибов получается бесплатным.
Технология выгонки грибов в АГК «Московский» была предельно проста. Подготовленный в тоннелях пастеризации субстрат перемешивали с мицелием (3%) и засыпали в полиэтиленовые мешки по 20 кг субстрата в каждый. Мешки для выращивания грибов вешенок завязывали, перфорировали ножами их боковую поверхность и отвозили на инкубацию в свободное бетонное овощехранилище или в складское помещение площадью до 800 м2. Мешки ставили на пол с небольшими промежутками, а температуру воздуха поднимали до +5…+10 °С переносными нагревателями. После этого субстратные блоки, разогреваясь сами, помогают нагревателям. Температуру воздуха в теплицах для грибов вешенок поддерживали в диапазоне +20…+28 °С в зависимости от температуры субстрата внутри блоков, которая не должна превышать 35 °С. Спустя 20-25 дней те блоки, которые обросли мицелием, перевозили для выгонки грибов в теплицу.
Мешки ставили на пол с небольшими промежутками, а температуру воздуха поднимали до +5…+10 °С переносными нагревателями. После этого субстратные блоки, разогреваясь сами, помогают нагревателям. Температуру воздуха в теплицах для грибов вешенок поддерживали в диапазоне +20…+28 °С в зависимости от температуры субстрата внутри блоков, которая не должна превышать 35 °С. Спустя 20-25 дней те блоки, которые обросли мицелием, перевозили для выгонки грибов в теплицу.
В теплицах площадью более 1000 м2 используется оборудование для выращивания грибов вешенок с нагревательными регистрами по периферии, системой дождевания (полива) и открываемыми фрамугами для вентиляции. На землю был насыпан слой сосновой щепы толщиной 5 см. Нет ни вентиляторов, ни датчиков влажности воздуха, ни измерителей содержания СО2. В морозные дни вентиляция свежим воздухом осуществлялась лишь за счет щелей в воротах, иногда открываемых для вывоза тележек с собранными грибами и для размещения новых мешков с субстратом. Для увлажнения почвы и воздуха проводили два полива в сутки. Чтобы вырастить грибы вешенки в теплице, поливы (интенсивное дождевание по всей поверхности теплицы) включали на 10 мин в полдень и в 3 ч дня. Чтобы избежать пожелтения грибов (их бактериоза) надо следить, чтобы к вечеру грибы просыхали от воды. Единственный параметр, который поддерживался автоматически, это температура воздуха +12…+15 °С. Фрамуги вентиляции при выращивании в теплице грибов вешенок открывали только иногда, весной или осенью. За счет низкой плотности размещения субстрата (менее 50 кг/м2 поверхности земли) и большого объема воздуха в теплице грибы росли высококачественными. Урожайность достигала 17% за цикл культивации 90 дней (3 волны).
Для увлажнения почвы и воздуха проводили два полива в сутки. Чтобы вырастить грибы вешенки в теплице, поливы (интенсивное дождевание по всей поверхности теплицы) включали на 10 мин в полдень и в 3 ч дня. Чтобы избежать пожелтения грибов (их бактериоза) надо следить, чтобы к вечеру грибы просыхали от воды. Единственный параметр, который поддерживался автоматически, это температура воздуха +12…+15 °С. Фрамуги вентиляции при выращивании в теплице грибов вешенок открывали только иногда, весной или осенью. За счет низкой плотности размещения субстрата (менее 50 кг/м2 поверхности земли) и большого объема воздуха в теплице грибы росли высококачественными. Урожайность достигала 17% за цикл культивации 90 дней (3 волны).
На тепличный грунт насыпают слой щепы или опилок толщиной 4-6 см. В дальнейшем это покрытие в период плодоношения постоянно поддерживают во влажном состоянии. Испарение воды со щепы обеспечивает нормальный режим влажности воздуха для формирования качественных грибов.
Выращивание вешенки в домашних условиях – идея для грибников и бизнесменов
7122 Просмотров
Большинство людей ошибочно считает, что вырастить грибы самостоятельно непросто, так как требуется особое оборудование и сложные технологии. На самом деле выращивание вешенки в домашних условиях – дело нехитрое, ведь их можно высаживать даже на подоконнике. Еще лучше для этой цели подойдут отапливаемый гараж, подвал или теплица – такой вариант позволит не только обеспечить себя и семью этим ценным продуктом, но и немного заработать, организовав свой малый бизнес.
На самом деле выращивание вешенки в домашних условиях – дело нехитрое, ведь их можно высаживать даже на подоконнике. Еще лучше для этой цели подойдут отапливаемый гараж, подвал или теплица – такой вариант позволит не только обеспечить себя и семью этим ценным продуктом, но и немного заработать, организовав свой малый бизнес.
Преимущества разведения
Эта грибная культура не требует особого внимания или ухода. Если соблюдалась технология выращивания вешенки, можно получить отличный результат при относительно небольших затратах. Этому способствуют следующие факторы:
- Гриб неприхотлив, способен расти при температуре от 9 до 25°C, если обеспечить необходимую влажность.
- Высаженные грибы занимают мало места. В помещении площадью 50 м2 получается разместить 200-250 грибных блоков, каждый из которых дает урожай в 2-3 кг около 10 раз за год.
- За грибными посадками под силу ухаживать одному человеку – они не требуют выполнения трудоемких работ.
Этапы выращивания вешенок в домашних условиях
Для успеха доходного культивирования грибов необходимо:
- Подготовить помещение для выращивания вешенки.

- Обустроить место, где будут произрастать грибы (пень, мешок с соломой или ящик с субстратом для вешенки).
- Приобрести мицелий.
- Посеять грибные споры (мицелий) на подготовленную почву.
- Выждать период инкубации (при температуре около 20°C он составит 10 дней).
- Собирать урожай по мере роста грибницы.
Соблюдая несложные технологии на каждом этапе, можно за короткое время получить хороший урожай.
Подготовка помещения для произрастания гриба
Для успешного культивирования грибной культуры в помещении должен быть определенный микроклимат. Для его создания нужны:
- Постоянная температура +15-20°C. Температурные колебания повлекут за собой изменения влажности, что отрицательно скажется на урожае.
- Влажность 80-95%. При понижении влажности ниже этого предела грибы начнут высыхать, а при 100% будет слишком «запревать» субстрат, древесина заплесневеет, а металлические крепления покроются ржавчиной.
- Все грибы хорошо растут только при низком уровне углекислого газа, поэтому в помещении необходимо создать хорошую вентиляцию.
 Лучше всего для этого установить центробежные вентиляторы, обеспечивающие усиленную циркуляцию воздушных масс.
Лучше всего для этого установить центробежные вентиляторы, обеспечивающие усиленную циркуляцию воздушных масс. - Грибам для развития и роста необходим свет, но не обычный, а от флуоресцентной лампы. Выращивание вешенки при использовании обычных ламп дает плохой результат.
- Санитарные условия. Помещение должно быть чистым, обработанным от плесени. Тогда грибная культура лучше развивается и меньше болеет.
В качестве пригодных для разведения вешенки помещений можно взять:
- Капитальные гаражи. В гараже очень удобно заниматься разведением грибов: помещение почти не требует переоборудования, ведь там уже имеются вентиляция и отопление.
- Теплица для этой цели подойдет не любая. Простые термостойкие теплицы, установленные у большинства людей на даче, не подходят из-за того, что во время летнего периода температура внутри поднимается свыше 20°C, что будет губительным для грибницы. В теплице с хорошей вентиляцией, чуть затемненными окнами и контролем температуры культура дает хороший урожай.

- Теплые подвалы с хорошей вентиляцией станут почти идеальным местом, где можно круглогодично поддерживать необходимую температуру и влажность. Выращивание вешенки в подвале практикуется среди предпринимателей намного чаще, чем использование для этой цели наземных построек. В подвале намного проще обеспечить постоянный климат-контроль и освещенность.
- Бывшие хозпостройки (птичники, коровники): после небольших работ по установке дополнительного оборудования там вполне можно сажать грибную культуру.
- На улице во время весенне-летнего сезона также можно получить хороший урожай на пеньках, оставшихся после вырубки деревьев на участке.
Для грибоводства можно использовать также другие подземные или наземные постройки, если их переоборудование позволяет создать подходящие условия для выращивания грибницы.
Подготовка почвы
Для того чтобы урожайность была высокой, необходимо обеспечить грибам почву для произрастания. Это может быть:
- Выращивание вешенки на пнях.
 Рекомендуется использовать пеньки, оставшиеся на улице после спила деревьев, или обрезки любых бревен (искусственные пни).
Рекомендуется использовать пеньки, оставшиеся на улице после спила деревьев, или обрезки любых бревен (искусственные пни). - Культивация грибов в мешках с питательным субстратом.
- Разведение грибной культуры на соломе, выложенной в мешки.
- Выращивание вешенки на опилках.
Приготовление субстрата – процесс несложный. Чтобы почва для вешенок способствовала хорошему плодоношению, нужно:
- Взять солому любых зерновых культур, шелуху гречихи или кукурузные отходы (листья, пустые початки). Можно использовать одну составляющую или несколько.
- Желательно использовать мелкую древесную стружку или опилки в качестве добавки или самостоятельного наполнителя.
- Все компоненты хорошо измельчить, тщательно перемешать.
- Выложить в варочную посуду и залить водой, чтобы жидкость покрывала поверхность.
- Варить около 2-х часов.
- Излишки жидкости слить.
- Готовым субстратом для вешенки заполняется подготовленная тара, производится посев мицелия.

Приготовить питательный субстрат можно только из опилок или только из соломы, но лучше использовать оба компонента, взятые в произвольных пропорциях.
Покупка мицелия
Мицелий может храниться только 5 дней при комнатной температуре, поэтому подкупать его нужно небольшими партиями, необходимыми для посадки.
Для ускорения роста и повышения урожайности на 30% можно обработать грибные поры специальными органическими добавками, которые легко приобрести вместе с мицелием. Добавку используют по рекомендациям инструкции изготовителя.
Правила посадки
Для получения высокой урожайности необходимо правильно выполнить инструкцию, как посадить вешенки с учетом поверхности, куда планируется высаживать мицелий вешенки.
Высев мицелия производится либо на пни (природные или искусственные), либо на мешки с субстратом.
Посадка спор на пни
Если планируется засевать уличные пни, то посадку надо проводить в начале апреля, чтобы активное плодоношение пришлось на лето-осень. После высадки спор пенек обсыпается землей и укутывается полиэтиленом.
После высадки спор пенек обсыпается землей и укутывается полиэтиленом.
Перед высаживанием на природные или искусственные пни на древесине делаются пропилы глубиной 5 см, отстоящие друг от друга на 30 см, в них высеивается мицелий. Если планируется проводить проращивание в домашних условиях, то деревянные бруски ставятся в помещении вертикально или укладываются на специальные металлические этажерки.
Высадка мицелия на мешки
Этот способ наиболее удобный. Для посадки подойдут любые чистые строительные мешки. Инструкция по выращиванию вешенки рекомендует высевать грибницу одновременно с заполнением мешков субстратом, соблюдая следующие правила пошагово:
- Первый и последний слой в мешке должны состоять из субстрата.
- В тару укладывается слой субстрата толщиной 5 см, потом 0,5 см семян, и так чередуется до полного заполнения.
- На заполненном и завязанном мешке делаются маленькие надрезы через каждые 10 см (получается грибной блок). Блоки укладываются на полки или подвешиваются на крюках.

Санитарные правила
Правильно выполнив эти рекомендации, можно получить высокий урожай и избежать болезней культуры:
- Перед посадкой обязательно помыть и продезинфицировать руки (перчатки).
- За 3 часа до высадки достать из холодильника мицелий, дать ему прогреться до комнатной температуры.
Уход за культурой и сбор урожая
Чтобы вырастить дома хороший урожай, надо:
- Обильно поливать грибные блоки, как только начнется проращивание спор.
- При сборе готового урожая, когда грибная шляпка становится упругой, а тело плотным, нужно выдергивать его с корнем, а не срезать. Если этого не сделать, то срезы ножек станут местом для развития триходермы (зеленой плесени).
Причины возможных неудач
Некоторые предприниматели, изучив, как выращивать вешенки в домашних условиях, вскоре разочаровываются. Они отмечают, что культура плохо прорастает после посева, дает плохой урожай. Это связано с тем, что многие из них во время посева или ухода за грибницами допускают следующие ошибки:
- Неправильный температурно-влажностный режим мешает дружному прорастанию мицелия.
 Проблема решается регулировкой систем, отвечающих за создание оптимального микроклимата.
Проблема решается регулировкой систем, отвечающих за создание оптимального микроклимата. - Появление на поверхностях блока темно-зеленых пятен указывает, что они поражены плесенью. Такое может случиться из-за несоблюдения санитарных норм. Поврежденные блоки сжигаются, а помещение тщательно дезинфицируется.
- Грибы начинают желтеть, усыхать. Такое случается из-за низкой влажности. В этом случае следует отрегулировать приборы, смочить стены, поставить дополнительные емкости с водой.
- Сероватый налет, свидетельствующий о загнивании вешенки, провоцирует плесневый грибок. Помещение необходимо обработать солевым раствором, зараженные блоки уничтожить. Уцелевший урожай собирается, но такие грибы пригодны в пищу.
- Под блоками скапливается вода, ощущается гнилостный запах. Чтобы удалить излишки влаги, нужно увеличить дренажные разрезы. Во избежание таких проблем при поливе следует использовать распылитель, а не лейку.
Если правильно ухаживать за вешенкой, создавая для нее оптимальные условия, можно круглогодично получать высокий урожай. Достаточно только подобрать оптимальный температурно-влажностный режим, учитывая характеристики используемого помещения – тип вентиляции, отопления, наличие сквозняков.
Достаточно только подобрать оптимальный температурно-влажностный режим, учитывая характеристики используемого помещения – тип вентиляции, отопления, наличие сквозняков.
приготовление маточного мицелия в домашних условиях для выращивания грибов
Мицелий — это грибница, которую подсаживают в специальный грунт. При соблюдении необходимых условий грибница разрастётся, превращаясь в съедобные грибы. Происходит это довольно быстро, где-то через 6−8 недель. В домашних условиях мицелий вешенки можно приготовить, используя зёрна злаковых или древесину. Большим успехом у грибоводов пользуется первый вариант — злаковый субстрат.
Технология выращивания мицелия
Грибы ещё с глубокой древности прочно вошли в жизнь людей. Великое разнообразие видов, их приспособляемость к разным климатическим условиям сделали их доступными. Только вот грибы — продукт сезонный, а потребность в них есть круглый год. Выход нашёлся. Люди научились выращивать этот замечательный, ценный и питательный продукт. Особенно широкое распространение получило разведение вешенок и шампиньонов в домашних условиях.
Особенно широкое распространение получило разведение вешенок и шампиньонов в домашних условиях.
Для личного пользования, естественно, жёстко контролируется весь процесс производства, гарантируется защита от канцерогенов, которые легко всасываются грибами. И наконец, очень интересно заниматься их разведением.
Особенно учитывая доступность самостоятельного выращивания мицелий. Многие грибоводы вполне успешно справляются с этой задачей. Домашнее выращивание грибов даёт возможность сохранит семейный бюджет, а также уверенность в получении качественного урожая. Ещё вешенки помогают противостоять некоторым болезням, замедляют процессы увядания.
В природе грибы размножаются в основном спорами. Для культурного разведения учёными были опробованы различные способы. Первоначально приносились из леса фрагменты грибницы и подсаживались на специальный грунт, составленный по образцу природного. Грибница приживалась, давала плоды, но быстро вырождалась. Ожидаемого урожая не было. Через некоторое время во Франции разработали метод выведения грибницы из спор в лабораторных условиях. Способ тоже не нашёл широкого применения. И наконец, было запатентовано приготовление мицелия грибов вешенка в домашних условиях на зерне, опилках, подсолнуховой лузге.
Через некоторое время во Франции разработали метод выведения грибницы из спор в лабораторных условиях. Способ тоже не нашёл широкого применения. И наконец, было запатентовано приготовление мицелия грибов вешенка в домашних условиях на зерне, опилках, подсолнуховой лузге.
Выведение маточной культуры
Маточный мицелий своими руками можно изготовить непосредственно из свежего гриба. Вешенка разрезается пополам и из верхней части ножки отрезается маленький кусочек и помещается в колбочку со специальной стерильной средой. Сама частичка гриба тоже ложна быть стерильной. Для этого его окунают в перекись водорода. Для чистоты опыта пробочку от колбы обжигают над огнём и плотно укупоривают пробирку.
Важно! Закрытую колбу очень осторожно перекладывают в тёплое, тёмное место (24 градуса с плюсом). Через 2−3 недели материал будет готов для высаживания в специальную среду. Среда тоже легко готовится в домашних условиях. Это студенистое вещество, агар, получается из овса, моркови, картофеля. Такой агар стерилизуется и наливается в пробирку, а как остынет, туда закидывается кусочек гриба.
Среда тоже легко готовится в домашних условиях. Это студенистое вещество, агар, получается из овса, моркови, картофеля. Такой агар стерилизуется и наливается в пробирку, а как остынет, туда закидывается кусочек гриба.
Надо помнить! Весь процесс должен проходить в исключительной стерильности.
Культивирование промежуточного мицелия
Дальше происходит разведение самой грибницы. Качественные зёрна злаковых провариваются в воде около 15 минут, просушиваются и перемешиваются с углекислым кальцием и гипсом. После этого смесь засыпается в стеклянную посуды до 2/3 объёма и стерилизуется. Как остынет, добавляется кусочек маточного мицелия. За две недели при температуре от 0 до +20 он разрастется до нужных размеров.
Готовую грибницу можно хранить до трёх месяцев. Рекомендуется промежуточный материал хранить в герметичных пакетиках.
Выращивание посевного мицелия
Посевной материал разводится так же, как промежуточный, только в больших объёмах. Опять готовят ёмкости, например, пластиковые мешки с субстратом и в каждую добавляют немного промежуточного продукта. В пропорции на литровую посудину одна столовая ложка. Готовый мицелий также можно подсадить на пенёчки или валежник.
Урожай вешенки сильно зависит от того, как размножить мицелий вешенки, и качества субстрата. Рекомендуется материал для грунта хорошо пропарить в кипятке не менее двух часов и сильно отжать. Допустимая влажность субстрата 70%. Повышенная влажность недопустима.
Для организации производства грибов пойдёт теплица, сарай, гараж и даже балкон. Просто нужно создать оптимальные условия для успешного развития грибниц. Это постоянная влажность в пределах 85−90%, температура около 15−20 градусов, хорошая вентиляция и освещение 9 часов в сутки.
Методы разведения грибов
Вешенки — самые удачные в разведении грибы, обеспечивающие быстрое получение урожая. От посева до срезки первых грибов всего полтора месяца. С одного квадратного метра грибницы в месяц можно получить до десяти килограммов продукции.
Вырастить мицелий вешенки в домашних условиях можно применяя два основных метода:
- Экстенсивный. Это следование естественному развитию грибницы. То есть на больших участках создаётся природная атмосфера — с пнями и валежником. В пропилы на пнях помещают шляпки вешенки и мицелий. Но выход товарной продукции целиком зависит от погодных условий. Стабильного урожая планировать не приходится.
- Интенсивный. Этим методом выращивают грибы в специальных ёмкостях, к примеру, используют плотные пластиковые мешки. И это оправдано, легко исполнимо и дёшево. Где взять мицелий вешенки, тоже не проблема. Можно купить сертифицированный и вполне доступный по стоимости или сделать самостоятельно.
 Что тоже легко выполнимо.
Что тоже легко выполнимо.
Полезные советы
Хороший урожай грибов можно получить только от посева качественного мицелия. Чтобы добиться успехов в выведении мицелия и товарного разведения грибов, требуется соблюдение некоторых правил:
- Лучшим субстратом являются опилки лиственных пород деревьев.
- Опилки должны иметь белый либо желтоватый цвет.
- Запах основы субстрата должен быть свежим.
- При перевозках мицелия нужно поддерживать влажность 30−45%.
- Внутри грибных блоков тоже должны соблюдаться температурные нормы и влажность.
- Оптимальное количество вложения мицелия в один блок размером 35*75 — примерно 300 грамм.
- Весь цикл производства необходимо выполнять с соблюдением правил санитарии.
- Должна соблюдаться технология изготовления мицелия.
Занятие грибоводством — довольно хлопотное дело. Требует соблюдения определённых правил, много времени и усердия. Зато не требуется специального образования, дорогостоящего оборудования и материалов. Не требует постоянного присутствия и обслуживания. При этом гораздо выше вероятность получения качественного продукта.
Требует соблюдения определённых правил, много времени и усердия. Зато не требуется специального образования, дорогостоящего оборудования и материалов. Не требует постоянного присутствия и обслуживания. При этом гораздо выше вероятность получения качественного продукта.
Способы выращивания вешенки
Грибы вешенки известны как очень вкусные и полезные. Грибоводам-любителям советуют начинать разведение именно с них. Однако выращивание вешенки в домашних условиях требует соблюдения определенных правил.Способы выращивания
Вешенки — ценный и питательный продукт Вешенки быстро приносят плоды и они очень неприхотливы. Через 40 дней после посадки можно собирать первый урожай. С каждого «квадрата» земли обычно снимают около 10 кг грибов за 1 месяц. Вешенки дома выращивать не так уж сложно и дорого.
Грибы активно растут на твердой древесине, лузге подсолнечника, шелухе семян хлопчатника. Выращивание вешенки в домашних условиях началось сравнительно недавно. Вначале использовали экстенсивный способ. Для этого необходимо было распилить деревья на небольшие бруски, просверлить в них отверстия и поместить туда шляпки вешенок, а затем мицелий. Такое разведение грибов являлось полным подражанием природе. Подобный способ отлично подходит каждому, кто не располагает временем, которое можно уделить процессу выращивания.
Выращивание вешенки в домашних условиях началось сравнительно недавно. Вначале использовали экстенсивный способ. Для этого необходимо было распилить деревья на небольшие бруски, просверлить в них отверстия и поместить туда шляпки вешенок, а затем мицелий. Такое разведение грибов являлось полным подражанием природе. Подобный способ отлично подходит каждому, кто не располагает временем, которое можно уделить процессу выращивания.
Но так выращивать вешенки дома не рекомендуется, поскольку этот способ имеет ряд недостатков: зависимость от погоды может продлить процесс зарастания до 3 месяцев, что значительно снизит урожайность. Поэтому существуют более простые способы выращивания этих грибов дома.
Обработка субстрата
Для субстрата рекомендуется применять солому различных злаковых культур (ячмень или пшеница). Он обязан быть чистым и сухим, не иметь запахов и примесей. Солома подобных культур считается самым распространенным сырьем для выращивания вешенок.
Соломины необходимо выбирать не инфицированные, пористые и широкие. Их нужно измельчить или расплющить. Солому следует покупать у одного продавца. Если она свежая, имеет толстый налет воска, то ее необходимо замочить на 12 часов.
Дома часто используется гидротермическая обработка. Берется емкость большого объема, в нее утрамбовывается солома. Она заливается теплой водой, а затем подогревается до 70 градусов. При установившейся температуре субстрат необходимо продержать около 3 часов, затем слить воду. Далее субстрат достают, удаляя излишек воды. Когда его температура достигнет 25 градусов, можно перейти к посадке.
Солома остывает полчаса. За это время требуется подготовить мицелий, пакет из полиэтилена, место инокуляции. Субстрат высыпается на дно пакета, затем выкладывается слой мицелия. Процедура повторяется до полного заполнения пакета. Мицелия должно быть не более 5% от веса субстрата.
Иногда для того, чтобы вырастить вешенки, используют лузгу подсолнечника. Ее необходимо очень быстро нагреть до 90 градусов, выдержать не более 2-х часов. Затем слить воду, подождать, пока субстрат стечет (не более получаса), после чего провести инокуляцию.
Ее необходимо очень быстро нагреть до 90 градусов, выдержать не более 2-х часов. Затем слить воду, подождать, пока субстрат стечет (не более получаса), после чего провести инокуляцию.
Необходимо запомнить
В домашних условиях вырастить эти грибы не так уж сложно. При их разведении следует помнить о нескольких правилах. Во-первых, мицелий нужно рассеивать таким образом, чтобы 4/5 располагалось ближе к стенкам пакета. Во-вторых, количество слоев не должно быть меньше 12. Большее их число приведет к ускорению обрастанию субстрата мицелием.
После того, как закончена утрамбовка, необходимо оставить немного места для завязки. Блок (пакет, в котором есть мицелий и субстрат) необходимо оставить в темном месте с температурой 20°С. Если же температура увеличится более чем на 4°С, то мицелий может погибнуть (внутри субстрата температура может доходить до 35°С).
Если все выполнено правильно, то максимум через 16 дней блок будет похож на монолит белого цвета. Если некоторые места заражены, то общая урожайность будет ниже. Пока не появятся примордии, необходимо просто поддерживать нужную влажность, температуру, иногда можно опрыскивать блок.
Если некоторые места заражены, то общая урожайность будет ниже. Пока не появятся примордии, необходимо просто поддерживать нужную влажность, температуру, иногда можно опрыскивать блок.
В течение двух дней примордии становятся взрослыми грибами. В процессе их роста важно следить за вентиляцией в помещении. Поливать зачатки грибов не нужно, это может вызвать их гибель. Собирать урожай можно тогда, когда на шляпках на вершине сростка будут выровнены края.
Размножение грибов на примере вешенки и строфарии / Съедобные грибы, ягоды, травы
Выше было сказано, что объектом исследования является Вешенка обыкновенная — Pleurotus ostreatus (Fr.) Kummer.
Видовое описание Вешенки обыкновенной.
Надцарство: Эукариоты — Eucaryota.
Царство: Грибы — Fungi.
Отдел: Настоящие грибы — Eumycota.
Класс: Базидиальные — Basidiomycetes.
Порядок: Агариковые — Agaricales.
Семейство: Трихоломовые — Tricholomtaceae.
Род: Вешенка — Pleurotus.
Вид: Вешенка обыкновенная — Pleurotus ostreatus.
• Шляпка 3-17 см., выпуклая или широковоронковидная, часто эксцентрическая, в начале темно-
бурая, затем грязножелтовато-серая, гладкая.
• Мякоть хорошо развитая, белая, вначале мягкая, затем жестковатая, особенно в ножке, без
особого запаха и вкуса.
• Пластинки нисходящие, белые, чистые, с перемычками.
• Ножка 1- 4 х 1-3 см., цилиндрическая, сплошная, волосисто-опушенная, белая или буроватая,
иногда отсутствует.
• Споры 8 -12 х 3 — 4 мкм, вытянуты — эллипсоидальные или палочковидно-цилиндрические,
гладкие, бесцветные.
Видовое описание строфарии кубенсис. Stropharia cubensis.
Надцарство: Эукариоты – Eucaryota. Царство: Грибы – Fungi. Отдел: Настоящие грибы – Eumycota.
Класс – Базидиомицеты.
Порядок – Агариковые или пластинчатые.
Семейство – Strophariasea.
Род – Строфария.
Вид — Stropharia cubensis Earle.
Возможные синонимы: Psilocybe cubensis (Earle) Singer, Psilocybe cubensis var. caerulescens (Murr.)
Singer et Smit, Stropharia cuanensis Murr. , Stropharia caerulescens (Pat) Sing., «Golden Tops», «Cubies»,
, Stropharia caerulescens (Pat) Sing., «Golden Tops», «Cubies»,
«San Isidros», «Hongos Kentesh».
Дополнение. Не следует путать строфарию с грибами из рода псилоцибов.
Род Псилоцибе – это самостоятельный род в общем семействе строфариевых.
Вид – Псил. Семиланцеата, Псил. Мексикана, и др. А например, Панеолус относится уже к Семейству Копринацеа (навозниковые), Роду Панеолус. Таким образом, правильнее называть Строфарию кубенсис именно строфария, а не псилоцибе. А произрастающую в умеренных широтах псилоцибе семиланцеата (полуланцетовидную) называть именно псилоцибе, как и псилоцибе мексикана по ряду признаков, таких как отсутствие вторичной оболочки на ножке у псилоцибов, откуда собственно и пошло название «строфария» — перевязь, и некоторых других отличий.
Местообитание: Повсеместно в субтропических регионах, неизвестен в тропиках (там встречается субкубенсис, отличающийся чуть меньшими размерами спор и плодов, но с таким же набором химических составляющих – вид Эквадор). Известен в Центральной Америке, юге США (во Флориде, в Штате Техас, и Север Джорджии), Кубе, Мексике, Гватемале, Южной Америке, Вьетнаму, Камбодже, Таиланде, Малайзии, Индии, и Австралии, Гондурасе. Растет преимущественно на коровьем навозе. Также на богатой почве, на пастбищах и лугах, по обочинам в навозных кучах. У нас выращивается искусственно в домашних условиях на субстрате культуры.
Известен в Центральной Америке, юге США (во Флориде, в Штате Техас, и Север Джорджии), Кубе, Мексике, Гватемале, Южной Америке, Вьетнаму, Камбодже, Таиланде, Малайзии, Индии, и Австралии, Гондурасе. Растет преимущественно на коровьем навозе. Также на богатой почве, на пастбищах и лугах, по обочинам в навозных кучах. У нас выращивается искусственно в домашних условиях на субстрате культуры.
• Шляпка
Размеры: (10-) 25-70 (-85) мм диаметр.
Цвет: бледно — желтоватый, более темный в центре, в старости коричневатый.
Форма: сначала конусооборазная, затем в старости в форме колокола, в конце выпуклая (конец
загнут вверх).
Поверхность: грязная, гладкая. Мякоть прочная, беловатая, синеет при повреждении.
• Hожка
Размеры: (40-) 70-120 (-170) мм длиной, (4-) 8-13 (-16) мм в диаметре.
Форма: равномерно толстая, в основании сильнее, полая.
Цвет: беловатый к сливочно — белому или желто — коричневому в старости, при повреждении голубеет, сухое, гладкое, белое кольцо (остатки Velum partiale), окрашенное темно
коричневыми спорами. Синеет при повреждении.
Синеет при повреждении.
• Спороносный слой
Цвет: вначале — от серого до серо – фиолетового при созревании, иногда пятнистый с
беловатыми краями.
Расположение: от adnat до sinuat.
• Споры: Споры темно — коричневые, с фиолетовым налетом (пурпурно – коричневые), (12-)
13.2-15.4 (-17.6) x 7.7-9.9 (-11) x 7-8.8 микрон, от эллиптической до овальной формы,
толстостенные.
Доза: 1 или 2 больших свежих гриба, весящих приблизительно 30 гр. или от 10 до 40 грибов, весящих по 1 грамму, это средняя доза, от трех до пяти грамм сухих, эквивалентно.
Грибы и растения имеют следующие сходства — поступление питательных веществ в клетку, основанное, главным образом, на явлениях осмоса (диффузии веществ через полупроницаемые перегородки поверхности клеток), не является чисто физическим, но является физиологическим явлением. При поступлении питательных веществ в клетку гриба, клетка играет роль активную, а не пассивную, так как проницаемость протоплазмы, от которой она зависит, является величиной переменной. Кроме того, существует избирательная проницаемость для определенных веществ и при том различная в разном состоянии клеток организма. Отсюда появляется возможность применения сходным образом некоторых стимуляторов, например гетероауксина и эпина для грибов.
Кроме того, существует избирательная проницаемость для определенных веществ и при том различная в разном состоянии клеток организма. Отсюда появляется возможность применения сходным образом некоторых стимуляторов, например гетероауксина и эпина для грибов.
Дикариотная грибница способна на неограниченный рост — вегетативное тело грибов состоит из гиф имеющих вид цилиндрических трубок до 10 мкм в диаметре, они характеризуются верхушечным (апикальным) и неограниченным ростом и обильным ветвлением.
Отсутствие большей частью подвижности в вегетативном состоянии у высших растений тканевое строение возникает при делении клеток во всех направлениях. А у грибов мицелий делится только с образованием поперечных направлений, т.е. только в одном направлении. Поэтому принято считать, что у грибов нет настоящих тканей, а есть лишь ложные ткани. В зависимости от морфологических особенностей у грибов различают два типа тканей: параплектенхиму и прозоплектенхиму. Кроме морфологического понятия существует и физиологическое понятие ткани у грибов. С точки зрения функционального назначения различают покровные, механические и проводящие ткани. Из покровной ткани состоит поверхность склероциев и плодовых тел высших грибов. Клетки такой ткани имеют утолщенные оболочки, на поверхности откладывается пигмент, поглощающий лучи солнечного спектра, тем самым выполняющий защитную роль. Механическая ткань представлена гифами сильно утолщенными стенками и суженым просветом, которые придают прочность плодовому телу или какой-либо его части. Типичной проводящей ткани у грибов нет, его функции выполняют особые специализированные гифы лишенные поперечных перегородок. Эти гифы, пронизывая плодовое тело в разных направлениях, снабжают его водой. Для продвижения органических веществ имеются гифы, являющиеся ответвлениями обычных гиф. Они отличаются густым окрашенным содержимым. Все перечисленное — т.е. функциональное сходство тканей высших растений и специализированных гиф грибов говорит об еще одном сходстве.
С точки зрения функционального назначения различают покровные, механические и проводящие ткани. Из покровной ткани состоит поверхность склероциев и плодовых тел высших грибов. Клетки такой ткани имеют утолщенные оболочки, на поверхности откладывается пигмент, поглощающий лучи солнечного спектра, тем самым выполняющий защитную роль. Механическая ткань представлена гифами сильно утолщенными стенками и суженым просветом, которые придают прочность плодовому телу или какой-либо его части. Типичной проводящей ткани у грибов нет, его функции выполняют особые специализированные гифы лишенные поперечных перегородок. Эти гифы, пронизывая плодовое тело в разных направлениях, снабжают его водой. Для продвижения органических веществ имеются гифы, являющиеся ответвлениями обычных гиф. Они отличаются густым окрашенным содержимым. Все перечисленное — т.е. функциональное сходство тканей высших растений и специализированных гиф грибов говорит об еще одном сходстве.
Вегетативное размножение — вегетативное размножение осуществляется фрагментами мицелия, которые, отделяясь, дают начало новому мицелию. У агариковых известно вегетативное размножение путем почкования мицелия или его клеток, в результате чего образуются отдельные клетки — оидии, дающие начало новому грибному организму.
Съедобные грибы характеризуются заметным количеством минеральных веществ, содержание которых у отдельных видов может достигать 11,5% (в среднем 7,7%). Плодовые тела грибов богаты калием, фосфором, в незначительных количествах содержится в них натрий и кальций, содержание железа у макромицетов приблизительно аналогично тем количествам его, которое обнаруживают в большинстве растительных продуктов.
Вешенка королевская
Описание:
Описание.
Нежный гриб с мясистой, плотной мякотью и приятным, тонким ароматом. Растет большими группами с мая по октябрь на влажных пнях, стволах засохших или ослабленных лиственных деревьев. Ее можно жарить, варить, солить и мариновать. По своей пищевой ценности вешенка опережает не только овощи, но и мясо. Лучше всего употреблять в пищу молодые грибы или только шляпки зрелых грибов. Вешенка королевская или степная, «Боровик древесный», степной «белый гриб». Произрастает в сухих степях. Отличается мясистой ножкой, хрящеватой структурой, а не волокнистой как у других вешенок. В гастрономическом плане ценится как самая вкусная из вешенок.
По своей пищевой ценности вешенка опережает не только овощи, но и мясо. Лучше всего употреблять в пищу молодые грибы или только шляпки зрелых грибов. Вешенка королевская или степная, «Боровик древесный», степной «белый гриб». Произрастает в сухих степях. Отличается мясистой ножкой, хрящеватой структурой, а не волокнистой как у других вешенок. В гастрономическом плане ценится как самая вкусная из вешенок.
Советы по разведению.
Необходимо: 1. Бревно или палка лиственных пород (бук, граб, ольха, осина, клен, береза, тополь, ива, каштан, дуб) без признаков гнили, не свежее 1 месяца после рубки Влажность древесины должна быть не менее 50-60%. Диаметр – 20-50 см, длина 30-50 см, с корой (без веток). 2. Дрель. 3. Стерильные перчатки. 4. Полиэтилен. 5. Древесная зола.
Выращивание и уход.
В саду: посев производится с апреля по август включительно.
I этап. 1. Лучше использовать здоровую древесину с высокой влажностью. Перед применением замочить в воде в течение 2-3 дней. Избыток воды должен стечь, полностью пропитанная водой древесина должна сначала полежать несколько дней в отапливаемом подвале или на брезенте под солнцем. 2. В подготовленном бревне просверлить отверстия диаметром 0,8 см и длиной 4 см в шахматном порядке на расстоянии около 10 см друг от друга. 3. Надеть стерильные перчатки или протереть руки спиртом. Вставить грибные палочки в отверстия до упора. 4. Обернуть древесину в полиэтиленовую пленку, сделав небольшие отверстия для воздуха для сохранения влажности бревна. 5. Поместить бревно в темное влажное помещение и оставить обрастать мицелием. При t = 20 -25 ˚С оброст бревна – 2-3 месяца, при t = 14 ˚С – 5 месяцев. При температуре выше 34 ˚С мицелий может погибнуть. Бревна заросли, если в местах заражения и на торцах виден белый мицелий.
Перед применением замочить в воде в течение 2-3 дней. Избыток воды должен стечь, полностью пропитанная водой древесина должна сначала полежать несколько дней в отапливаемом подвале или на брезенте под солнцем. 2. В подготовленном бревне просверлить отверстия диаметром 0,8 см и длиной 4 см в шахматном порядке на расстоянии около 10 см друг от друга. 3. Надеть стерильные перчатки или протереть руки спиртом. Вставить грибные палочки в отверстия до упора. 4. Обернуть древесину в полиэтиленовую пленку, сделав небольшие отверстия для воздуха для сохранения влажности бревна. 5. Поместить бревно в темное влажное помещение и оставить обрастать мицелием. При t = 20 -25 ˚С оброст бревна – 2-3 месяца, при t = 14 ˚С – 5 месяцев. При температуре выше 34 ˚С мицелий может погибнуть. Бревна заросли, если в местах заражения и на торцах виден белый мицелий.
II этап. 1. В затененном и защищенном от ветра месте в саду вырыть лунку глубиной 10-15 см, дно лунки увлажнить. (Можно выращивать на балконе, посадив древесину после зароста в кадку с землей). 2. Обросшую грибницей древесину закопать горизонтально на глубину до 50% их толщины. Обсыпать почву вокруг бревна древесной золой (для борьбы с улитками). Оптимальная температура для образования плодовых тел – от 10 до 15 ˚С. 3. В сухую погоду поливать почву вокруг древесины ежедневно в течение 2-3 недель. 4. В зимний период бревно не выкапывать – просто присыпать листьями. Первый урожай при выращивании на мягкой древесине (береза, тополь, ива, липа) — через 3 месяца, на твердой (бук, дуб, ясень, клен) – через 6 месяцев. Плодоношение волнами до 5 лет на мягкой древесине, до 8 лет — на твердой. Урожайность — от 20 до 50% от веса бревна.
2. Обросшую грибницей древесину закопать горизонтально на глубину до 50% их толщины. Обсыпать почву вокруг бревна древесной золой (для борьбы с улитками). Оптимальная температура для образования плодовых тел – от 10 до 15 ˚С. 3. В сухую погоду поливать почву вокруг древесины ежедневно в течение 2-3 недель. 4. В зимний период бревно не выкапывать – просто присыпать листьями. Первый урожай при выращивании на мягкой древесине (береза, тополь, ива, липа) — через 3 месяца, на твердой (бук, дуб, ясень, клен) – через 6 месяцев. Плодоношение волнами до 5 лет на мягкой древесине, до 8 лет — на твердой. Урожайность — от 20 до 50% от веса бревна.
Категория: Мицелий Грибов
Пчелы, вешенки, бобы: ради чего люди подают заявки на «дальневосточный гектар» — Экономика и бизнес
МОСКВА, 1 июня. /ТАСС/. На Сахалине в первые часы действия закона были поданы четыре заявки на получение земли в Тымовском районе, который определен как пилотный по предоставлению «дальневосточного гектара». Об этом сообщила ТАСС начальник отдела земельных отношений администрации Тымовского района области Надежда Мосевнина.
Об этом сообщила ТАСС начальник отдела земельных отношений администрации Тымовского района области Надежда Мосевнина.
«Один заявитель берет на свою семью 4 гектара (закон допускает получение 1 гектара на каждого члена семьи — прим. ТАСС). Они планируют использовать их под сенокошение. Еще один заявитель — молодой парень со своей мамой. Они хотят открыть турбазу в районе верхнего Армудана. Следующий заявитель будет использовать участок по выращивание грибов, и еще один — под выпас крупнорогатого скота», — рассказала Мосевнина.
Сахалин обеспечат вешенками и шампиньонами
Как рассказал ТАСС один из заявителей Александр Тырцев, он планирует организовать на своем участке крестьянско-фермерское хозяйство «Восход». «Землю оформил в экологически чистом районе. Я занимаюсь выращиванием грибов вешенок, поставляю их в центральную часть Сахалина. Моя продукция востребована и на юге. Гектар позволит мне расширить производство», — сказал молодой предприниматель.
На эту тему
По его словам, сейчас он производит 400-500 кг грибов, новый цех позволит выращивать 4 тонны в месяц. «Думаю, что осенью мы уже сможем обеспечить поставки на юг Сахалина. Кроме того, планирую заняться и выращиванием шампиньонов», — заявил Тырцев.
«Думаю, что осенью мы уже сможем обеспечить поставки на юг Сахалина. Кроме того, планирую заняться и выращиванием шампиньонов», — заявил Тырцев.
В правительстве Сахалинской области ТАСС сообщили, что власти помогут сахалинцам осваивать дальневосточные гектары. «Безусловно, мы будем оказывать всестороннюю помощь и тем, кто захочет получить один гектар земли для ее обработки или обустройства под различные виды деятельности. Они могут быть разнообразными. Главное, чтобы это приносило пользу ее обладателю и региону. Надеюсь, что многие сахалинцы воспользуются этим правом», — сказал губернатор региона Олег Кожемяко.
Готовились заранее
В Октябрьском районе Еврейской автономной области первой оформила заявку на получение «дальневосточного гектара» глава крестьянско-фермерского хозяйства Тамара Юрченко.
»Я заранее подготовилась к выдаче «дальневосточного» гектара, это хорошая возможность для расширения посевных площадей, на которых выращиваю зерновые и бобовые культуры. Поэтому и расположение участка выбирала таким образом, чтобы оно было выгодно для нашего крестьянско-фермерского хозяйства», — сказала ТАСС Юрченко.
Поэтому и расположение участка выбирала таким образом, чтобы оно было выгодно для нашего крестьянско-фермерского хозяйства», — сказала ТАСС Юрченко.
«Тамара Демьяновна предоставила сразу все необходимые документы, в том числе схему расположения выбранного земельного участка», — рассказали ТАСС в департаменте пресс-службы правительства и губернатора региона.
По данным председателя комитета по управлению имуществом Октябрьского муниципального района Виктории Смирновой, в первой половине дня 1 июня за консультацией и разъяснениями в районную администрацию обратились четыре жителя разных населенных пунктов, в том числе один из города Биробиджана. Их интерес к получению одного гектара земли связан с ведением личного подсобного хозяйства. «Людям важно знать все тонкости этой новой и интересной процедуры получения бесплатной земли, и они ответственно к этому относятся», — привели в пресс-службе облправительства слова Смирновой.
Приморье: оформление в ручном режиме
Жители Приморья с момента вступления с 1 июня в силу закона о «дальневосточном гектаре» подали 11 заявок на предоставление участков в Ханкайском районе, земли они планируют использовать для разведения пчел и выпаса скота. Об этом сообщили в среду корреспонденту ТАСС в отделении градостроительства Ханкайского района.
«У нас взяли уже 11 участков, пришли люди, живущие рядом, и взяли земли одним массивом. Участки берут под сельское хозяйство: пчеловодство, сенокос, выпас скота», — сказал собеседник агентства.
Представитель администрации добавил, что с утра в администрации наблюдаются сбои в работе электронной системы по выбору участков, поэтому пока власти очерчивают участки на карте и выдают заявителям бумажные договоры. Когда специалисты наладят работу системы, все данные перенесут в нее.
Пилотные территории
С 1 июня вступил в силу закон о «дальневосточном гектаре», который подразумевает получение гражданами РФ бесплатно участка площадью в размере 1 га на территории Дальнего Востока.
Закон будет вступать в силу поэтапно. Первыми право на выбор земельного участка получили жители девяти муниципальных районов (по одному из каждого субъекта в ДВФО), выбранного в качестве «пилотного» региона, в этих же районах в первую очередь и будет выделяться земля. С 1 октября право оставить заявку на «дальневосточный гектар» будет распространено на всех жителей Дальнего Востока, и только с 1 февраля 2017 года — на жителей других регионов России.
С 1 октября право оставить заявку на «дальневосточный гектар» будет распространено на всех жителей Дальнего Востока, и только с 1 февраля 2017 года — на жителей других регионов России.
Перспективы «дальневосточного гектара»
Закон о «дальневосточном гектаре» имеет хорошие перспективы. Об этом свидетельствует опыт Амурской области, которая начала осуществлять свою программу бесплатной раздачи земли раньше всех других регионов. В регионе еще в 2015 году был принят местный закон, согласно которому, любой житель области может получить до 2,5 гектара для ведения личного подсобного хозяйства можно получить и до 20 гектаров для крестьянско-фермерского хозяйства.
На эту тему
С марта 2015 года, когда закон вступил в силу было удовлетворено 106 заявок, из них три — 1 июня. Сегодня сертификаты на землю получили три человека, которые намерены использовать участки для разведения пчел, сообщил ТАСС главный специалист отдела по управлению муниципальным имуществом администрации Архаринского района Амурской области Эдуард Чеушев.
«Мой участок расположен в лесу на берегу реки Архара возле заброшенной деревни Татакан. Там я планирую заняться пчеловодством, почти все для этого уже готово», — сообщил корр. ТАСС один из обладателей сертификата Вадим Островерх. Он добавил, что фермерских хозяйством занимается с 2007 года, и у него уже 420 гектаров земли, на которых он выращивает сою и гречиху.
А первые полноправные владельцы земли, оформленной именно по закону о «дальневостоном гектаре» могут появиться на Дальнем Востоке к концу июля, сообщал ранее заместитель министра по развитию Дальнего Востока Кирилл Степанов на круглом столе в ТАСС.
По словам Степанова, уполномоченный орган в регионе рассматривает заявление на получение участка в течение 20 дней и в случае положительного решения направляет заявителю договор о безвозмездном пользование гектаром. «У гражданина есть 30 дней, чтобы его подписать. Таким образом первые пользователи дальневосточным гектаром могут появится уже к концу июля 2016 года», — отметил замминистра.
Генетическое улучшение Pleurotus (вешенка): обзор
3 Биотехнология. 2019 сен; 9 (9): 322.
, , 1 , 1 , 1 , , 1 , 1 , 1 и 2Anupam Barh
1 ICAR-Dipartment Meходяhroom Research, Solan , Химачал Pradesh India
VP Sharma
1 ICAR-управление Грибные исследования, Solan, Himachal Pradesh India
Sudheer Kumar Annepu
1 ICAR-Dipartment из грибных исследований, Solan, Himachal Pradesh India
Shwet Kamal
1
1 ICAR-управление Грибные исследования, Солн, Гимачал Прадеш Индия
Швета Sharma
1 ICAR-управление Грибные исследования, Solan, Himachal Pradesh India
Pankaj Bhatt
2 отдел Микробиология, Дельфин (П.G) Институт биомедицинских и естественных наук, Дехрадун, Уттаракханд, Индия
1 ICAR-Директорат исследований грибов, Солан, Химачал-Прадеш, Индия
2 Департамент микробиологии, Дельфин (PG) Институт биомедицинских и естественных наук, Дехрадун, Уттаракханд, Индия
Автор, ответственный за переписку.
Поступила в редакцию 20 августа 2018 г.; Принято 29 июля 2019 г.
Copyright © King Abdulaziz City for Science and Technology 2019Эта статья была процитирована другими статьями в PMC.Abstract
Pleurotus — важный род, включающий несколько съедобных видов, имеющих большое коммерческое значение. Эти виды выращивают по всему миру. Районы производства Pleurotus в основном относятся к азиатской части и приобретают широкую популярность во всем мире благодаря их многообещающим преимуществам в питании. Спрос на улучшенные сорта с высокой продуктивностью также растет. Генетическое улучшение Pleurotus началось с простой техники селекции, которая позже использовала гибридизацию (внутривидовую, межвидовую и межродовую) и мутационную селекцию.Такие признаки, как продуктивность, отсутствие спор и улучшение качества, являются важными задачами, над которыми до сих пор было выполнено большинство работ. Однако подходы нового поколения, такие как молекулярное размножение, генетическая трансформация и методы редактирования генома, также добавили темпа нынешнему процессу совершенствования. К настоящему времени было секвенировано семь видов Pleurotus , и получен значительный объем данных, которые можно использовать в дальнейших программах разведения. В этой статье обсуждаются и обобщаются различные результаты исследований по генетическому улучшению Pleurotus , а также даются перспективы будущих программ разведения.
К настоящему времени было секвенировано семь видов Pleurotus , и получен значительный объем данных, которые можно использовать в дальнейших программах разведения. В этой статье обсуждаются и обобщаются различные результаты исследований по генетическому улучшению Pleurotus , а также даются перспективы будущих программ разведения.
Ключевые слова: Pleurotus селекция, Бесспорность, Молекулярная селекция, Улучшение признаков
Введение
Грибы являются относительно новыми для пищевых привычек и являются ценными культурами. Потребительский спрос на грибы заметно вырос в последние годы, и этот рост более заметен в отношении специальных грибов, таких как Pleurotus spp. В роде Pleurotus культивируется больше видов, чем в любых других родах агариков (Singh and Kamal 2017).Род Pleurotus, известный как вешенка , относится к классу Basidiomycota и семейству Pleurotaceae. Pleurotus является вторым по величине выращиваемым грибом в мире после шиитаке (Royse et al. 2017). Тенденции производства Pleurotus , описанные Royse et al. 2017 год показал, что только Китай обеспечивает 87% производства, в то время как остальной мир производит всего 13%. В питательном отношении вешенки богаты белками, минералами, витаминами и клетчаткой с меньшей калорийностью (Gupta et al.2011). Вначале генетическое улучшение Pleurotus было достигнуто за счет прямого отбора из зародышевой плазмы, собранной во время набегов грибов, а позже были использованы более систематические методы селекции. Вид Pleurotus является гетероталличным по своей природе (Larraya et al. 1999) и, следовательно, требует двух разных совместимых типов спаривания для начала репродуктивной фазы (Roach et al. 2014). Если сравнивать систему спаривания растений с грибами, то гетероталлизм весьма похож на аллогамный характер, а гомоталлический — на автогамный механизм.Будучи гетероталличным грибом, вешенка демонстрирует огромное разнообразие. Существует огромное разнообразие штаммов и видов Pleurotus в Индии, и до 2017 года было зарегистрировано 26 таксонов (Upadhyay et al.
2017). Тенденции производства Pleurotus , описанные Royse et al. 2017 год показал, что только Китай обеспечивает 87% производства, в то время как остальной мир производит всего 13%. В питательном отношении вешенки богаты белками, минералами, витаминами и клетчаткой с меньшей калорийностью (Gupta et al.2011). Вначале генетическое улучшение Pleurotus было достигнуто за счет прямого отбора из зародышевой плазмы, собранной во время набегов грибов, а позже были использованы более систематические методы селекции. Вид Pleurotus является гетероталличным по своей природе (Larraya et al. 1999) и, следовательно, требует двух разных совместимых типов спаривания для начала репродуктивной фазы (Roach et al. 2014). Если сравнивать систему спаривания растений с грибами, то гетероталлизм весьма похож на аллогамный характер, а гомоталлический — на автогамный механизм.Будучи гетероталличным грибом, вешенка демонстрирует огромное разнообразие. Существует огромное разнообразие штаммов и видов Pleurotus в Индии, и до 2017 года было зарегистрировано 26 таксонов (Upadhyay et al. 2017). Из-за разнообразия видов разнообразия и напряжения ( Pleurotus eryngii , Pleurotus Ostreatus , Pleurotus Plusmanarius , PLEUROTUS CITRINOPILEATUS PREUROTUS CITRINOPILEATUS и PLEUROTUS Djamor ) можно развить определенные штаммы региона, используя простую гибридизацию /спаривание.Хотя цели селекции вешенки варьируются в зависимости от географических и временных вариаций, более высокая продуктивность, качество плодовых тел, отсутствие спор, устойчивость/толерантность к биотическим и абиотическим стрессам, а также лучший срок хранения и т. д. являются одними из общих целей селекции. Для достижения этих целей применяются различные селекционные подходы, включающие селекцию, гибридизацию, мутационную селекцию, молекулярную селекцию и генетическую трансформацию. Настоящий обзор охватывает эти подходы.
2017). Из-за разнообразия видов разнообразия и напряжения ( Pleurotus eryngii , Pleurotus Ostreatus , Pleurotus Plusmanarius , PLEUROTUS CITRINOPILEATUS PREUROTUS CITRINOPILEATUS и PLEUROTUS Djamor ) можно развить определенные штаммы региона, используя простую гибридизацию /спаривание.Хотя цели селекции вешенки варьируются в зависимости от географических и временных вариаций, более высокая продуктивность, качество плодовых тел, отсутствие спор, устойчивость/толерантность к биотическим и абиотическим стрессам, а также лучший срок хранения и т. д. являются одними из общих целей селекции. Для достижения этих целей применяются различные селекционные подходы, включающие селекцию, гибридизацию, мутационную селекцию, молекулярную селекцию и генетическую трансформацию. Настоящий обзор охватывает эти подходы.
В настоящем обзоре информация о размножении и генетическом улучшении Pleurotus была собрана из различных научных баз данных, включая Elsevier, Google Scholar, PubMed, Springer и т. д., а также связанной литературы. В обзоре основное внимание уделяется методам, механизму и ограничениям генетического улучшения.
д., а также связанной литературы. В обзоре основное внимание уделяется методам, механизму и ограничениям генетического улучшения.
Жизненный цикл и генетические исследования
Pleurotus Методы селекции связаны с жизненным циклом организма.Как обсуждалось ранее, Pleurotus является гетероталлическим гомобазидиомицетом. Спаривание контролируется двухфакторной тетраполярной генетической системой. Жизненный цикл гриба начинается с прорастания гаплоидных базидиоспор. Проросшие базидиоспоры развиваются в гаплоидный мицелий. Два совместимых гаплоидных мицелия сливаются (анастомоз) и образуют дикариотический мицелий, имеющий два неслитых ядра. Кариогамия, т. е. слияние двух гаплоидных ядер, происходит у базидия в плодовом теле (базидиокарпе).Это дает начало четырем гаплоидным базидиоспорам, которые снова вступают в тот же самый цикл (Larraya et al. 1999) (рис. ). Как и у большинства базидиомицетов, у монокариотических гиф отсутствуют зажимные соединения. Дикариотический мицелий можно легко отличить по наличию зажимных соединений (Bhandal and Mehta 1994).
Методы селекции грибов
Pleurotus видовПри улучшении сельскохозяйственных культур селекционные подходы направлены на выявление вариаций тремя основными методами. Это рекомбинантная селекция, трансгенная селекция и мутационная селекция (Shu and Lagoda 2007).Рекомбинационная селекция включает в себя создание новых сортов и штаммов с помощью традиционных подходов к селекции, таких как селекция и гибридизация/скрещивание. При улучшении гриба Pleurotus в первую очередь используется селекция. Отбор может быть прямым отбором из зародышевой плазмы, собранной во время набегов грибов, или из культур, полученных путем прорастания множества спор. Отбор и спаривание генетически разных родителей — еще один подход к использованию гетерозиса посредством гибридизации.
Отбор мультиспор
Многочисленные споры, собранные с отобранных плодовых тел, проращивают в чашках с питательной средой, которые в конечном итоге переплетаются.В этом процессе дикариотический мицелий отбирается путем естественного отбора. Согласно отчету, опубликованному на Pleurotus eryngii , новые разновидности обычно создаются путем скрининга мультиспоровых культур (Sonnenberg et al. 2016).
Согласно отчету, опубликованному на Pleurotus eryngii , новые разновидности обычно создаются путем скрининга мультиспоровых культур (Sonnenberg et al. 2016).
Отбор родителей и гибридизация (двухточечный метод/метод двойного культивирования)
Vandendries (1933) был первым, кто обнаружил двухфакторный гетероталлизм у P. ostreatus с помощью анализа формирования зажимов. У Pleurotus генетическое содержание штаммов определяет продуктивность и качество урожая (Kaur and Sodhi 2012).Генетическое улучшение любого признака путем селекции в основном достигается за счет гибридизации и фенотипического отбора по урожайности и качеству грибов. Концепция гибридизации грибов является относительно новой для селекционеров, поскольку она приобрела большую популярность только после 1983 г. (Zhou 2017). Желаемые признаки могут быть переданы агрономически адаптируемому штамму путем гибридизации. Гибридизацию Pleurotus можно провести тремя методами: (а) внутривидовая гибридизация, (б) межвидовая гибридизация, (в) межродовая гибридизация. Внутри- и межвидовая гибридизация обычно проводится с использованием метода двойной культуры (Kumara and Edirimanna 2009). Активно растущий мицелий культур отдельных спор держат на расстоянии около 1 см от центра чашки Петри на среде, а именно на картофельно-декстрозном агаре/агаре с солодовым экстрактом и т. д. Слитые мицелии, показывающие обильный рост гиф в точке контакта, берут и переносят на новые чашки Петри и проверяют на наличие зажимных соединений.
Внутри- и межвидовая гибридизация обычно проводится с использованием метода двойной культуры (Kumara and Edirimanna 2009). Активно растущий мицелий культур отдельных спор держат на расстоянии около 1 см от центра чашки Петри на среде, а именно на картофельно-декстрозном агаре/агаре с солодовым экстрактом и т. д. Слитые мицелии, показывающие обильный рост гиф в точке контакта, берут и переносят на новые чашки Петри и проверяют на наличие зажимных соединений.
Внутривидовая гибридизация
Спаривание между совместимыми монокарионами из разных штаммов одного и того же вида, которые скрещиваются с образованием дикариона, называется внутривидовой гибридизацией, также называемой мон-мон или моно-моногибридизацией.Из-за существования множественных факторов аллелизма и несовместимости монокариотический мицелий P. ostreatus , полученный из разных плодовых тел (представляющих разные штаммы, собранные из разных мест или хозяев), скрещивался со 100% процентом по сравнению с возможностью инбридинга всего 25%. (Бресински и др., 1987).
(Бресински и др., 1987).
Дикариотизация, т. е. превращение гомокариона в дикарион, может происходить либо путем слияния с совместимым гомокарионом, либо путем слияния монокариона с другим дикариотическим мицелием.Гибридизация, которая происходит между дикарионами и монокарионами, независимо от типа спаривания, называется спариванием димонов (Chang 1992). Этот простой подход также можно использовать для гибридизации.
Выбор различных родителей, производящих базидиоспоры, является ключом к успешной гибридизации. Кроме того, отбор изолятов с одной спорой (SSI) также является еще одним критерием для некоторых экономически важных признаков, таких как урожайность. Было обнаружено, что у Agaricus bisporus вертикальный рост в пробирке с SSI связан с урожайностью (Singh and Kamal 2017).Многие рабочие разработали внутривидовые гибриды, используя двойную культуру и слияние протопластов (таблица).
Таблица 1
Исследования по внутривидовой гибридизации у Pleurotus
Sl. нет. нет. | Родительские виды | Кресты получил | Результаты | Рекомендации | Ссылки | Семь изолятов были получены от слияния с разной скоростью роста | Тойомасу и Мори (1987) |
|---|---|---|---|---|---|---|
| 2 | Pleurotus ostreatus | Гибридизация протоклонов бесспорового штамма и коммерческого штамма | Исследование показало, что бесспоровый признак является рецессивным | Baars et al. (2000) (2000) | ||
| 3 | Pleurotus eryngii | Спаривание Di-mon было проведено между 22 дикарионами и 47 монокарионами | Семь скрещиваний были отобраны на основе показателей урожайности | Pyung-Gyun et al. (2004) | ||
| 4 | Pleurotus ostreatus | В ходе исследования было получено 27 гибридов | Было идентифицировано пять штаммов, монокарионы пушистого мицелия оказались несовместимыми | Goltapeh et al.(2007) | ||
| 5 | Pleurotus ostreatus | Скрещивание 12 отдельных спор привело к получению 16 гибридных штаммов | Были идентифицированы штаммы с высокой биологической эффективностью и производительностью, подходящие для тропических условий florida | Было выделено 49 монокарионов, и из 356 скрещиваний 5 оказались совместимыми | Результаты показали, что внутригибридизация может изменять фенотипическое выражение признаков | Kaur et al. (2008) (2008) |
| 7 | Pleurotus eryngii | Моно-моно-скрещивание было проведено между двумя монокариотическими штаммами | Полученный гибрид имел более длительный срок хранения, чем 67,5 дней в холодильной камере при 4 °C | Kim et al. (2011) | ||
| 8 | Pleurotus ostreatus | В ходе исследования скрещивание производилось по методу Di-mon, и был выведен новый сорт Hwaseong 5ho | Урожайность оказалась выше, чем у контрольного штамма | Lee et al.(2013) | ||
| 9 | Pleurotus eryngii | Этот сорт был выведен для устойчивости к высоким температурам, т. е. к 20 °C. В исследовании скрещивали монокарионы родителей Da (Ga5Na5-4 × KNR2312-7) и KNR2322 е. к 20 °C. В исследовании скрещивали монокарионы родителей Da (Ga5Na5-4 × KNR2312-7) и KNR2322 | . Выведенным сортом в исследовании был Taeyangsongi. Качество оказалось лучше, чем у эталонного сорта при 20 °C | Im et al. (2014) | ||
| 10 | Pleurotus eryngii | Исследование было проведено для создания сорта с несколькими плодовыми телами на бутылку.Использованными родителями были E12-176 и aerini № 3 | Выведенный штамм Saegonji имел меньшие плодовые тела и большую длину плодов, чем эталонный штамм | Ha et al. (2014) | ||
| 11 | Pleurotus eryngii var. ferulae ferulae | Di-mon Скрещивание монокариотического штамма ASI 2850-24 и дикариотического штамма ASI 2803 | Выведенный штамм Beesan No.1 показал раннее начало плодоношения с толстой ножкой и высокое качество по сравнению с другими сортами | Shin et al.(2014a) | ||
| 12 | Pleurotus eryngii var . ferulae | В дополнение к вышеуказанному исследованию было проведено скрещивание Di-mon монокариотического штамма ASI 2798-24 и дикариотического штамма ASI 2803, и был выведен Beesan No. ниже, чем у Beesan № 1 | Shin et al. (2014b) | |||
| 13 | Pleurotus eryngii var . tuoliensis tuoliensis | Изофермент эстеразы и индукция примордиев изучались в 150 комбинациях скрещивания | Пятьдесят штаммов образовали примордии | Gao et al.(2015) | ||
| 14 | Pleurotus ostreatus | Было проведено скрещивание монокариотического штамма и дикариотического штамма | Был получен коммерческий штамм «Монгдол», который превосходил контроль | Oh et al. (2015) | ||
| 15 | Легочная пузырчатка | 22 диаллельный дизайн односпорового изолята и наследуемость, а также общую и специфическую комбинационную способность (GCA и SCA) изучали | Компоненты генетической изменчивости и вариации наследуемости наблюдали в исследовании и обнаружили, что признаки были связаны с эффектом доминирования | Авин и другие. | ||
| 16 | Pleurotus ostreatus | В этом исследовании был разработан новый гибрид для воздействия на окружающую среду. Скрещивание Di-Mon между монокариотическим штаммом, полученным из Heuktari, и дикариотическим штаммом Suhan | Soltari был выведен с устойчивостью к высокой температуре и высокой концентрации CO 2 | Oh et al. (2016) | ||
| 17 | Pleurotus eryngii | Был выведен новый сорт под названием Aeryni 5 из Pleurotus eryngii | Было установлено, что качество и урожайность превосходят контрольный сорт | Park et al. (2016) (2016) | ||
| 18 | Pleurotus ostreatus | С помощью скрещивания Di-mon был получен новый штамм из родительских растений Gonji 7ho и Mongdol | Выведенный штамм «Gosol» в исследовании показал экологически стабильную продуктивность | Shin et al. (2016) | ||
| 19 | Pleurotus sajor — Caju были получены | 200 одиночных базидиоспоры изоляты и 10 быстро растущих изоляты диаметра колонии и 10 изолятов диаметра медленно растущей колонии были отобраны для гибридизации | гибридизовали изоляты имели более высокие диаметр колонии по сравнению с хотя бы одним из родителей | Ying et al. (2017) (2017) | ||
| 20 | Pleurotus flabellatus | 34 внутривидовых гибрида получены от родителей P. flabellatus | У двух гибридов обнаружено улучшенное содержание азота и белка | Baral et al. (2017) | ||
| 21 | Pleurotus ostreatus | Гибрид Heuksol был получен путем скрещивания mon-mon между изолятами с одной спорой Suhan и Gosol в исследовании | Выведенный гибрид Heuksol имел более высокую массу ножки | Min-Ji et al.(2017а) | ||
| 22 | Pleurotus citrinopileatus | В ходе исследования был выведен гибрид желтой вешенки для низких температур путем скрещивания мон-мон | Гибрид под названием Джангдари был выведен с повышенной урожайностью и устойчивостью к более низкой температуре | Min-Ji et al. (2017b) (2017b) | ||
| 23 | Pleurotus var. florida | Был выращен 31 монокариотический изолят и скрещена всего 961 возможная пара | Был сформирован один гибрид, который показал совместимость | Taram et al.(2018) | ||
| 24 | Pleurotus eryngii | Было проведено скрещивание для получения сорта среднего размера и быстрого роста | В ходе исследования был получен сорт Aeryni 6 более высокого качества по сравнению с эталонным штаммом | Hee et al. (2018) |
Межвидовая гибридизация
Многие из видов Pleurotus можно успешно скрещивать в лаборатории, и, следовательно, этот подход можно использовать для расширения генетической базы. Гибридизация осуществляется между монокарионами двух разных видов, которые совместимы. Два монокариотических мицелия совместимы, только если они имеют разные аллели в обоих локусах ( matA и matB ). Эта система совместимости через множественные аллели широко распространена среди гименомицетов, гастеромицетов и покрытосеменных растений (Папазиан, 1950). Множественные аллели для генов типа спаривания были впервые отмечены Терекавой (Terekawa 1957), и причина может быть связана с внутригенной рекомбинацией (Eugenio and Anderson 1968).Эта система создает идеальные условия для гибридизации и улучшения различных товарных признаков. Исследования, проведенные несколькими исследователями по межвидовой гибридизации грибов Pleurotus spp. с использованием двухкультурного скрещивания и методологии слияния протопластов приведены в таблице.
Гибридизация осуществляется между монокарионами двух разных видов, которые совместимы. Два монокариотических мицелия совместимы, только если они имеют разные аллели в обоих локусах ( matA и matB ). Эта система совместимости через множественные аллели широко распространена среди гименомицетов, гастеромицетов и покрытосеменных растений (Папазиан, 1950). Множественные аллели для генов типа спаривания были впервые отмечены Терекавой (Terekawa 1957), и причина может быть связана с внутригенной рекомбинацией (Eugenio and Anderson 1968).Эта система создает идеальные условия для гибридизации и улучшения различных товарных признаков. Исследования, проведенные несколькими исследователями по межвидовой гибридизации грибов Pleurotus spp. с использованием двухкультурного скрещивания и методологии слияния протопластов приведены в таблице.
Таблица 2
Исследования межвидовой гибридизации у Pleurotus
Sl. № № | Родительские виды | Полученные скрещивания | Результаты | Ссылки | |||
|---|---|---|---|---|---|---|---|
| 1 | P.Остроус, П. Коламбин, P. Pilmonarius и P. Sajor — Cajor — Caju — Caju — Caju — Caju — Caju — Caju — Caju | Protoplast Fusion | Некоторые из произведений Fusion были морфологически ненормальными | Toyomasu и Mori (1987) | |||
| 2 | P. sajor — caju и P. sapidus sajor — caju и P. sapidus | Были использованы два межвидовых гибрида, изоляты одной споры | Для разработки карты сцепления аллозимов | May et al. (1988) | |||
| 3 | П.ostreatus и P. djamor | Слияние протопластов | Из 412 изолятов 2 изолята обладают зажимным соединением. Оба фузанта показали морфологические вариации | Dhitaphichit and Pornsuriya (2005) | |||
| 4 | Pleurotus pulmonarius и Pleurotus var. Флорида. | Слияние протопластов, индуцированное ПЭГ (полиэтиленгликолем) | Образовались шесть фузантов, и один фузант был стабилен после последовательного субкультивирования | Eyini et al. (2006) (2006) | |||
| 5 | стр. вар. florida и P.cystigiosus | Были образованы два последних гибридных штамма | Хотя целью было увеличение срока годности, фузант показал высокую урожайность | P. eous и P. flabellatus | Слияние протопластов было сделано для улучшения разложения кофейной мякоти | 0.18% частоты Fusion была зафиксирована | Парани и Эссе (2010) |
| 7 | P. Пулмонарий, P. sapidus и P. osreatus и P. osreatus 4 | Dikaryon Mating , P. sapidus и P.ostreatus sapidus и P.ostreatus | Гибридный штамм, полученный в ходе исследования, показал лучшие результаты по сравнению с диким штаммом с точки зрения продуктивности икры, массы тела свежих плодов, биологической эффективности и производительности | Adebayo et al.(2013) | |||
| 8 | стр. вар. florida и P. sajor-caju | Было разработано пять гибридных дикарионов | У гибридов наблюдались различия в отношении качества, профиля ферментов, родства, скорости линейного роста и т. д. по сравнению с родительскими | Jaswal et al. . (2014) | |||
| 9 | P. ostreatus var . Флорида и P. djamor var . roseus ostreatus var . Флорида и P. djamor var . roseus | Слияние протопластов, опосредованное ПЭГ | Образовалось пять соматических гибридов, но только два из них смогли плодоносить.Урожайность одного фузанта выше, чем у обоих родителей | Selvakumar et al. (2015) | |||
| 10 | стр. вар. Флорида и P. Sajor-Caju P. Sajor-Caju | ElectromFusion | Гибридные штаммы выпускаются показали более высокий выход и нижняя спорная масса | Kaur и Kapoor (2015) | |||
| 11 | P . | Десять монокарионных культур родительских штаммов скрестили во всех комбинациях для получения гибридов | Несколько полученных гибридов оказались хорошими по окраске и урожайности.Гетерозис оценивали по родительскому гетерозису | Роснина и соавт. (2016) | |||
| 12 | |||||||
| в производстве и один для урожая | Tagavi et al. (2016) | ||||||
| 13 | P. pulmonarius и P.citrinopileatus | Десять монокарионов от каждого родителя скрещивали в комбинациях. Всего было получено пять гибридов | Один гибрид показал более высокий рост мицелия и урожайность по сравнению с родителями | Abdulgani et al. 2017 г. и другие.(2018) 2017 г. и другие.(2018) |
Межродовая гибридизация
Межродовая гибридизация, т. е. скрещивание между монокарионами двух разных родов, используется для объединения признаков, отсутствующих в роде, или для улучшения некоторых специфических признаков или свойств, таких как использование сред и производство красителей. Несмотря на непрекращающиеся усилия, до сих пор не удалось добиться больших успехов в межродовой гибридизации. Основным ограничением является отсутствие образования плодовых тел из-за стерильности и монокариотизации.Эти типы экспериментов по гибридизации в основном используют технику слияния протопластов. Некоторые исследования межродовой гибридизации упомянуты в таблице.
Таблица 3
Исследования межродовой гибридизации у Pleurotus
| Sl. NO | Род и вид | Цель | Результаты | Результаты | Ссылки | |||
|---|---|---|---|---|---|---|---|---|
| 1 | Pleurotus Sajor-Caju и Schizophyllum Commune 4 | Исследование было направлено на то, чтобы узнать возможность использования протопласта как инструмент для аутбридинга между Pleurotus sajor — caju и Schizophyllum commune | Менее нормальное плодоношение наблюдалось в исследовании и S. | Лян и Чанг (1989) | ||||
| 2 | PLEUROTUS Orsreatus и Schizophyllulum Commune и Schizophyllulum Commune и Schizophyllum Commune | исследование было нацелено на понять гетерокариоз межгенерических протопластовских богослужений | Большинство флангов были стерильными и монокариотическими гетерокариоза не обнаружено. Сообщалось об увеличении содержания ДНК. Образован рекомбинантный гибрид | Zhao and Chang (1996) | ||||
| 3 | Calocybe indica и Pleurotus var. florida florida | Получение плодовых тел соматического гибрида путем слияния протопластов с использованием ПЭГ | Гибрид имеет Calocybe в качестве доминирующего родителя, и было обнаружено значительное повышение биологической эффективности и содержания γ-линолевой кислоты | Chakraborty and Sikdar ( 2010) | ||||
4 | 4 | Plurotus Florida и Calocybe INDICA 9009 | Изучение нового полисахарида, присутствующего в гибридном | в исследовании, гетерогликан, водорастворимый экстракт был найден в соматическом гибридном с антиоксидантом | Майти и др. |  (2011) (2011) | |||
| 5 | Ganoderma lucidum и Pleurotus var. florida | Слияние протопластов было проведено для получения фузанта с высокой способностью к обесцвечиванию красителя | Полученный гибрид в исследовании показал более высокую скорость обесцвечивания красителя для Reactive Black 5 и Reactive Yellow 44 и быстрое обесцвечивание для Reactive Red 2 | Nanthini и другие. (2013) | ||||
| 6 | Pleurotus var. florida и Lentinus squarrosulus | Исследование было сосредоточено на разработке соматических гибридов путем слияния протопластов | В ходе исследования были успешно получены шесть штаммов соматических гибридов, которые успешно культивировались на субстрате из рисовой соломы 7 | Pleurotus Oreatus, Pleurotus Djamor и Lentinula Edodes 194| Neohaplonts были сгенерированы из каждого родительского типа, а гибрид разработан 9009 9007 , образованный из PLEUROTUS и LENTINULA показал наибольший уровень роста на агаре солода зерно пшеницы | Cobos et al. |  (2017) (2017) |
Механизм гетерозиса у
Pleurotus Гетерозис превосходство или неполноценность F 1 s над родителями/коммерческая проверка. Термин гетерозис был введен Г. Х. Шуллом (Crow 2001). Преобладающая гипотеза гетерозиса основана на доминировании и сверхдоминировании. Гипотеза доминирования — это устранение вредных эффектов рецессивных аллелей из-за превосходства доминантных аллелей, тогда как гипотеза сверхдоминирования — это ассоциация разных аллелей, создающая генетическую гетерозиготность, которая отвечает за гетерозис.Гетерозис рассчитывают как процентное превосходство над средним значением родительского (MP), лучшего родительского (BP) и коммерческого сорта (CC). В Pleurotus было проведено несколько исследований гетерозиса. Avin и коллеги использовали MP и BP в качестве критериев для определения гетерозиса у Pleurotus pulmonarius . В этом исследовании было обнаружено, что высокое значение доминирования важно для гетерозиса (Avin et al. 2016).
2016).
Исследование паттернов экспрессии генов в масштабах всего генома, проведенное Liu et al.(2017) показали, что гетерозис является результатом дифференциальной экспрессии генов, которая приводит к возникновению всех пяти типов паттернов экспрессии генов. Паттерны показаны на рис. и обобщены в исследовании Лю и его коллеги. A, B, C и D показывают вариацию из-за наличия и отсутствия экспрессии генов, тогда как E предполагает наличие двух экспрессий генов (аддитивной и неаддитивной) (Liu et al. 2017). Аналогичное исследование, проведенное на Pleurotus ostreatus в отношении лакказной активности, показало, что дикариотическое превосходство лакказной активности по сравнению с монокарионами обусловлено неаддитивным повышением транскрипционной активности лакказы (гены lacc6 и lacc10) (Castanera et al.2013). Таким образом, исследования доказывают механизм дикариотического превосходства, то есть гетерозиса, но для понимания гетерозиса по количественным признакам все еще требуется больше уточнений.
Дифференциальная экспрессия генов, обнаруженная во время гетерозиса у родителей и гибрида Pleurotus (Создано на основе исследования Liu et al., 2017)
Мутационное размножение
Действительно, мутация является мощным инструментом для создания изменчивости у генетически насыщенных видов. Мутация как инструмент селекции используется во многих культурах для улучшения желаемых агрономических признаков.Мутационная селекция приводит к созданию новых генов либо путем спонтанной мутации, либо с помощью индуцированных мутагенов. Мутационная селекция — это полностью создание новых генов либо путем спонтанной мутации, либо с использованием мутагенов. Мутация может вызывать изменения на трех уровнях, т. е. нуклеотидная вариация (изменения в последовательности нуклеотидов), хромосомная вариация (изменение структуры хромосом в результате разрыва и воссоединения) и геномная вариация (изменения числа хромосом в результате анеуплоидии и эуплоидии) (Donini и Соннино, 1998). Мутации в основном вредны, но некоторые признаки, такие как отсутствие потемнения и развитие бесспоровых штаммов, хорошо подходят для этой методологии. В Pleurotus было использовано много таких мутаций, которые представлены в таблице . Таблица 4 нет.
 (2001)
(2001) 75 кГр при скорости облучения 1,149 кГрэй/час
75 кГр при скорости облучения 1,149 кГрэй/час (2012)
(2012) florida
florida  д., 5–10 см с временными диапазонами 10, 15, 20 и 25 мин. Дозы EMS от 0,001-0,005%
д., 5–10 см с временными диапазонами 10, 15, 20 и 25 мин. Дозы EMS от 0,001-0,005% (2017)
(2017)Генетические исследования и селекция
Характеристика генома и митохондриальная наследственность
Развитие высокопроизводительных технологий генома позволяет проводить глубокое исследование неизученных признаков генома грибов. К настоящему времени секвенированы геномы семи видов рода Pleurotus (база данных NCBI). Сравнительный анализ последовательностей геномов показал, что размеры генома Pleurotus eryngii и Pleurotus tuoliensis значительно больше, чем у других Pleurotus spp. Основная причина связана с более высоким процентом мобильных элементов (TS) и большим количеством долговременных повторяющихся мобильных элементов у Pleurotus eryngii и Pleurotus tuoliensis (Zhang et al.2018). Эти мобильные элементы играют эпигенетическую роль и вызывают молчание в геномах Pleurotus (Borgognone et al. 2018). Также сообщается, что около 1845 повторов одной последовательности присутствуют в Pleurotus citrinopileatus . Это число в семь раз выше у Pleurotus eryngii (Li et al. 2018). Митохондриальный геном Pleurotus ostreatus также показал наличие 73 242 п.н., 26,4% содержания GC, 44 генов, кодирующих 18 белков, и 26 генов РНК.
К настоящему времени секвенированы геномы семи видов рода Pleurotus (база данных NCBI). Сравнительный анализ последовательностей геномов показал, что размеры генома Pleurotus eryngii и Pleurotus tuoliensis значительно больше, чем у других Pleurotus spp. Основная причина связана с более высоким процентом мобильных элементов (TS) и большим количеством долговременных повторяющихся мобильных элементов у Pleurotus eryngii и Pleurotus tuoliensis (Zhang et al.2018). Эти мобильные элементы играют эпигенетическую роль и вызывают молчание в геномах Pleurotus (Borgognone et al. 2018). Также сообщается, что около 1845 повторов одной последовательности присутствуют в Pleurotus citrinopileatus . Это число в семь раз выше у Pleurotus eryngii (Li et al. 2018). Митохондриальный геном Pleurotus ostreatus также показал наличие 73 242 п.н., 26,4% содержания GC, 44 генов, кодирующих 18 белков, и 26 генов РНК. Сообщается о девяти интронах в гене cox1 Pleurotus ostreatus (Wang et al. 2008). Митохондриальная ДНК слиток Pleurotus показала митохондриальное наследование в зависимости от местоположения образца при гибридизации. Замечено, что иногда в месте соединения совместимых гиф содержится мтДНК любой особи, смесь как родительской мтДНК, так и/или рекомбинантной мтДНК. Его наследственность зависит от места, откуда было взято потомство (Мацумото и Фукумаса-Накаи, 1996; Уилсон и Сюй, 2012) (таблица).
Сообщается о девяти интронах в гене cox1 Pleurotus ostreatus (Wang et al. 2008). Митохондриальная ДНК слиток Pleurotus показала митохондриальное наследование в зависимости от местоположения образца при гибридизации. Замечено, что иногда в месте соединения совместимых гиф содержится мтДНК любой особи, смесь как родительской мтДНК, так и/или рекомбинантной мтДНК. Его наследственность зависит от места, откуда было взято потомство (Мацумото и Фукумаса-Накаи, 1996; Уилсон и Сюй, 2012) (таблица).
Таблица 5
Таблица 5
Размер генома, содержание GC и общих генов разных PLEUROTUS видов
| вид | Размер генома (MB) | GC% | Total Gene | |
|---|---|---|---|---|
| Pleurotus ostreatus | 34,34 | 50,9 | 12 460 | |
| Рыжий утконос | 39,96 | 51,0 | 17 105 | |
| Pleurotus citrinopileatus | 36. 84 84 | 49,2 | 15 237 | |
| Pleurotus salmoneo-stramineus | 39,19 | 50,0 | – | |
| Pleurotus eryngii | 49.92 | 49.92 | 494 | 13 213 |
| Pleurotus tuber — REGIUM | 33.56 | 46.1 | — | |
| Pleurotus tuoliensis | 48,23 | 50. 2 2 | 13,097 |
Селекция и генетические исследования экономически важных признаков
Селекция/селекция по признакам используется для улучшения конкретных признаков многих товарных культур. Поскольку грибы являются неотъемлемой частью системы товарного земледелия, требуется более интенсивное генетическое улучшение. Тем не менее, уже предпринимаются усилия по селекции грибов Pleurotus по конкретным признакам.
Селекция на раннеспелые сорта Для селекции раннеспелых сортов необходимо понимание механизма перехода от вегетативной к репродуктивной стадии посредством кодирующего белка.Хотя некоторые виды, такие как P. djamor и P . membranaceus плодоносят рано, переносимость этого признака скороспелости зависит от правильной идентификации ответственного за него гена. Берн и др. в 2007 г. обнаружили белок под названием «остреолизин», который может быть ответственным за первичное образование и спорообразование (Berne et al. 2007). Точно так же другие белки, подобные эгеролизинам, такие как эрингеолизин и плевротолизин, присутствуют в Pleurotus spp. Развитие булавочной головки у Pleurotus начинается с агрегации мицелия, который трансформируется в булавочную головку (рис.).
2007). Точно так же другие белки, подобные эгеролизинам, такие как эрингеолизин и плевротолизин, присутствуют в Pleurotus spp. Развитие булавочной головки у Pleurotus начинается с агрегации мицелия, который трансформируется в булавочную головку (рис.).
Стадии развития булавочных головок Pleurotus
Выведение бесспоровых штаммов Спорокарпии вешенки производят большое количество спор, которые могут вызывать аллергическую реакцию у рабочих во время выращивания. Респираторная аллергия, связанная со спорами, была зарегистрирована у рабочих, работающих с вешенками (Cox, 1988; Helbling et al., 1999; Vereda et al., 2007). Сообщается, что признаки отсутствия спор часто связаны с такими признаками, как низкое качество и урожайность (Okuda et al.2013). Окуда и его коллеги идентифицировали гена stpp1 , который кодирует белок, принадлежащий к семейству гомологов MutS (MSH) и связанный с репарацией несоответствия в синтезе ДНК или рекомбинации во время мейоза. Они также идентифицировали маркеры STS (Sequence-Tagged Site), которые были предназначены для размножения бесспоровых признаков в Pleurotus pulmonarius . Лишь ограниченный успех был достигнут в разработке настоящих бесспоровых сортов.
Они также идентифицировали маркеры STS (Sequence-Tagged Site), которые были предназначены для размножения бесспоровых признаков в Pleurotus pulmonarius . Лишь ограниченный успех был достигнут в разработке настоящих бесспоровых сортов.
Селекция на пищевую ценность и качество Улучшение морфологии и питательных свойств грибов важно для роста рынка грибов.Биообогащение витамином D и ловастатином предлагает многочисленные возможности. Ким и его коллеги разработали штамм с длительным сроком хранения в Pleurotus eryngii с использованием гибридизации mon-mon. Разработанный гибридный штамм оставался нормальным после периода 59 дней при 4 °C. Исследование выявило корреляцию срока годности с твердостью ножки (Ким и др., 2013).
Разведение на урожай Для различных видов были созданы карты сцепления. Исследования QTL, проведенные на Pleurotus ostreatus , показали, что QTL признаков, связанных с урожайностью, расположены на хромосоме VII. QTL, связанные с качеством, разбросаны по геному с меньшими вариациями (Larraya et al. 2003). Также было идентифицировано картирование связи фермента, разлагающего лигнин, в Pleurotus ostreatus со структурными генами и контролирующими генами (Santoyo et al. 2008). Была идентифицирована область генома, определяющая скорость роста мицелия с помощью картирования QTL (Larraya et al. 2002). Генетическая карта сцепления признаков отсутствия спор была изучена у Pleurotus pulmonarius , и было обнаружено, что область гена, ответственная за бесспоровую мутацию, находилась в группе сцепления II (Okuda et al.2009).
QTL, связанные с качеством, разбросаны по геному с меньшими вариациями (Larraya et al. 2003). Также было идентифицировано картирование связи фермента, разлагающего лигнин, в Pleurotus ostreatus со структурными генами и контролирующими генами (Santoyo et al. 2008). Была идентифицирована область генома, определяющая скорость роста мицелия с помощью картирования QTL (Larraya et al. 2002). Генетическая карта сцепления признаков отсутствия спор была изучена у Pleurotus pulmonarius , и было обнаружено, что область гена, ответственная за бесспоровую мутацию, находилась в группе сцепления II (Okuda et al.2009).
Селекция на устойчивость к вредителям и болезням Грибные мухи становятся серьезными вредителями и представляют значительную угрозу для урожая вешенки. Поскольку это грибковый организм, распыление неорганических химикатов для защиты растений не рекомендуется для борьбы с грибными мухами. Поддержание гигиены и распыление продуктов на микробной основе и растительных препаратов предпочтительнее инсектицидов (Erler and Polat 2015). В качестве селекционной стратегии создание толерантных штаммов может предложить эффективный подход к управлению.Выведение штаммов, которые могут проявлять механизмы антибиоза и антиксеноза, может открыть большие возможности для развития штаммов, устойчивых к мухам. Однако селекционные усилия по созданию таких штаммов мизерны. В ближайшем будущем устойчивые к вредителям штаммы будут пользоваться большим спросом в грибной индустрии.
В качестве селекционной стратегии создание толерантных штаммов может предложить эффективный подход к управлению.Выведение штаммов, которые могут проявлять механизмы антибиоза и антиксеноза, может открыть большие возможности для развития штаммов, устойчивых к мухам. Однако селекционные усилия по созданию таких штаммов мизерны. В ближайшем будущем устойчивые к вредителям штаммы будут пользоваться большим спросом в грибной индустрии.
Генетическая трансформация в
Pleurotus Генетическая трансформация стала ценным инструментом для улучшения сорта. Существует четыре техники трансформации.Это полиэтиленгликоль/CaCl 2 (Honda et al. 2000), электропорация, бомбардировка частицами (Sunagawa and Magae 2002) и использование Agrobacterium (Sharma and Kuhad 2010). С развитием молекулярных методов была начата генетическая трансформация Pleurotus для повышения пищевой и лекарственной продуктивности, что утомительно при использовании традиционных подходов к гибридизации. Это ценный инструмент для улучшения штамма, особенно для признаков, которые утомительно обрабатывать с помощью традиционных подходов гибридизации.Генетическая трансформация Pleurotus ostreatus была стандартизирована для маркерного гена селекции на основе присутствия карбоксина Honda et al. в 1999 г. Это первый гомологичный маркерный ген, доступный для молекулярной селекции съедобных грибов (Honda et al. 2000). Эта новая система маркеров более эффективна, чем маркер устойчивости к гигромицину В, поскольку обладает большей воспроизводимостью. Генетическая трансформация Pleurotus полиэтиленгликолем/CaCl 2 была использована для переноса желаемых генов с более стабильной интеграцией.Например, урациловые ауксотрофы Pleurotus ostreatus были получены путем переноса гена ura3 Trichoderma reesei , который показал устойчивость к 5P-фторороту (5-FOA) (Kim et al. 1999). Точно так же в P. ostreatus ген устойчивости к биалафосу из Streptomyces hygroscopicus и β-глюкуронидаза (GUS) из Escherichia coli были экспрессированы и котрансформированы с использованием промотора гена ras и терминатора гена priA из Lentinus edodes (Yana) др.
Это ценный инструмент для улучшения штамма, особенно для признаков, которые утомительно обрабатывать с помощью традиционных подходов гибридизации.Генетическая трансформация Pleurotus ostreatus была стандартизирована для маркерного гена селекции на основе присутствия карбоксина Honda et al. в 1999 г. Это первый гомологичный маркерный ген, доступный для молекулярной селекции съедобных грибов (Honda et al. 2000). Эта новая система маркеров более эффективна, чем маркер устойчивости к гигромицину В, поскольку обладает большей воспроизводимостью. Генетическая трансформация Pleurotus полиэтиленгликолем/CaCl 2 была использована для переноса желаемых генов с более стабильной интеграцией.Например, урациловые ауксотрофы Pleurotus ostreatus были получены путем переноса гена ura3 Trichoderma reesei , который показал устойчивость к 5P-фторороту (5-FOA) (Kim et al. 1999). Точно так же в P. ostreatus ген устойчивости к биалафосу из Streptomyces hygroscopicus и β-глюкуронидаза (GUS) из Escherichia coli были экспрессированы и котрансформированы с использованием промотора гена ras и терминатора гена priA из Lentinus edodes (Yana) др. 1996). С использованием метода биолистического переноса/практической бомбардировки также была проведена трансформация Pleurotus . Первые исследования бомбардировки частицами были проведены Sunagawa and Magae 2002. Частота трансформации составляла один трансформант на мкг ДНК. Для трансформации использовали плазмиду pTRura 3-2 (pUC8), содержащую ген оротидин-5Р-фосфатдекарбоксилазы из Trichoderma reesei (Sunagawa and Magae 2002). Опосредованная Agrobacterium трансформация осуществлялась либо плодовыми телами (Chen et al.2000), проросшими спорами (Ding et al. 2011) или протопластом (Zhang et al. 2014). Применение генетической трансформации безгранично для использования лекарственных соединений, присутствующих в грибах.
1996). С использованием метода биолистического переноса/практической бомбардировки также была проведена трансформация Pleurotus . Первые исследования бомбардировки частицами были проведены Sunagawa and Magae 2002. Частота трансформации составляла один трансформант на мкг ДНК. Для трансформации использовали плазмиду pTRura 3-2 (pUC8), содержащую ген оротидин-5Р-фосфатдекарбоксилазы из Trichoderma reesei (Sunagawa and Magae 2002). Опосредованная Agrobacterium трансформация осуществлялась либо плодовыми телами (Chen et al.2000), проросшими спорами (Ding et al. 2011) или протопластом (Zhang et al. 2014). Применение генетической трансформации безгранично для использования лекарственных соединений, присутствующих в грибах.
Инструменты редактирования генома
Инструменты редактирования генома — это самые мощные инструменты, которые могут усилить или уменьшить нежелательное проявление признака. Одним из таких средств является CRISPER Cas-9. РНК-управляемый CRISPER (кластеры коротких палиндромных повторов с регулярными промежутками) — нуклеазы Cas представляют собой микробную адаптивную иммунную систему, которая разрушает чужеродные генетические элементы с помощью нуклеаз (Ran et al. 2013). Эта система использовалась в грибах для получения штаммов шампиньонов, устойчивых к потемнению. Это было достигнуто за счет удаления одного гена из шести, кодирующего полифенолоксидазу (PPO), что снизило активность фермента на 30% (Waltz 2016). Помимо этого, для улучшения желаемых признаков у Pleurotus можно использовать несколько других молекулярных методов, основанных на омике. Кроме того, мы можем передать полезные признаки от других видов, используя подходы, основанные на генной инженерии и селекции.Однако этические соображения важны, прежде чем эти технологии можно будет использовать в коммерческих целях.
2013). Эта система использовалась в грибах для получения штаммов шампиньонов, устойчивых к потемнению. Это было достигнуто за счет удаления одного гена из шести, кодирующего полифенолоксидазу (PPO), что снизило активность фермента на 30% (Waltz 2016). Помимо этого, для улучшения желаемых признаков у Pleurotus можно использовать несколько других молекулярных методов, основанных на омике. Кроме того, мы можем передать полезные признаки от других видов, используя подходы, основанные на генной инженерии и селекции.Однако этические соображения важны, прежде чем эти технологии можно будет использовать в коммерческих целях.
Будущие возможности
Генетическое улучшение — это непрерывный процесс. Несмотря на то, что была проделана огромная работа, необходимо получить много жизненно важной информации для достижения цели, а также для повышения генетической выгоды в программе селекции грибов. Требуются дополнительные исследования комбинированной способности, наследуемости, генетического прогресса, корреляции, параметров стабильности и т. д. Необходима долгосрочная программа для улучшения генофонда Pleurotus .Преимуществом этого гриба является более короткий жизненный цикл, что позволяет селекционерам увеличить цикл селекции по сравнению с растениями. Разработка тестовых штаммов для гибридизации также является одной из областей, требующих изучения. Информация, полученная в результате секвенирования генома, должна быть объединена с подходами молекулярной селекции и полногеномной селекции, а также должна быть приведена в соответствие с текущими протоколами селекции.
д. Необходима долгосрочная программа для улучшения генофонда Pleurotus .Преимуществом этого гриба является более короткий жизненный цикл, что позволяет селекционерам увеличить цикл селекции по сравнению с растениями. Разработка тестовых штаммов для гибридизации также является одной из областей, требующих изучения. Информация, полученная в результате секвенирования генома, должна быть объединена с подходами молекулярной селекции и полногеномной селекции, а также должна быть приведена в соответствие с текущими протоколами селекции.
Соответствие этическим нормам
Конфликт интересовОт имени всех авторов соответствующий автор заявляет об отсутствии конфликта интересов.
Ссылки
- Abdulgani R, Lau CC, Abdullah N, Vikineswary S. Морфологическая и молекулярная характеристика гибридов Pleurotus pulmonarius (Fr.) quél с улучшенными характеристиками спорофора и более высокой биологической эффективностью. Int J Agric Biol. 2017;19:707–712.
 doi: 10.17957/IJAB/15.0343. [CrossRef] [Google Scholar]
doi: 10.17957/IJAB/15.0343. [CrossRef] [Google Scholar] - Adebayo EA, Oloke JK, Yadav A, Barooah M, Bora TC. Повышение урожайности Pleurotus pulmonarius за счет слияния дикарионов с гифальным анастомозом.World J Microbiol Biotechnol. 2013;29:1029–1037. doi: 10.1007/s11274-013-1266-8. [PubMed] [CrossRef] [Google Scholar]
- Adebayo EA, Oloke JK, Bordoloi AK, Barooah M, Bora TC. Улучшение Pleurotus pulmonarius Lau 09 посредством мутации для увеличения урожайности. Рез Джей Мутаген. 2014; 4:1–13. doi: 10.3923/rjmutag.2014.1.13. [CrossRef] [Google Scholar]
- Adejumo IO, Adetunji CO, Adeyemi OS. Влияние воздействия УФ-излучения на минеральный состав и продукцию биомассы микомойса, полученного из различных сельскохозяйственных субстратов.J Сельскохозяйственные науки. 2017;62:51–59. doi: 10.2298/JAS1701051A. [CrossRef] [Google Scholar]
- Авин Ф.А., Бхассу С., Рамех В. и др. Генетика и гибридная селекция Pleurotus pulmonarius : гетерозис, наследуемость и комбинационная способность.
 Эвфитика. 2016;209:85–102. doi: 10.1007/s10681-016-1638-x. [CrossRef] [Google Scholar]
Эвфитика. 2016;209:85–102. doi: 10.1007/s10681-016-1638-x. [CrossRef] [Google Scholar] - Baars JJP, Sonnenberg ASM, Mikosch TSP, Van Griensven LJLD. Разработка бесспорового штамма вешенки Pleurotus ostreatus . В: Гринсвен Ван., редактор. Наука и выращивание съедобных грибов. Роттердам: Балкема; 2000. стр. 317–323. [Google Scholar]
- Bamigboye CO, Oloke JK, Dames JF. Биологическая активность внеклеточных и внутриклеточных полисахаридов из Pleurotus tuber — regium гибридных и мутантных штаммов. J Food Nutr Res. 2016; 4: 422–428. doi: 10.12691/JFNR-4-7-2. [CrossRef] [Google Scholar]
- Барал Д., Рой А., Тапа С., Чеванг Бхутиа К. Разработка внутривидовой гибридизации Pleurotus flabellatus для повышения урожайности и питания.Int J Curr Microbiol App Sci. 2017; 6: 735–742. doi: 10.20546/ijcmas.2017.611.086. [CrossRef] [Google Scholar]
- Baral D, Roy A, Thapa S, Chettri D. Выбор питательных сред и монокариотических изолятов Pleurotus flabellatus и P.
 sajor – caju для их дикариотизации с последующим тестированием производительности дикариотических изолятов на агаризованной среде с солодовым экстрактом. Curr J Appl Sci Technol. 2018; 26:1–10. doi: 10.9734/CJAST/2018/40423. [CrossRef] [Google Scholar]
sajor – caju для их дикариотизации с последующим тестированием производительности дикариотических изолятов на агаризованной среде с солодовым экстрактом. Curr J Appl Sci Technol. 2018; 26:1–10. doi: 10.9734/CJAST/2018/40423. [CrossRef] [Google Scholar] - Berne S, Pohleven J, Vidic I, et al.Остреолизин усиливает начало плодоношения у вешенки ( Pleurotus ostreatus ) Mycol Res. 2007; 111:1431–1436. doi: 10.1016/j.mycres.2007.09.005. [PubMed] [CrossRef] [Google Scholar]
- Bhandal MS, Mehta KB. Генетическое улучшение видов Pleurotus . В: Nair MC, Gokulapalan C, Das L, редакторы. Прогресс в биотехнологии грибов. Джодхпур: научные издательства; 1994. С. 127–133. [Google Scholar]
- Боргоньоне А., Кастанера Р., Морселли М., Лопес-Варас Л., Рубби Л., Писабарро А.Г., Пеллегрини М., Рамирес Л.Связанное с транспозоном эпигенетическое замалчивание во время жизненного цикла Pleurotus ostreatus . Рез. ДНК 2018;25:1–14. doi: 10.1093/dnares/dsy016.
 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
[Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] - Bresinksy A, Fisher M, Meixner B, Paulus W. Видообразование в Pleurotus . Микология. 1987; 79: 234–245. doi: 10.1080/00275514.1987.12025703. [CrossRef] [Google Scholar]
- Castanera R, Omarini A, Santoyo F, et al. Неаддитивные профили транскрипции лежат в основе дикариотического превосходства в лакказной активности Pleurotus ostreatus .ПЛОС Один. 2013;8:e73282. doi: 10.1371/journal.pone.0073282. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
- Chakraborty U, Sikdar SR. Межродовое слияние протопластов между Calocybe indica (молочный гриб) и Pleurotus florida способствует качественному и количественному улучшению спорофора молочного гриба. World J Microbiol Biotechnol. 2010;26:213–225. doi: 10.1007/s11274-009-0162-8. [CrossRef] [Google Scholar]
- Chang AC. Генетика и селекция съедобных грибов.США: CRC Press; 1992. [Google Scholar]
- Chen X, Stone M, Schlagnhaufer C, Romaine CP.
 Метод ткани плодового тела для эффективной опосредованной Agrobacterium трансформации Agaricus bisporus . Appl Environ Microbiol. 2000;66:4510–4513. doi: 10.1128/AEM.66.10.4510-4513.2000. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Метод ткани плодового тела для эффективной опосредованной Agrobacterium трансформации Agaricus bisporus . Appl Environ Microbiol. 2000;66:4510–4513. doi: 10.1128/AEM.66.10.4510-4513.2000. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] - Cobos JDV, Páramo D, Aguilar MEG, Hernández AS, Lara HL, del Toro GV. Получение гибридных штаммов среди Pleutorus и Lentinula и оценка кинетики их мицелиального роста на агаре с солодовым экстрактом и зерне пшеницы с использованием моделей Гомперца и Хилла.Эмир Джей Фуд Агрик. 2017;29:927–935. doi: 10.9755/ejfa.2017.v29.i12.1563. [CrossRef] [Google Scholar]
- Кокс А. Внешний аллергический альвеолит, вызванный спорами вешенки Pleurotus ostreatus . Eur Respir J. 1988; 1: 466–468. [PubMed] [Google Scholar]
- Crow JF. Гетерозис. Энцикл Генет. 2001 г.: 10.1006/RWGN.2001.0611. [CrossRef] [Google Scholar]
- Даопин XXX. Исследование мутационной селекции высокопродуктивного и бесспорового Pleurotus ostreatus с помощью УФ-облучения протопласта.
 Acta Edulis Fungi. 1997; 4:13–17. [Google Scholar]
Acta Edulis Fungi. 1997; 4:13–17. [Google Scholar] - Dhitaphichit P, Pornsuriya C. Слияние протопластов Pleurotus ostreatus и P. djamor . Songklanakarin J Sci Technol. 2005; 27: 975–982. [Google Scholar]
- Ding Y, Liang S, Lei J, Chen L, Kothe E, Ma A. Agrobacterium tumefaciens опосредовала экспрессию слитых генов egfp-hph под контролем промотора gpd в Pleurotus ostreatus . Микробиолог Рез. 2011; 166:314–322. doi: 10.1016/j.мкр.2010.07.001. [PubMed] [CrossRef] [Google Scholar]
- Djajanegara I, Harsoyo Белый вешенка ( Pleurotus florida ) мутант с измененным содержанием антиоксидантов. Ж биотропия. 2008; 15:65–73. doi: 10.11598/BTB.2008.15.1.6. [CrossRef] [Google Scholar]
- Джаджанегара И., Масдуки А. Слияние протопластов белых и коричневых вешенок. Индонез J Agric Sci. 2010; 11:16–23. doi: 10.21082/ijas.v11n1.2010.p16–23. [CrossRef] [Google Scholar]
- Донини П., Соннино А.Индуцированная мутация в селекции растений: современное состояние и перспективы.
 В: Джейн С.М., Брар Д.С., Ахлоувалиа Б.С., редакторы. Сомаклональная изменчивость и индуцированная мутация в улучшении сельскохозяйственных культур: современная наука о растениях и биотехнология в сельском хозяйстве. Дордрехт: Спрингер; 1998. С. 255–291. [Google Scholar]
В: Джейн С.М., Брар Д.С., Ахлоувалиа Б.С., редакторы. Сомаклональная изменчивость и индуцированная мутация в улучшении сельскохозяйственных культур: современная наука о растениях и биотехнология в сельском хозяйстве. Дордрехт: Спрингер; 1998. С. 255–291. [Google Scholar] - Эрлер Ф., Полат Е. Мухи на грибах, выращиваемых в районе Анталья-Коркутели, и борьба с ними. Akdeniz Üniv Ziraat Fak Derg. 2015;28:61–66. [Google Scholar]
- Eugenio CP, Anderson NA.Генетика и культивирование Pleurotus ostreatus . Микология. 1968;60:627. дои: 10.2307/3757430. [CrossRef] [Google Scholar]. Микобиология. 2006; 34:73–78. doi: 10.4489/MYCO.2006.34.2.073. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
- Gaitan-Hernandez R, Salmones D. Получение и характеристика штаммов Pleurotus ostreatus для коммерческого выращивания в теплых условиях окружающей среды.Научный Хортик. 2008; 118:106–110. doi: 10.1016/J.SCIENTA.2008.05.029. [CrossRef] [Google Scholar]
- Gao K, Xing Z, et al.
 Селекция и идентификация гибридного штамма Pleurotus eryngii var. туолиенсис . Северный Хортик. 2015;9:36. [Google Scholar]
Селекция и идентификация гибридного штамма Pleurotus eryngii var. туолиенсис . Северный Хортик. 2015;9:36. [Google Scholar] - Голтапе Э.М., Гарехаджи А.Н., Масиха С., Гордан Х.Р. Гибридная продукция вешенки Pleurotus ostreatus (Jacq: Fries) kummer. Пакистан J Biol Sci. 2007; 10: 2334–2340. doi: 10.3923/pjbs.2007.2334.2340. [PubMed] [CrossRef] [Google Scholar]
- Гупта Б., Ниранджан Редди Б.П., Котастане А.С. Молекулярная характеристика и анализ типа спаривания вешенки ( Pleurotus spp.) с использованием отдельных базидиоспор для улучшения штамма. World J Microbiol Biotechnol. 2011; 27:1–9. doi: 10.1007/s11274-010-0419-2. [CrossRef] [Google Scholar]
- Ha TM, Choi JI, Jeon DH, Ju YC, Shin PG. Характеристика и селекция нового сорта Pleurotus eryngii , Saegonji.Дж Гриб. 2014;12:127–131. doi: 10.14480/JM.2014.12.2.127. [CrossRef] [Google Scholar]
- Hee LS, Min-Keun K, Jae-San R. Характеристики нового сорта Pleurotus eryngii , Aeryni 6.
 J Mushroom. 2018;16:16–21. doi: 10.14480/JM.2018.16.1.16. [CrossRef] [Google Scholar]
J Mushroom. 2018;16:16–21. doi: 10.14480/JM.2018.16.1.16. [CrossRef] [Google Scholar] - Хелблинг А., Гайер Ф., Брандер К.А. Респираторная аллергия на споры грибов: недостаточно изучена, но актуальна. Энн Аллергия Астма Иммунол. 1999;83:17–19. doi: 10.1016/S1081-1206(10)63506-5. [PubMed] [CrossRef] [Google Scholar]
- Henglei C, Honggui W, Jun Z, Xianxian Z.Скрининг мутаций Pleurotus ferulae с устойчивостью к высокой температуре с помощью имплантации ионов азота. Плазменные технологии. 2008; 10: 503–505. doi: 10.1088/1009-0630/10/4/21. [CrossRef] [Google Scholar]
- Honda Y, Matsuyama T, Irie T, Watanabe T, Kuwahara M. Трансформация резистентности к карбоксину гриба-гомобазидиомицета Pleurotus ostreatus . Карр Жене. 2000; 37: 209–212. doi: 10.1007/s002940050521. [PubMed] [CrossRef] [Google Scholar]
- Im CH, Kim MK, Kim KH, Cho SJ, Lee JJ, Joung WK, Lee SD, Choi YJ, Ali A, Ryu JS.Выведение Pleurotus eryngii с признаком устойчивости к высоким температурам.
 Дж Гриб. 2014;12:187–192. doi: 10.14480/JM.2014.12.3.187. [CrossRef] [Google Scholar]
Дж Гриб. 2014;12:187–192. doi: 10.14480/JM.2014.12.3.187. [CrossRef] [Google Scholar] - Джасвал Р.К., Соди Х.С., Шарма С. Характеристика межвидовых гибридных дикарионов вешенки, Pleurotus florida PAU-5 и P. sajor — caju PAU-3 (высшая Базидиомицеты) из Индии. Int J Med Mushrooms. 2014;16:355–364. doi: 10.1615/IntJMedMushrooms.v16.i4.60. [PubMed] [CrossRef] [Google Scholar]
- Jeong Y, Jung M, Kim MJ, Hwang CH.Индуцированный 4-нитрохиноленоксидом мутантный сорт Pleurotus eryngii увеличивает экспрессию Pin1 в мозге крыс. Джей Мед Фуд. 2017;20:65–70. doi: 10.1089/jmf.2016.3809. [PubMed] [CrossRef] [Google Scholar]
- Karavan R, Singh T. Разработка Pleurotus ostreatus с этилметилсульфонатом и ультрафиолетовым светом в качестве мутагенов. Int J Mycol Plant Pathol. 2014; 1:55–58. [Google Scholar]
- Каур Л., Капур С. Электрослияние протопластов для создания соматических гибридов между Pleurotus florida и Pleurotus sajor — caju .
 Int J Pharma Bio Sci. 2015;5:507–519. [Google Scholar]
Int J Pharma Bio Sci. 2015;5:507–519. [Google Scholar] - Каур Дж., Содхи Х.С. Молекулярная характеристика мутантных штаммов Calocybe indica с использованием RAPD-PCR. Биоскан. 2012; 7: 527–532. [Google Scholar]
- Каур Дж., Содхи Х.С., Капур С. Селекция Pleurotus florida (вешенки) на фенотипическую пигментацию и высокий потенциал урожайности. J Sci Food Agric. 2008; 88: 2676–2681. doi: 10.1002/jsfa.3389. [CrossRef] [Google Scholar]
- Kim BG, Magae Y, Yoo YB, Kwon ST.Выделение и трансформация урациловых ауксотрофов съедобного базидиомицета Pleurotus ostreatus . FEMS Microbiol Lett. 1999; 181: 225–228. doi: 10.1111/j.1574-6968.1999.tb08848.x. [PubMed] [CrossRef] [Google Scholar]
- Kim MK, Ryu JS, Park KK, Je HJ, Jeong SG, Suk SW, Song WD. Характеристика нового сорта KNR11-1 путем моно-моногибридизации в Pleurotus eryngii . Корейский Soc Mushroom Sci. 2011;15:56. [Google Scholar]
- Kim JK, Lim SH, Kim IJ, Lee YH, Kang HW.
 Мутагенез Pleurotus eryngii под действием гамма-излучения. Корейский J Mycol. 2012;40:93–97. doi: 10.4489/KJM.2012.40.2.93. [CrossRef] [Google Scholar]
Мутагенез Pleurotus eryngii под действием гамма-излучения. Корейский J Mycol. 2012;40:93–97. doi: 10.4489/KJM.2012.40.2.93. [CrossRef] [Google Scholar] - Ким М.К., Рю Дж.С., Ли Ю.Х., Ким Х.Р. Выведение штамма с длительным сроком хранения для коммерческого выращивания путем моно-моно-скрещивания Pleurotus eryngii . Научный Хортик. 2013; 162: 265–270. doi: 10.1016/J.SCIENTA.2013.08.028. [CrossRef] [Google Scholar]
- Кодзима С., Хисано Ю., Миура К.И. Изменение ингибирующих свойств ингибитора 1 протеиназы А Pleurotus ostreatus путем мутации его С-концевой области.Biochem Biophys Res Commun. 2001; 281:1271–1276. doi: 10.1006/BBRC.2001.4515. [PubMed] [CrossRef] [Google Scholar]
- Kumara KLW, Edirimanna ICS. Улучшение штаммов двух сортов вешенки методом двойного культивирования. World Appl Sci J. 2009; 7: 654–660. [Google Scholar]
- Larraya L, Penas MM, Perez G, Santos C, Ritter E, Pisabarro AG, Ramírez L. Идентификация аллелей несовместимости и характеристика молекулярных маркеров, генетически связанных с локусом несовместимости A в грибе белой гнили Pleurotus остриатус .
 Карр Жене. 1999; 34: 486–493. doi: 10.1007/s002940050424. [PubMed] [CrossRef] [Google Scholar]
Карр Жене. 1999; 34: 486–493. doi: 10.1007/s002940050424. [PubMed] [CrossRef] [Google Scholar] - Ларрайя Л.М., Идарета Э., Арана Д., Риттер Э., Писабарро А.Г., Рамирес Л. Локусы количественных признаков, контролирующие скорость вегетативного роста съедобного базидиомицета Pleurotus ostreatus . Appl Environ Microbiol. 2002;68:1109–1114. doi: 10.1128/AEM.68.3.1109-1114.2002. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
- Ларрайя Л.М., Альфонсо М., Писабарро А.Г., Рамирес Л. Картирование геномных регионов (локусы количественных признаков), контролирующих производство и качество в промышленных культурах съедобного базидиомицета Pleurotus ostreatus .Appl Environ Microbiol. 2003;69:3617–3625. doi: 10.1128/AEM.69.6.3617-3625.2003. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
- Lee J-W, Han Y-S, Cheong J-C. Характеристики нового сорта «Хвасон 5хо» в Pleurotus ostreatus . Дж Гриб. 2013; 11: 244–248. doi: 10.
 14480/JM.2013.11.4.244. [CrossRef] [Google Scholar]
14480/JM.2013.11.4.244. [CrossRef] [Google Scholar] - Li H, Wu S, Ma X и др. Геномные последовательности 90 грибов. Научн. отп. 2018; 8:9982. doi: 10.1038/s41598-018-28303-2. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
- Liang ZR, Chang ST (1989) Исследование межродовой гибридизации между Pleurotus sajor — caju и Schizophyllum commune с помощью Protoplast Fusion.В кн.: Грибоведение XII Наука и выращивание съедобных грибов. Брауншвейг, Германия, стр. 12–137
- Liu T, Li H, Ding Y, Qi Y, Gao Y, Song A, Shen J, Qiu L. Полногеномные паттерны экспрессии генов в дикарионе базидиального гриба Pleurotus ostreatus . Браз Дж Микробиол. 2017;48:380–390. doi: 10.1016/j.bjm.2016.12.005. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
- Майти К., Кар Э., Майти С., Гантайт С.К., Дас Д., Майти С., Майти Т.К., Сикдар С.Р., Ислам С.С.Структурная характеристика и изучение иммуностимулирующих и антиоксидантных свойств нового полисахарида, выделенного из водного экстракта соматического гибридного гриба Pleurotus florida и Calocybe indica сорта APK2.
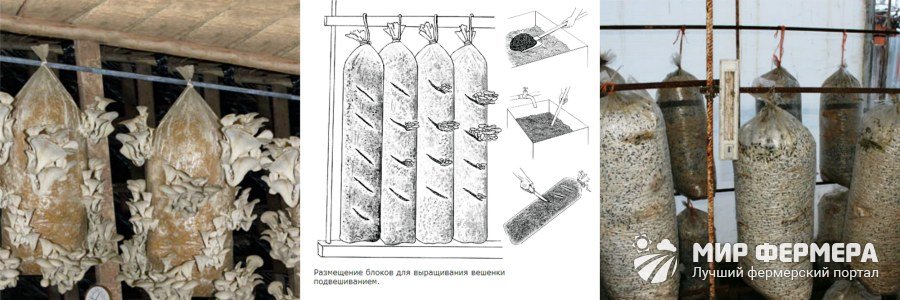 Int J Биол Макромоль. 2011;48:304–310. doi: 10.1016/j.ijbiomac.2010.12.003. [PubMed] [CrossRef] [Google Scholar]
Int J Биол Макромоль. 2011;48:304–310. doi: 10.1016/j.ijbiomac.2010.12.003. [PubMed] [CrossRef] [Google Scholar] - Маллик П., Сикдар С.Р. Получение плодовых тел и характеристика гибридных штаммов съедобных грибов, полученных путем слияния протопластов Pleurotus florida и Lentinus squarrosulus .Int J Pharm Bio Sci. 2015;6:301–314. [Google Scholar]
- Мацумото Т., Фукумаса-Накаи Ю. Наследование митохондриальной ДНК в половых скрещиваниях Pleurotus ostreatus . Карр Жене. 1996; 30: 549–552. doi: 10.1007/s002940050168. [PubMed] [CrossRef] [Google Scholar]
- May B, Henley KJ, Fisher CG, Royse DJ. Отношения сцепления 19 локусов, кодирующих аллозимы, в коммерческом роде грибов Pleurotus . Геном. 1988; 30: 888–895. doi: 10.1139/g88-143. [CrossRef] [Google Scholar]
- Min-Ji O, Ji-Hoon I, Pyung-Gyun S и др.Характеристика и селекция нового сорта Pleurotus ostreatus «Heuksol» J Mushroom. 2017;15:129–133. doi: 10.
 14480/JM.2017.15.3.129. [CrossRef] [Google Scholar]
14480/JM.2017.15.3.129. [CrossRef] [Google Scholar] - Мин-Джи О, Джи-Хун Л, Юн-Ли О и др. Характеристика и селекция сорта Pleurotus citrinopileatus «Jangdari» J Mushroom. 2017;15:73–77. doi: 10.14480/JM.2017.15.2.73. [CrossRef] [Google Scholar]
- Наказава Т., Изуно А., Кодера Р., Миядзаки Ю., Сакамото М., Исаги Ю., Хонда Ю.Идентификация двух мутаций, которые вызывают дефекты в лигнинолитической системе посредством эффективной прямой генетики у агаромицета белой гнили Pleurotus ostreatus . Окружающая среда микробиол. 2017;19:261–272. дои: 10.1111/1462-2920.13595. [PubMed] [CrossRef] [Google Scholar]
- Nantini UR, Selvam M, Singh R. Эффект деградации красителя межродового гибрида между Ganoderma lucidum и Pleurotus florida . Int J Adv Res. 2013;1:112–123. [Google Scholar]
- Обатаке Ю., Мураками С., Мацумото Т., Фукумаса-Накаи Ю.Выделение и характеристика бесспорового мутанта Pleurotus eryngii . Миконаука.
 2003; 44:33–40. doi: 10.1007/S10267-002-0074-Z. [CrossRef] [Google Scholar]
2003; 44:33–40. doi: 10.1007/S10267-002-0074-Z. [CrossRef] [Google Scholar] - Oh MJ, Kim EJ, Jung JH, Shin PG, Kim ES, Oh YL, Jang KY, Kong WS, Yoo YB. Характеристика нового коммерческого штамма «Монгдол» путем внутривидового анастомоза гиф у Pleurotus ostreatus . Дж Гриб. 2015;13:212–216. doi: 10.14480/JM.2015.13.3.212. [CrossRef] [Google Scholar]
- Oh MJ, Shin PG, Oh YL, Jang KY, Sung-I Woo, Kong Won-Sik.Характеристика и селекция нового сорта Pleurotus ostreatus «Soltari» J Mushroom. 2016;14:202–206. doi: 10.14480/JM.2016.14.4.202. [CrossRef] [Google Scholar]
- Okuda Y, Murakami S, Matsumoto T. Карта генетического сцепления Pleurotus pulmonarius на основе маркеров AFLP и локализация области гена для бесспоровой мутации. Геном. 2009; 52: 438–446. doi: 10.1139/G09-021. [PubMed] [CrossRef] [Google Scholar]
- Окуда Ю., Мураками С., Хонда Ю., Мацумото Т.Гомолог MSh5, stpp1, из Pleurotus pulmonarius , является серебряной пулей для решения проблем, вызванных спорами в культивируемых грибах.
 Appl Environ Microbiol. 2013;79:4520–4527. doi: 10.1128/AEM.00561-13. [Статья PMC бесплатно] [PubMed] [CrossRef] [Google Scholar]
Appl Environ Microbiol. 2013;79:4520–4527. doi: 10.1128/AEM.00561-13. [Статья PMC бесплатно] [PubMed] [CrossRef] [Google Scholar] - Пандей М., Равишанкар С. Разработка бесспоровых и низкоспоровых мутантов съедобных грибов для облегчения респираторной аллергии. Curr Sci. 2010;99:1449–1453. [Google Scholar]
- Папазян Л.С. Физиология факторов несовместимости у Schizophyllum commune .Бот Газ. 1950; 112: 143–163. дои: 10.1086/335643. [CrossRef] [Google Scholar]
- Парани К., Эйини М. Улучшение штамма за счет слияния протопластов для усиления деградации кофейной мякоти. Afr J Basic Appl Sci. 2010;2:37–41. [Google Scholar]
- Park B, Kim M-K, Kim HD и др. Разведение Pleurotus eryngii , «Aeryni 5» J Mushroom. 2016;14:94–99. doi: 10.14480/JM.2016.14.3.94. [CrossRef] [Google Scholar]
- Патель Ю., Нараян Р., Сунита К., Аббаси П., Сингх В.К. Новый устойчивый к антибиотикам мутант Pleurotus sajor — caju с улучшенной экспрессией фермента малатдегидрогеназы.
 Int J Adv Life Sci. 2013;6:36–43. [Google Scholar]
Int J Adv Life Sci. 2013;6:36–43. [Google Scholar] - Pyung-Gyun S, Young-Bok Y, Won-Sik K, Chang-Hyun Y, Se-Jong O. Характеристика внутривидовых гибридов путем скрещивания di-mon в Pleurotus eryngii . Дж Гриб. 2004; 2: 109–113. [Google Scholar]
- Ран Ф.А., Хсу П.Д., Райт Дж., Агарвала В., Скотт Д.А., Чжан Ф. Инженерия генома с использованием системы CRISPR-Cas9. Нат Проток. 2013; 8: 2281–2308. doi: 10.1038/nprot.2013.143. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
- Равишанкар С., Пандей М., Тевари Р.П., Кришна В.Развитие бесспоровых/низкоспорящих штаммов Pleurotus посредством мутации. World J Microbiol Biotechnol. 2006; 22:1021–1025. doi: 10.1007/s11274-005-2891-7. [CrossRef] [Google Scholar]
- Роуч К.С., Ферецаки М., Сан С., Хейтман Дж. Однополое размножение. Ад Генет. 2014; 85: 255–305. doi: 10.1016/B978-0-12-800271-1.00005-6. [PubMed] [CrossRef] [Google Scholar]
- Роснина А.Г., Тан Ю.С., Абдулла Н., Викинесвари С.
 Морфологическая и молекулярная характеристика вешенки желтой, Pleurotus citrinopileatus , гибридов, полученных межвидовым скрещиванием.World J Microbiol Biotechnol. 2016;32:18. doi: 10.1007/s11274-015-1959-2. [PubMed] [CrossRef] [Google Scholar]
Морфологическая и молекулярная характеристика вешенки желтой, Pleurotus citrinopileatus , гибридов, полученных межвидовым скрещиванием.World J Microbiol Biotechnol. 2016;32:18. doi: 10.1007/s11274-015-1959-2. [PubMed] [CrossRef] [Google Scholar] - Royse DJ, Baars J, Tan Q. Текущий обзор производства грибов в мире. В: Зиед Д.К., Артуро П.Г., редакторы. Съедобные и лекарственные грибы: технология и применение. 1. Нью-Йорк: Уайли; 2017. С. 5–13. [Google Scholar]
- Сантойо Ф., Гонсалес А.Э., Террон М.С., Рамирес Л., Писабарро А.Г. Количественное картирование ферментативной активности, разлагающей лигнин, у Pleurotus ostreatus .Ферментная микробная технология. 2008;43:137–143. doi: 10.1016/J.ENZMICTEC.2007.11.007. [CrossRef] [Google Scholar]
- Sathesh-Prabu C, Lee Y-K. Генетическая изменчивость и профилирование протеома радиационно-индуцированного мутанта целлюлазы гриба Pleurotus florida . Пол Дж Микробиол. 2016;65:271–277. doi: 10.
 5604/17331331.1215606. [PubMed] [CrossRef] [Google Scholar]
5604/17331331.1215606. [PubMed] [CrossRef] [Google Scholar] - Selvakumar P, Rajasekar S, Babu AG, Periasamy K, Raaman N, Reddy MS. Повышение биологической эффективности штамма Pleurotus за счет слияния протопластов между P.ostreatus вар. флорида и P. djamor var. розовый . Пищевая биотехнология. 2015; 24:1741–1748. doi: 10.1007/s10068-015-0226-5. [CrossRef] [Google Scholar]
- Sharma KK, Kuhad RC. Генетическая трансформация грибов, разлагающих лигнин, облегчается Agrobacterium tumefaciens . БМС Биотехнология. 2010;10:67. дои: 10.1186/1472-6750-10-67. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
- Sharma R, Sharma BM. Улучшение штамма Pleurotus ostreatus с использованием ультрафиолетового света и этилметилсульфоната в качестве мутагенов.Afr J Microbiol Res. 2014; 8: 432–436. doi: 10.5897/AJMR2013.6410. [CrossRef] [Google Scholar]
- Шин П.Г., Ю Ю.Б., Конг В.С., О И.Л. Характеристика и селекция нового сорта Pleurotus eryngii var.
 ferulae, «Beesan No. 1» J Mushroom. 2014;12:52–57. doi: 10.14480/JM.2014.12.1.52. [CrossRef] [Google Scholar]
ferulae, «Beesan No. 1» J Mushroom. 2014;12:52–57. doi: 10.14480/JM.2014.12.1.52. [CrossRef] [Google Scholar] - Шин П.Г., Ю Ю.Б., Конг В.С., О И.Л. Характеристика и селекция нового сорта Pleurotus eryngii var. ferulae, «Beesan No. 2» J Mushroom.2014;12:58–62. doi: 10.14480/JM.2014.12.1.58. [CrossRef] [Google Scholar]
- Shin PG, Oh MJ, Kim ES, Oh YL, Jang KY, Kong WS, Yoo YB. Характеристика и селекция нового сорта Pleurotus ostreatus , устойчивого к изменениям окружающей среды. Дж Гриб. 2016;14:59–63. doi: 10.14480/JM.2016.14.2.59. [CrossRef] [Google Scholar]
- Shu QY, Lagoda PJL. Методы мутации для открытия генов и улучшения урожая. Порода растений Мол. 2007; 5: 193–195. [Google Scholar]
- Сингх М., Камаль С.Генетические аспекты и стратегии получения гибридов. В: Zied DC, Pardo-Gimnez A, редакторы. Съедобные и лекарственные грибы. Чичестер: Уайли; 2017. С. 35–87. [Google Scholar]
- Sonnenberg ASM, Visser MHM, Lavrijssen B, Cone JW, Hendrickx PM (2016) Оценка штаммов королевских вешенок ( Pleurotus eryngii ) по избирательному разложению лигнина в пшеничной соломе: обновление.
Wageningen
- Sunagawa M, Magae Y. Трансформация съедобного гриба Pleurotus ostreatus путем бомбардировки частицами.FEMS Microbiol Lett. 2002; 211:143–146. doi: 10.1016/S0378-1097(02)00635-3. [PubMed] [CrossRef] [Google Scholar]
- Tagavi G, Motallebi-Azar A, Panahandeh J. Характеристики межвидовых гибридов между Pleurotus ostreatus и P . эринги . Russ Agric Sci. 2016;42:230–235. doi: 10.3103/S1068367416030228. [CrossRef] [Google Scholar]
- Тарам Л., Кемро И.К., Пандей С., Марави К.К. Метод получения дикарионов посредством внутривидовых совместимых пар спаривания Pleurotus florida .J Pharmacogn Phytochem. 2018; 1:1838–1842. [Google Scholar]
- Teimoori BB, Pourianfar HR, Moeini MJ, Janpoor J. Химически и физически индуцированный мутагенез в базидиоспорах вешенки Pleurotus ostreatus var. Флорида . Int J Adv Res. 2013;2:915–921. [Google Scholar]
- Терекава Х. Поведение ядер и морфогенез у Pleurotus ostreatus .
 Sci Pap Coll Gen Educ Univ Tokyo. 1957; 7: 61–88. [Google Scholar]
Sci Pap Coll Gen Educ Univ Tokyo. 1957; 7: 61–88. [Google Scholar] - Тойомасу Т., Мори К-И.Формирование плодовых тел продуктов слияния, полученных при межвидовом слиянии протопластов видов Pleurotus . Сельскохозяйственная биохимия. 1987;51:2037–2040. doi: 10.1080/00021369.1987.10868328. [CrossRef] [Google Scholar]
- Upadhyay RC, Verma B, Sood S, Atri NS, Lakhanpal TN, Sharma VP. Документальный фильм об агаромицетных грибах Индии (Отряды — Agaricales, Boletales и Russulales) Дели: Издательство Jaya; 2017. [Google Scholar]
- Vandendries R. De la valeur du barrage sex comme criterium dans l’ analysis spore tetraspolaire de Basidiomycete: Pleurotus ostreatus .Генетика. 1933; 15: 202–212. doi: 10.1007/BF01507332. [CrossRef] [Google Scholar]
- Vereda A, Quirce S, Fernandez-Nieto M, Bartolome B, Sastre J. Профессиональная астма, вызванная спорами Pleurotus ostreatus . Аллергия. 2007; 62: 211–212. doi: 10.1111/j.1398-9995.2006.
 01286.x. [PubMed] [CrossRef] [Google Scholar]
01286.x. [PubMed] [CrossRef] [Google Scholar] - Waltz E. Гриб CRISPR с отредактированным геномом избегает регулирования США. Природа. 2016; 532:293. doi: 10.1038/nature.2016.19754. [PubMed] [CrossRef] [Google Scholar]
- Wang Y, Zeng F, Hon CC, Zhang Y, Leung FCC.Митохондриальный геном гриба Basidiomycete Pleurotus ostreatus (вешенки) FEMS Microbiol Lett. 2008; 280:34–41. doi: 10.1111/j.1574-6968.2007.01048.x. [PubMed] [CrossRef] [Google Scholar]
- Уилсон А.Дж., Сюй Дж. Митохондриальное наследование: разнообразные закономерности и механизмы с упором на грибы. Микология. 2012;3:158–166. doi: 10.1080/21501203.2012.684361. [CrossRef] [Google Scholar]
- Яна К., Йонекура К., Усами Х., Хираяма М., Кадзивара С., Ямадзаки Т., Шишидо К., Адачи Т.Интегративная трансформация Pleurotus ostreatus с использованием устойчивости к биалафосу в качестве доминантного селектируемого маркера. Биоски Биотехнолог Биохим. 1996; 60: 472–475. doi: 10.1271/bbb.60.472. [PubMed] [CrossRef] [Google Scholar]
- Ying FJL, Bolhassan MH, Yeo FKS. Вариации и гибридизационная совместимость отдельных изолятов базидиоспор Pleurotus sajor — caju (Fr.) Sings. Борнео J Resour Sci Technol. 2017;7:47–55. doi: 10.33736/bjrst.392.2017. [CrossRef] [Google Scholar]
- Zhang J, Shi L, Chen H и др.Эффективный метод агробактериальной трансформации съедобного гриба Hypsizygus marmoreus . Микробиолог Рез. 2014; 169:741–748. doi: 10.1016/J.MICRES.2014.01.004. [PubMed] [CrossRef] [Google Scholar]
- Zhang Z, Wen J, Li J, Ma X, Yu Y, Tan X, Wang Q, Liu B, Li X, Li Y, Gong L. Эволюция геномных и эпигеномные особенности у двух грибов Pleurotus . Научный доклад 2018; 8: 8313. doi: 10.1038/s41598-018-26619-7. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
- Zhao J, Chang ST.Межродовая гибридизация между Pleurotus ostreatus и Schizophyllum commune путем индуцированного ПЭГ слияния протопластов. World J Microbiol Biotechnol. 1996; 12: 573–578. doi: 10.1007/BF00327717. [PubMed] [CrossRef] [Google Scholar]
- Zhou X-W. Культивирование Ganoderma lucidum . В: Zied DC, Pardo-Gimnez A, редакторы. Съедобные и лекарственные грибы. Чичестер: Уайли; 2017. С. 385–413. [Google Scholar]
Полное руководство по грибным субстратам
Чтобы успешно выращивать грибы, вам нужно убедиться, что вы используете правильный субстрат.
Использование субстрата для выращивания грибов эквивалентно использованию почвы для выращивания растений. Именно здесь грибы будут получать все свои питательные вещества во время роста.
Точно так же, как растениям требуется почва с разными свойствами, разные виды грибов предпочитают определенные типы субстратов.
К концу этого руководства вы будете знать, что такое грибной субстрат и для чего он используется. Вы узнаете некоторые распространенные рецепты субстрата для грибов и предпочтительные субстраты для разных грибов.Мы также научим вас, как пастеризовать или стерилизовать субстрат и многому другому.
Что такое грибной субстрат? Для чего это используется?
Субстрат для грибов — это материал, в котором грибной мицелий может расти и закрепляться. Субстрат обеспечивает грибы питательными веществами, влагой и энергией, необходимыми им для роста и плодоношения.
Существует множество различных субстратов, которые используют производители. Разные виды грибов имеют свои предпочтения. Поэтому важно сочетать ваши грибы с правильным субстратом, чтобы иметь наилучшие шансы на успех.
Что делает хороший субстрат для грибов?
Хороший субстрат состоит из плотных древесных, волокнистых материалов, таких как лигнин, целлюлоза и гемицеллюлоза. (Они содержат много углерода, который является основным источником пищи для вашего мицелия.) Вот несколько важных вещей, которые следует учитывать при выборе субстрата:
- Ваш субстрат должен содержать от 1 до 2 процентов азота. К большинству субстратов (таких как опилки или солома) необходимо добавить дополнительные материалы, чтобы достичь этого порога.
- Ваш субстрат должен содержать небольшое количество магния, калия, кальция, серы и фосфора. Большинство исходных субстратов уже содержат эти минералы, но это зависит от того, откуда поступил материал. Вам, вероятно, придется поэкспериментировать здесь, чтобы увидеть, нужно ли вам добавлять дополнительные минералы.
- Субстрат должен быть слегка кислым, с уровнем pH около 5–6,5. (Некоторые грибы, такие как вешенки, могут выдерживать рН до 8.)
- Ваш субстрат должен иметь хорошую структуру для обеспечения воздухообмена. Это необходимо для того, чтобы мицелий хорошо заселился.
- Влажность субстрата должна составлять 50-70%.
- . Наконец, в вашем субстрате не должно быть конкурирующих организмов. Это обеспечивает чистый холст для процветания вашего грибного мицелия.
Подготовка основания
Прежде чем засеять субстрат грибными спорами или мицелием, его необходимо подготовить.В субстрат нужно будет добавить воду, а также, возможно, потребуется добавить дополнительные питательные вещества.
После того, как субстрат будет готов, его необходимо стерилизовать или пастеризовать. Это убивает любую конкурирующую плесень или бактерии и дает нужным видам грибов наилучшие шансы закрепиться.
Если такие слова, как прививка или мицелий, кажутся вам ошеломляющими, наша статья Как растут грибы? Подробное объяснение поможет вам освоиться.
Субстрат для грибов можно размещать в различных емкостях. Коммерческие производители чаще всего упаковывают субстрат в большие прозрачные пластиковые пакеты. Домашние производители могут подготовить банки с субстратом для грибов из каменных банок или других небольших контейнеров или упаковать субстрат в ведра.
После того, как ваш субстрат будет пастеризован или стерилизован и помещен в окончательный контейнер, настало время инокуляции грибной икрой или спорами, чтобы начать процесс выращивания.
Вы поймете, что все сделано правильно, когда начнете видеть признаки колонизации или рост и распространение грибного мицелия по субстрату.
Мицелию потребуются недели или, возможно, месяцы, чтобы разложить субстрат и полностью распространиться по нему. После полного завершения колонизации весь субстрат будет покрыт мицелием. В этот момент он готов плодоносить.
Для получения дополнительной информации об остальных этапах выращивания грибов см. Как выращивать грибы: полное руководство .
Общие материалы субстрата для грибов (и рецепты субстрата для грибов)
Существует множество материалов, которые можно использовать в качестве субстрата для выращивания грибов.Некоторые из них довольно традиционны, в то время как другие немного новее и более экспериментальны. Вот некоторые из наиболее распространенных субстратов, которые в настоящее время используют грибоводы.
Кофейная гуща
Здесь, в Grocycle, мы начали с выращивания на кофейной гуще и с тех пор занимаемся этим уже много лет. Если вы обратитесь в местные кофейни, они часто сохранят использованную кофейную гущу и отдадут ее вам бесплатно.
Одним из больших преимуществ является то, что в процессе пивоварения происходит пастеризация гущи, и вы можете сразу же приступить к выращиванию в ней.
Рецепт выращивания в кофейной гуще тоже один из самых простых. Просто смешайте килограмм кофейной гущи со 100 граммами грибной икры. Вы можете дополнительно добавить в смесь 20% соломы для лучшего воздухообмена и более высокой скорости заселения.
Соломинка
Солома — еще один дешевый и эффективный материал для использования в качестве подложки. Его можно купить в фермерских магазинах или в большинстве мест, где можно найти корм для животных или подстилку. Вы также можете поэкспериментировать с подобными сельскохозяйственными отходами, такими как стебли кукурузы.
Вы можете либо выращивать в субстрате, состоящем из 100% соломы, либо добавлять добавки, чтобы обеспечить дополнительные питательные вещества.
Существует несколько способов приготовления субстрата из соломы. Многие используют химические вещества, такие как перекись или гидроксид кальция, или полагаются на ферментацию соломы в течение недели или более. Мы предпочитаем использовать метод нагрева, который является одновременно быстрым и органичным.
Начните с разрезания соломинки на кусочки по три-четыре дюйма. Если вы работаете с большим количеством соломы, может быть проще использовать измельчитель сорняков в мусорном баке, чтобы быстро измельчить материал.
Чтобы пастеризовать соломинку, положите ее в мешок для стирки или наволочку и погрузите в воду с температурой 160 градусов по Фаренгейту на один час. В небольших масштабах это можно сделать в помещении на плите. Для более крупных операций используйте бочку на 55 галлонов и бутановую горелку.
После того, как соломинка готова, ее нужно хорошо высушить. Когда вы сжимаете горсть субстрата для выращивания грибов, должно выйти всего несколько капель воды. В этот момент он готов к инокуляции грибной икрой.
Кокосовая койра и вермикулит
Кокосовая койра — это материал, изготовленный из измельченной скорлупы и шелухи кокосовых орехов.Продается в большинстве садовых магазинов. Вермикулит — это желтовато-коричневый минерал, который используется для удержания влаги, а также повсеместно доступен в садовых центрах.
Смешивание этих двух материалов может создать идеальный субстрат для выращивания некоторых видов грибов.
В большинстве рецептов требуется одна часть кокосовой койры и одна часть вермикулита.
Для стандартного кирпича из сушеной кокосовой койры (около 1,5 фунта) добавьте восемь чашек сухого вермикулита и 16 чашек кипятка.
Замочите материал в пятигаллонном ведре примерно на час. Затем все перемешайте, снова накройте крышкой и дайте остыть в течение четырех часов перед посевом.
Имейте в виду, что кокосовое волокно увеличится в объеме в пять-семь раз, когда вы добавите воду, поэтому в итоге вы получите гораздо больше субстрата, чем кажется на первый взгляд!
Пеллеты из твердой древесины
Все формы твердой древесины, такие как клен, дуб или бук, являются отличным субстратом для нескольких видов грибов.Просто избегайте использования опилок или гранул из хвойных пород деревьев.
Люди используют пеллеты из твердой древесины для печей и грилей, и в настоящее время они продаются в большинстве магазинов древесины. Они довольно недороги, и в большинстве мест вы можете найти 40-фунтовую сумку за 5 долларов.
Вам не нужны более дорогие пеллеты, сделанные из дерева, такого как гикори или яблоки, которые используются для копчения мяса.
Чтобы сделать 10-фунтовый блок субстрата, вам понадобится 10 чашек гранул твердой древесины и 2,8 литра воды. Древесные гранулы не нужно стерилизовать, так как процесс превращения опилок в гранулы означает, что они уже стерилизованы.
Однако большинство производителей добавляют в опилки лиственных пород отруби. Одна только древесина может не содержать питательных веществ, необходимых для выращивания некоторых видов грибов.
Таким образом, можно добавить 2 с половиной чашки пшеничных или овсяных отрубей, чтобы обеспечить мицелий дополнительными питательными веществами. Добавление отрубей означает, что всю смесь необходимо пастеризовать или стерилизовать.
Некоторые фермеры также смешивают древесные гранулы лиственных пород с разным соотношением соевой шелухи для получения аналогичного эффекта.Эту комбинацию часто называют «мастерской смесью», и она может давать впечатляющие урожаи.
Навоз
Мы не считаем навоз идеальной средой для выращивания по очевидным причинам. Вы не хотите регулярно обрабатывать и разогревать экскременты животных. Однако для некоторых видов грибов, таких как обычные шампиньоны, это необходимо.
Для грибов можно использовать конский, куриный, коровий или другой навоз. Рецепты обычно требуют две части навоза с одной частью кокосовой койры.
Затем необходимо добавить воду, чтобы достичь полевой емкости. Это в основном количество воды, которое субстрат может удерживать без дополнительного скопления воды на дне. При легком сжатии вода не должна выходить, а при сильном сжатии должно выделяться всего несколько капель воды.
Затем всю смесь необходимо стерилизовать, прежде чем в нее можно будет инокулировать грибную икру.
Журналы
Да, даже цельные куски дерева можно считать подложкой! Бревна часто используются для выращивания шиитаке и других грибов на открытом воздухе.
Подходит для большинства лиственных пород деревьев, включая бук, тополь, клен, дуб, березу, вяз и другие.
Идеальные бревна для выращивания грибов имеют длину от трех до четырех футов и диаметр от четырех до шести дюймов.
Вы не хотите использовать древесину, которая уже давно мертва или умирает. Другие виды грибков, возможно, уже начали колонизировать древесину, и это может затруднить приживление желаемого мицелия.
Также следует избегать свежесрубленных бревен, поскольку деревья обладают естественными свойствами защиты от грибков, пока они еще живы.Лучше всего хранить свежеспиленные бревна в чистом и сухом месте в течение нескольких месяцев до прививки.
Чтобы инокулировать бревно, в бревне рядами просверливают отверстия от четырех до шести дюймов. Используйте сверло 5/16 или 12 мм для оптимального размера отверстия. Ряды располагаются в шахматном порядке на расстоянии двух-трех дюймов друг от друга.
Мицелий заносится в отверстия с помощью икры пробок. Это небольшие кусочки деревянного дюбеля, заселенные мицелием, которые забиваются в отверстия.Отверстия затем запечатываются воском, чтобы предотвратить загрязнение.
У нас есть статья под названием «Как выращивать грибы на бревнах: полное руководство», в которой более подробно рассматривается весь процесс.
Картон
Картон – хороший субстрат для новичков, которые только начинают заниматься выращиванием грибов в домашних условиях. Это дешево и легко найти. Картон хорошо удерживает влагу, а гофры обеспечивают хороший воздухообмен.
Вешенки и некоторые другие агрессивные виды растут только на картоне, хотя для достижения наилучших результатов полезно смешивать их с кофейной гущей или другими добавками.
Вы даже можете использовать картон, чтобы вырастить грибную икру из стеблей вешенки, которую вы покупаете в продуктовом магазине. Все, что вам нужно сделать, это положить гриб между слоями влажного картона, и мицелий начнет расти.
Выращивание на картоне настолько просто, что вам даже не нужен рецепт. Просто соберите столько картона, сколько хотите использовать, а затем замочите его в кипящей воде.
Дайте вашему картону остыть и отожмите лишнюю воду, и тогда вы будете готовы добавить кусочки грибов, чтобы заселить его.
Как пастеризовать или стерилизовать грибные субстраты
Помимо выбора субстрата для использования, решение о том, когда следует пастеризовать или стерилизовать материал, является еще одной важной частью обучения приготовлению субстрата для грибов.
У некоторых людей есть очень сложные установки для выращивания грибов, которые включают чистые помещения с отрицательным давлением воздуха и дорогостоящим оборудованием.
Однако мы обнаружили, что это делает процесс намного сложнее, чем он должен быть, без существенной выгоды.Поэтому мы выбираем более низкотехнологичный стиль выращивания грибной фермы.
Полное руководство см. в нашей статье «Как создать низкотехнологичную грибную ферму».
Мы обнаружили, что при соблюдении основных процедур стерилизации или пастеризации грибных субстратов вероятность заражения очень мала.
Содержать поверхности в чистоте и протирать их 70% изопропиловым спиртом во время инокуляции – это все, что требуется большинству гроверов.
В чем разница между пастеризацией и стерилизацией субстрата?
Как пастеризация, так и стерилизация субстрата включают нагревание субстрата в попытке уничтожить существующие бактерии или грибки, но при пастеризации субстрат нагревается до 185 градусов по Фаренгейту, а при стерилизации субстрат подвергается воздействию температуры выше 250 градусов по Фаренгейту.
Продолжайте читать, чтобы узнать больше об отличиях.
Как пастеризовать грибной субстрат
Цель пастеризации состоит в том, чтобы очистить субстрат от загрязнений и дать любой грибной культуре хороший старт. Есть два способа пастеризации:
Пастеризация в ванне с горячей водой
Один из способов пастеризации субстрата — просто погрузить его в кипящую воду как минимум на один или два часа. Мы обнаружили, что для большинства операций пастеризации достаточно для выращивания грибов с минимальным риском заражения.
Пастеризация извести холодной водой
Чтобы использовать этот метод, замочите субстрат в ванне с холодной водой, обработанной гашеной известью, на 24 часа. Это увеличивает pH воды, убивая загрязняющие вещества в процессе.
Как стерилизовать грибной субстрат
Стерилизация включает воздействие на подложку температур выше 250 градусов по Фаренгейту, а также помещение подложки под давление. Стерилизация направлена на полное устранение всех загрязняющих веществ, которые могут находиться в субстрате, как живых, так и находящихся в состоянии покоя.
Простое кипячение субстрата не делает его достаточно горячим для полной стерилизации. Для полной стерилизации необходима скороварка или аналогичное оборудование.
Как стерилизовать грибной субстрат без скороварки
Существует несколько способов стерилизации субстрата без использования скороварки.
Также можно использовать процесс, называемый тиндализацией или фракционной стерилизацией. Это достигается кипячением банок или пакетов в течение определенного времени в течение нескольких дней подряд.
Целью этого является уничтожение как любой микробной жизни, которая в настоящее время существует в субстрате, так и любых спор, которым может потребоваться несколько дней, прежде чем они начнут расти.
Все, что подвергает ваш субстрат температуре выше 250 градусов по Фаренгейту в течение длительного периода времени, может стерилизоваться. Это включает помещение субстрата в печь или автоклав.
Однако проблема в том, что он поджаривает субстрат и полностью его высыхает. Некоторые субстраты также могут начать гореть.Если вы стерилизуете свой субстрат таким образом, вам нужно будет использовать дистиллированную воду для его повторной гидратации, сохраняя при этом его стерильность.
Зачем нужна пастеризация или стерилизация?
Пастеризация или стерилизация уменьшают количество плесени и бактерий и помогают гарантировать, что то, что вы пытаетесь вырастить, будет иметь наилучшие шансы прижиться.
Субстрат, на котором любят расти грибы, очень влажный и богатый питательными веществами. Хотя это идеальная среда для грибов, это также идеальные условия для роста других вещей, таких как плесень и бактерии.
Бактерии и плесень могут расти быстрее, чем грибной мицелий. Если оставить их природе, эти загрязняющие вещества превзойдут мицелий и возьмут под контроль субстрат до того, как грибы успеют прижиться в большинстве случаев.
Итак, нам нужно что-то сделать, чтобы дать грибам преимущество и убедиться, что они колонизируют субстрат до того, как это сделают другие формы плесени или грибков.
Пастеризация субстрата для выращивания грибов эквивалентна выдергиванию с грядки как можно большего количества сорняков перед посадкой овощей.Стерилизация больше похожа на выжигание земли и уничтожение всех живых растений и семян в ней.
Нужно ли стерилизовать грибной субстрат?
Для некоторых разновидностей субстрата для грибов необходима стерилизация во избежание загрязнения. Для других видов субстрата можно обойтись только пастеризацией.
Наиболее важным фактором при выборе стерилизации или пастеризации является содержание питательных веществ в субстрате.
Навоз является прекрасным примером субстрата, который всегда следует стерилизовать.По самой своей природе он уже кишит бактериями и микробной жизнью.
Это может показаться не очень привлекательной средой обитания для людей. Но так как он сделан из частично переваренной пищи, он может быть удобным источником пищи для самых разных форм жизни.
Любые материалы субстрата, которые могут считаться пищевыми продуктами, необходимо стерилизовать по тем же причинам. Это включает в себя рожь, попкорн, коричневый рис и ягоды пшеницы.
Все эти субстраты богаты питательными веществами, и на них любят расти все виды различных грибков и плесени.Вы, наверное, наблюдали на своей кухне, как через неделю или две на продуктах начинает расти плесень.
Субстраты с высоким содержанием питательных веществ необходимо стерилизовать, чтобы дать выращиваемым грибам преимущество.
Менее питательные субстраты можно пастеризовать вместо стерилизации. Хорошим примером этого является солома. Солома — это высушенные стебли различных зерновых растений после удаления всего зерна.
Несмотря на то, что в нем все еще есть питательные вещества, он не так богат питательными веществами, как сами зерна.
Кокосовое волокно, бревна и картон также не нуждаются в стерилизации. Пастеризации достаточно, чтобы устранить большую часть конкурентов ваших грибов и дать им фору.
Если вы столкнулись с новым субстратом, который мы здесь не обсуждали, просто задайте себе один вопрос, чтобы узнать, следует ли пастеризовать или стерилизовать этот материал. Это то, что дикое животное съело бы?
Такие вещи, как вермикулит и солома, не являются привлекательным источником пищи для сельскохозяйственных животных или даже грызунов.Между тем животные и даже люди будут есть зерновые, потому что они полны питательных веществ.
На что следует обратить внимание, так это на смешивание субстратов, также известное как их добавление. Вы можете добавить более питательный субстрат к другому, чтобы сделать его более питательным.
Например, добавление навоза в опилки лиственных пород. Древесные гранулы или опилки обычно не требуют стерилизации. Но как только вы дополните его другим материалом, который облегчает рост плесени или бактерий, стерилизация становится необходимой.
Если вы сомневаетесь, вы можете стерилизовать любой субстрат для дополнительной безопасности. Это просто требует дополнительной рабочей силы и оборудования.
Ферментация соломы как альтернатива пастеризации
Вместо пастеризации соломы производители грибов могут ее ферментировать.
Это предполагает погружение мешка с соломой под воду примерно на неделю. Если вы ферментируете целый тюк соломы, вам, вероятно, потребуется погрузить его в воду на более длительный срок, примерно на две недели.
В это время солома начинает разрушаться (ферментироваться) анаэробными организмами. Это виды бактерий, которые могут выжить только в среде без кислорода.
В результате все остальные организмы, которым для выживания обычно требуется кислород, погибают. Как только влажная солома снова подвергается воздействию воздуха, все анаэробные организмы погибают, и солома по существу пастеризуется.
Одна из причин, по которой мы предпочитаем пастеризацию вместо ферментации, заключается в том, что этот метод в буквальном смысле воняет.Подумайте о процессе ферментации таких продуктов, как квашеная капуста, кимчи или чайный гриб.
Это в основном тот же процесс, но с использованием соломы. Если вы используете этот метод, вам следует избегать попадания воды на руки или одежду. Запах очень сложно вывести.
Другим недостатком ферментации вместо пастеризации являются затраты времени и планирования. Когда вы ферментируете, вам нужно предсказать, что потребуется вашему субстрату через неделю или больше.Если вы пастеризуете, ваш субстрат может быть готов к использованию всего за несколько часов.
Как смешать грибной субстрат?
Нет более простого способа смешать субстрат, чем просто перемешать его руками. Конечно, не забудьте тщательно вымыть руки перед началом работы и подумайте о том, чтобы надеть пару одноразовых перчаток.
Для больших партий вы можете использовать большую ложку или даже лопату, в зависимости от того, с каким объемом субстрата вы работаете. Вы также можете использовать стакан для компоста, который мы используем здесь, в GroCyle), или вы можете использовать коммерческий смеситель для субстрата.
Какие субстраты лучше всего подходят для каких видов грибов?
Как мы уже упоминали в этом руководстве, разные типы субстратов лучше всего подходят для разных видов грибов.
Если вы задаетесь вопросом: «Какой лучший субстрат для грибов?» К сожалению, у нас нет универсального ответа, применимого ко всем ситуациям. Если бы это было так просто, каждый грибник использовал бы только один идеальный субстрат!
Некоторые виды грибов, такие как вешенки, очень агрессивны и могут колонизировать самые разные материалы.Другие предпочитают подложки на древесной основе.
Некоторые разновидности грибов, такие как трюфели, даже предпочитают расти на корнях живых деревьев, что, как известно, затрудняет их выращивание в коммерческих условиях.
Выбор подложки
Выбор субстрата сводится к нескольким вариантам:
- Сколько времени и денег вы хотите потратить на выращивание грибов? Если вы хотите сэкономить время и деньги, обратите внимание на пастеризованные субстраты, не добавляя их и выбирая виды, которые хорошо растут на этих субстратах.
- Это наш подход в GroCycle, и он очень хорошо масштабируется.
Если вы хотите выращивать широкий ассортимент грибов для гурманов в промышленных масштабах и готовы инвестировать больше времени и денег, обратите внимание на материалы с добавками и метод обработки паром и стерилизации материалов.
Это позволит вам выращивать множество видов грибов.
- Какой субстрат доступен для вас? По логике, вам нужно выбрать носитель, доступный вам локально.Например, если там, где вы живете, мало соломы, вы можете попробовать кокосовое волокно.
Низкотехнологичный грибной субстрат
Если вы решили пойти по низкотехнологичному пути выращивания грибов, хорошие варианты субстрата включают солому, гранулы из соломы, гранулы из опилок, мульчу из сахарного тростника и кофейную гущу. Мы рассмотрим некоторые из них более подробно ниже.
Солома
Солома не очень питательна, поэтому подходит не для всех видов грибов. Однако он может быть весьма эффективным для выращивания видов вешенки.
Другие виды грибов, которые могут расти на соломе, включают и виды гарикусов, винный колпак (также известный как садовый великан), мохнатую гриву и эноки.
Бревна или опилки
Существует большое разнообразие съедобных и лекарственных лесолюбивых грибов. К ним относятся шиитаке, майтаке, индюшачий хвост, львиная грива и рейши . Некоторые виды вешенок также хорошо растут на древесине. Особенно королевские вешенки, которые в качестве субстрата предпочитают древесину, а не солому.
Большинство грибов, которые хорошо растут на бревнах, также будут расти на гранулах из древесных опилок или наоборот, поскольку оба субстрата основаны на древесине.
Помните, что если вы используете бревна, они должны быть достаточно свежими. Бревна, которые уже мертвы или гниют, уже могут стать домом для диких грибков и плесени.
Бревна не нужно стерилизовать перед использованием. Но имейте в виду, что, поскольку они являются более естественным субстратом для выращивания грибов, они могут быть домом для других видов грибов, которые могут производить ядовитые грибы.Это редкость.
Но убедитесь, что вы знаете, как определить вид грибов, которые вы выращиваете, и позаботьтесь о том, чтобы другие виды не смешались по ошибке.
Дополненные опилки
Если вы хотите выращивать более широкий ассортимент грибов на стерилизованном субстрате, попробуйте смесь опилок с добавками: 60% опилок лиственных пород, 20% древесной щепы, 18% отрубей и 2% гипса.
Мастерс Микс
Masters Mix, разработанный в Earth Angel Mushrooms, представляет собой еще один вариант простого субстрата, который на 50% состоит из пеллет лиственных пород и на 50 % из соевых бобов.Это имеет тенденцию давать очень хорошие урожаи, но требует стерилизации.
Если вы находитесь в Соединенных Штатах, вы можете купить уже изготовленные пакеты в Mushroom Media Online.
Навоз
Вы можете подумать, что навоз — идеальная среда для выращивания грибов. Однако большинству видов съедобных грибов это не нравится. Основными исключениями являются шампиньоны, кримини и портобелло .
На самом деле это одни и те же виды грибов на разных стадиях жизни.
Кофейная гуща
Мы рекомендуем выращивать вешенки только на кофейной гуще. Это проверенная комбинация.
Некоторые другие виды грибов, такие как шиитаке, также могут расти на кофейной гуще, но могут давать не такой хороший урожай, как выращивание на твердой древесине.
Смеси
Некоторые материалы, такие как вермикулит, сами по себе не имеют пищевой ценности. Однако их можно смешивать с другими материалами, такими как кокосовая койра или зерно, чтобы обеспечить лучшее удержание влаги или другие качества.
Эксперименты с различными смесями субстрата — это то, что вы можете попробовать, если уже какое-то время выращиваете грибы.
Однако, когда вы только учитесь делать субстрат для грибов, мы рекомендуем начинать с одного субстрата, пока вы не сможете получать стабильный урожай.
Дополнение субстрата
Если вы думаете о выращивании грибов в коммерческих целях, вы можете дополнить свой субстрат, чтобы увеличить урожай грибов.Чаще всего добавками являются производные отрубей или семян.
Или вы можете получить их в виде гранул в качестве высокобелкового корма для животных. Последний предпочтительнее, так как он уже пастеризован.
Вам нужно будет поэкспериментировать, чтобы узнать, сколько добавки добавить, и это количество также будет зависеть от того, стерилизован ли материал, который вы добавляете. Мы рекомендуем начинать с 5% и постепенно увеличивать.
Что делать с отработанным грибным субстратом
Если вы выращиваете грибы какое-то время, вскоре у вас останутся большие кучи отработанного субстрата.Это может заставить вас задаться вопросом: «Что я могу сделать со старым субстратом для грибов?» Самый распространенный вариант для грибоводов — это компостирование.
Можно смешать с существующей компостной кучей. Или вы можете создать компостную кучу из только что использованного субстрата, который со временем естественным образом разложится и превратится в богатый компост.
Если у вас есть сад, вы даже можете смешать использованный субстрат прямо с почвой.
Некоторые крупные коммерческие производители даже перерабатывают свой грибной субстрат и продают его в качестве компоста домашним садоводам.
Если вам повезет, вы можете получить несколько дополнительных сборов грибов из вашей компостной кучи или сада. Некоторые виды, такие как вешенки, могут даже прижиться и распространиться, и вы будете получать бесплатные грибы, растущие в вашем саду год за годом.
Часть вашего использованного субстрата также можно использовать для инокуляции новой партии субстрата. Таким образом, вам не нужно будет покупать грибную икру у поставщиков, и вы сможете вести действительно самодостаточную деятельность. Тем не менее, такая низкотехнологичная грибная ферма может привести к несколько более высоким случаям заражения.
Если вы фермер, у которого много места, вы можете легко утилизировать использованный субстрат самостоятельно. А как же люди, которые выращивают грибы в городе?
В настоящее время во многих городах действует бесплатная программа компостирования. Вы можете выбрасывать использованный субстрат в компостные ящики, которые опорожняются каждую неделю.
Или вам может потребоваться отвезти использованный субстрат на городской склад, где обрабатываются садовые отходы, компост и другие вторсырья, чтобы сдать его самостоятельно.
Если в вашем городе нет способа переработки вашего субстрата, вы можете обратиться к ближайшим фермерам. Возможно, они захотят добавить использованный вами субстрат в свои компостные кучи и позволят вам бесплатно его сдать.
Были даже исследования по использованию грибных субстратов в качестве ингредиента кормовых смесей для кур и крупного рогатого скота.
Последние мысли
Выбор правильного субстрата и его правильная подготовка для конкретного типа грибов, которые вы выращиваете, имеет решающее значение для вашего успеха.
Некоторые виды, такие как вешенки, могут расти на самых разных субстратах, включая солому или даже картон. Другие виды более специфичны и дают высокие урожаи только при выращивании на определенном субстрате.
После того, как вы выбрали правильный субстрат, вам необходимо либо пастеризовать, либо стерилизовать его, чтобы свести к минимуму риск роста плесени и бактерий. Эта часть процесса поможет вашему мицелию закрепиться.
После того, как ваши грибы закончат плодоношение, вы можете утилизировать отработанный субстрат, компостируя его.
Теперь вы знаете, как создать идеальный субстрат для ваших грибов. Пора расти!
Выращивание вешенки (Pleurotus spp.) на различных лигноцеллюлозных отходах
Массачусетс Ахмед (1994) Выращивание вешенки EditionNumber1 Комета Ко. Каир, Египт 63
Google Scholar
К.А. Азизи Т.Р. Шамала К.Р. Шрикантия (1990) СтатьяЗаголовокВыращивание Pleurotus sajor-caju на некоторых агропромышленных отходах и использование отходов для производства целлюлозы и d-ксиланазы Грибной журнал для тропиков 10 21–26
Google Scholar
П.Баджпай (1997) СтатьяЗаголовокМикробная ксиланолитическая ферментная система: свойства и применение Достижения в области прикладной микробиологии 43 141–194 Вхождение Ручка14
ПабМед Google Scholar
З.Бано М.Н. Шасирека С. Раджаратнам (1993) СтатьяЗаголовокУлучшение эффективности биоконверсии и биотрансформации вешенки ( Pleurotus sajor-caju) путем добавления в рисовую солому жмыха масличных семян Ферментные и микробные технологии 15 985–989
Google Scholar
П.Бобек О. Оздин М. Микус (1995) СтатьяЗаголовокПищевой вешенка ( Pleurotus ostreatus) ускоряет обмен холестерина в плазме у крыс с гиперхолестеринемией Физиологические исследования 44 287–291 Вхождение Ручка8869262
ПабМед Google Scholar
П.Бобек Л. Оздин С. Гальбави (1998) Статья НазваниеЗависимое от дозы и времени гиперхолестеринемическое действие вешенки ( Pleurotus ostreatus) у крыс Питание 14 282–286 Вхождение Ручка9583372
ПабМед Google Scholar
Дж.А. Басуэлл Ю.Дж. Кай С.Т. Чанг Дж.Ф. Пеберди С.Ю. Фу Х.С. Ю (1996) СтатьяЗаголовокПрофили лигноцеллюлолитических ферментов съедобных грибов Всемирный журнал микробиологии и биотехнологии 12 537–542
Google Scholar
С.Канжи А. Равноправно (1995) СтатьяЗаголовокИсследования производства Pleurotus на жоме сахарного тростника Африканский журнал микологии и биотехнологии 3 67–79
Google Scholar
Р.Коэн Л. Перский Ю. Хадар (2002) СтатьяЗаголовокБиотехнологические применения и потенциал разрушающих древесину грибов рода Pleurotus Прикладная микробиология и биотехнология 58 582–594 Вхождение Ручка11956739
ПабМед Google Scholar
Хоссейн С., Hashimoto, M., Choudhury, E., Alam, N., Hussain, S., Hasan, M., Choudhury, S. & Mahmud, I. 2003 Пищевой гриб ( Pleurotus ostreatus) улучшает атерогенные липиды у крыс с гиперхолестеринемией. . Клиническая и экспериментальная фармакология и физиология 30 , 470
Google Scholar
Р.А. Курцман СуффиксJr.(1994) Пищевые потребности грибов и субстратов М.К. Наир Г. Гопалапалан Д. Лулу (ред.) Достижения в биотехнологии грибов Научные издательства Джодхпур 106–110
Google Scholar
В.Мехта Дж.К. Гупта С.К. Каушал (1990) СтатьяЗаголовокВыращивание гриба Pleurotus florida на рисовой соломе и получение биогаза из отработанной соломы Всемирный журнал микробиологии и биотехнологии 6 366–370
Google Scholar
Патил Б.Д. и Джадхав, С.В. 1991 Урожайность Pleurotus sajor-caju на различных субстратах. In Indian Mushrooms . Труды Национального симпозиума по грибам. стр. 84–86. Тируванатхапурам, Индия: Керальский сельскохозяйственный университет.
Т.Х. Кимио С.Т. Чанг Д.Дж. Ройс (1990) СтатьяЗаголовокТехнические рекомендации по выращиванию грибов в тропиках ФАО Растениеводство и защита 106 62–70
Google Scholar
А. Ремтулла (1993) СтатьяЗаголовокИспользование лигноцеллюлозных остатков для выращивания Pleurotus sajor-caju Макилвейни 11 40–43
Google Scholar
Д.Дж. Ройс (1992) СтатьяЗаголовокПереработка использованного субстрата шиитаке для производства вешенки Pleurotus sajor-caju Прикладная микробиология и биотехнология 38 179–182
Google Scholar
А.Санчес Ф. Исунза М. Бельтран-Грация М. Эскеда (2002) СтатьяЗаголовокБиодеградация отходов виноградарства под действием Pleurotus: источник пищи для микробов и человека и его потенциальное использование в качестве корма для животных Журнал сельскохозяйственной и пищевой химии 50 2537–2542 гг. Вхождение Ручка11958618
ПабМед Google Scholar
С.Саксена Р.Д. Рай (1992) СтатьяЗаголовокВлияние азота на продукцию внеклеточных ферментов деградации Pleurotus sajor-caju (Fr.) Singer на пшеничной соломе Исследование грибов 1 45–48
Google Scholar
С.Шарма М. Мадан (1993) СтатьяЗаголовокМикробный белок из бобовых и небобовых субстратов Acta Biotechnologica 13 131–139
Google Scholar
А.К. Сингх (1998) СтатьяЗаголовокВыращивание вешенки ( Pleurotus spp.) на остатках сахарного тростника Журнал микологии и патологии растений 28 24–245
Google Scholar
С. Сото-Веласко Я.Альварес (1995) СтатьяЗаголовокПроизводство плодовых тел Pleurotus spp. на жоме сахарного тростника после обработки гидроксидом натрия Африканский журнал микологии и биотехнологии 3 61–66
Google Scholar
Г.В. Томас С.Р. Прабху М.З. Рини Б.М. Бопайя (1998) СтатьяЗаголовокОценка лигноцеллюлозной биомассы кокосовой пальмы в качестве субстрата для выращивания Pleurotus sajor-caju (Fr.) Певица Всемирный журнал микробиологии и биотехнологии 14 879–882
Google Scholar
Ф. Задразил Р.Х. Курцман СуффиксJr. (1982) Биология выращивания Pleurotus в тропиках С.Т. Чанг Т.Х. Кимио (ред.) Тропические грибы, биология, природа и методы выращивания Издательство китайского университета Гонконг 277–298
Google Scholar
(PDF) Селекция и разведение королевской вешенки
Три штамма королевской вешенки, Pleurotus eryngii (DC.:Fr.) Quél., были выращены с использованием системы культивирования в бутылках для оценки коммерческого производства. Это были штаммы АТСС 36047, АТСС и Holland 150. Один из них, а именно штамм АТСС 36047, показал высокий потенциал для коммерческого производства. Этот сорт давал средние и крупные плодовые тела с отличными характеристиками, твердой и тонкой текстурой и длительным сроком хранения, в то время как сорт Holland 150 плодоносил быстро и в основном давал крупные плодовые тела с хорошими характеристиками, мягкой и тонкой текстурой, а также короткий срок хранения.Последний имеет более высокую биологическую эффективность, чем штамм ATCC 36047, но при высокой относительной влажности образовывал много бородавок на поверхности шляпки. Для получения высокопродуктивного штамма, способного давать высококачественные плодовые тела, были выделены монокарионы из штаммов АТСС 36047 и Holland 150, а также определены их факторы спаривания. Проводили скрещивание между монокарионами, полученными из двух штаммов, и скрининг полученных таким образом гибридов. Четыре высокопродуктивных гибрида, т.е.Были получены B112, B012, B030 и B011. Гибрид B1l2 давал крупные плодовые тела с маленькой шляпкой, равной веретеновидной ножкой, средней мягкости и мелкой текстурой. Гибрид B012 давал крепкие плодовые тела с заметной эксцентричной или боковой ножкой и веерообразной шляпкой, на поверхности которой образовывались бородавки в условиях высокой влажности. Его ножка была ровной и твердой и состояла из белой и очень тонкой текстуры. Гибрид В030 дал тонкие плодовые тела среднего размера, с округлой шляпкой, ровной и прочной ножкой.Этот гибрид был склонен давать много мелких плодовых тел, когда влажность в помещении для выращивания не контролировалась должным образом во время выращивания. Гибрид B011 был склонен давать крепкие плодовые тела с большой шляпкой и белой твердой ножкой. У этих продуктивных гибридов гриба от инокуляции до конца урожая прошло от 54,4 до 60 дней, и они по-разному реагировали на состав субстрата в аспекте продуктивности.
Остатки кукурузы в качестве жизнеспособного субстрата для выращивания вешенки (Pleurotus ostreatus) в фермерских масштабах
и стебель кукурузы, каждый из которых был дополнен рисовыми отрубями, оценивались как среда для выращивания вешенки Pleurotus ostreatus (Kummer).Для испытанных альтернатив опилкам масса собранных плодовых тел, которые проросли на килограммовой среде из кукурузной шелухи на урожай (32,99 г), была самой высокой. Среда из опилок поддерживала значительно () более тяжелые плодовые тела (42,18), чем остатки кукурузы. Пиковые урожаи грибов для различных субстратов были получены между первым и седьмым приливами плодовых тел. Биологическая эффективность субстратов, в которой измерялись полезные питательные вещества, показала, что стебли кукурузы, дополненные рисовыми отрубями, составляли 39% по сравнению с опилками (60%).Среда из шелухи кукурузы и среда из початков кукурузы имели биологическую эффективность 32% и 9,5% соответственно. Эти результаты показывают, что две протестированные среды для выращивания (стебель кукурузы или шелуха) дали грибы с характеристиками урожайности, сравнимыми с хорошо используемыми опилками при выращивании вешенки. Экологические и экономические параметры, связанные с использованием и транспортировкой опилок, делают эти остатки сельскохозяйственных культур жизнеспособной альтернативой для выращивания грибов в особенно нелесных зонах Ганы.
1. Введение
К съедобным грибам относятся грибы, которые размножаются только на влажных разлагающихся органических веществах или в сочетании с почвой [1], поскольку они зависят от питательных веществ, полученных из мертвых и разлагающихся материалов. Грибы использовались в пищу и в медицине и часто считались роскошной пищей, предназначенной для элиты [2]. Мировое производство грибов значительно возросло: с 0,3 млн тонн в 1961 году до 3,41 млн тонн в 2010 году [3, 4]. Китай является ведущим производителем грибов в мире, производя около 65% мировых грибов и 85% вешенок в мире [3].Африка производит только 1% от общего мирового производства вешенки [5].
Вешенка ( Pleurotus ostreatus, Kummer) является вторым по величине коммерчески производимым и важным съедобным грибом на мировом рынке [6] после грибов Agaricus . Это самый популярный гриб, культивируемый в Гане, а также хорошо растет в других тропических и субтропических регионах [7]. P. ostreatus обладает уникальной адаптацией к широкому спектру лигноцеллюлозных субстратов [2, 8]; следовательно, нередко можно найти дикие вешенки, прорастающие естественным образом группами на мертвых деревьях.Это также простой и экономичный гриб для выращивания [8]. Вешенка употребляется в пищу из-за ее вкусовых и лечебно-питательных свойств [8]. Он содержит белки, витамины и сырую клетчатку и благодаря своим свойствам ловастатина [6] был рекомендован пациентам с заболеваниями, связанными с холестерином [4, 7, 9]. Считается, что вешенка может предотвратить высокое кровяное давление, запор и похмелье, а также может помочь в восстановлении от усталости, и снова она используется в качестве кондиционера почвы в сельском хозяйстве [2].
Вешенки выращивают с использованием бревен или контейнеров, таких как полки, ящики, мешки и бутылки, содержащие среду для выращивания [2]. Различные растительные остатки использовались при производстве вешенки либо в качестве основного субстрата, либо в сочетании с добавками [10]. Вешенку можно выращивать на различных субстратах, включая рисовую солому, стебли/початки кукурузы, растительные остатки, багассу [11, 12], опилки, пшеничную солому, хлопковые отходы, макулатуру и стебли хлопка [13, 14].Предпочтительный метод выращивания зависит от сорта грибов, рыночного спроса, предпочтений фермера и наличия среды для выращивания [15].
В Гане вешенки выращивают с использованием пластиковых пакетов, наполненных разложившимися опилками [16]. Однако по мере того, как древесина (древесина) становится дефицитной, отсутствие подходящего субстрата из опилок становится ограничивающим фактором для выращивания грибов в Гане. Кроме того, лесная промышленность, производящая опилки в качестве побочного продукта деревообрабатывающих предприятий, ограничена лесными зонами.Таким образом, производители грибов за пределами лесных зон сталкиваются с проблемой стоимости перевозки опилок, что увеличивает себестоимость продукции. Разработка методов выращивания, в которых используются другие устойчивые источники субстрата для выращивания вешенки, может заполнить пустоту в опилках и, вероятно, будет принята грибоводами.
Использование остатков кукурузы в качестве субстрата для вешенки в контролируемых условиях описано Atikpo et al. [15], Ободаи и соавт.[16] и Onyango et al. [5]. Кукуруза является одной из основных сельскохозяйственных культур, выращиваемых в Гане, и ее остатки (шелуха, початки и стебли) имеются в изобилии и доступны в течение года и могут использоваться в качестве устойчивого субстрата для выращивания грибов. Экстраполяция результатов лабораторного выращивания [5, 15, 16] грибов на остатках кукурузы должна быть проверена в полевых условиях с использованием выращенных в домашних условиях сортов сельскохозяйственных культур, прежде чем ее можно будет рекомендовать местным фермерам. В этом исследовании изучалась относительная эффективность местных остатков кукурузы (початков, шелухи и стеблей) при выращивании вешенки в фермерских полевых условиях.Также был определен потенциал этих субстратов и других добавок для поддержки выращивания вешенки.
2. Материалы и методы
2.1. Источник субстратов и икры
Исследование проводилось на ферме BenCom в Течимане в регионе Бронг Ахафо в Гане в период с марта по июль 2011 года. Ферма BenCom, расположенная на 7,5772° с. ш., 1,9292° з. около 2500 тонн грибов ежегодно. Икра Pleurotus ostreatus была получена на фермах BenCom.Опилки неизвестных пород древесины были собраны с местной лесопилки на лесном рынке Течиман. Остатки кукурузы (шелуха, початки и стебли) были в изобилии доступны у местных фермеров.
2.2. Подготовка субстрата для выращивания
Десять (10) кг опилок смешивали с 0,5% извести для поддержания pH. Смесь увлажняли до достижения влажности 70%. Затем смесь складывали в пирамидальную форму и повторно перемешивали с интервалом в 4 дня для обеспечения хорошей аэрации. Смесь была достаточно ферментирована и готова к расфасовке через 28 дней.Кукурузную шелуху и стебли нарезали на кусочки длиной примерно 4 см, а початки измельчали примерно до 0,5–4 см. Затем каждый из остатков замачивали в избытке воды на 12 часов. Избыток воды сливали, а влажный остаток сушили на солнце в течение одного часа, чтобы получить субстрат из остатков кукурузы. При лечении добавками добавляли 840 г рисовых отрубей. Каждая подложка была расфасована партиями по одному килограмму с использованием термостойких пропиленовых пакетов размером 33 × 18 см. Трубы из поливинилхлорида (ПВХ) использовались для придания жесткости горлышкам мешков, и их стерилизовали при 100°C в течение 4 часов в металлическом барабане над открытым пламенем и давали остыть перед использованием.
2.3. Нерест, инкубация и плодоношение
Субстраты в мешках помещали в стерилизованную комнату, и в каждый 1-килограммовый мешок инокулировали 50 г грибной икры, получая 5% икры. Для усиления роста мицелия использовали метод тщательного нереста, при котором икра полностью смешивалась с субстратом. Мешки накрывали стерилизованной ватой, а затем бумагой, которую закрепляли резинкой. Инкубировали при 26-28°С в течение 20-34 дней в хорошо проветриваемом помещении.Каждую обработку повторяли пять раз. Мешки были перемещены в теплицу для плодоношения, когда мицелий полностью вырос. Кольца из ПВХ, хлопковые пробки и бумагу удаляли для улучшения аэрации и стимуляции закрепления, когда стенки мешков были полностью заселены. На мешочках также делали отверстия для появления плодовых тел. Температуру и влажность регулировали смачиванием бетонного пола и нерестовых мешков.
2.4. Сбор данных и анализ
Плодовые тела вынимали и регистрировали количество грибов и их свежий вес каждые шесть дней в течение 6 недель подряд.Минимальный период (6,33 дня) между приливами, о котором сообщают Bhatti et al. [17] был принят. Общее количество плодовых тел, общее количество смывов, выход каждого мешка и общий выход (г) грибов рассчитывали после периода выращивания. После последней уборки определяли сухую массу отработанного субстрата, выдерживая его под прямыми солнечными лучами до тех пор, пока не прекратится изменение массы в течение 3 дней подряд. Биологическую эффективность (БЭ) каждой обработки рассчитывали по формуле: Массу и количество грибов перед статистическим анализом преобразовывали по квадратному корню.Данные подвергали дисперсионному анализу (ANOVA) с использованием GenStat 9-го издания. Среднее разделение было выполнено с использованием наименьшей значимой разницы, и эффекты были объявлены значимыми на уровне 5%.
3. Результаты
Количество плодовых тел вешенки значительно зависит от различных субстратов. Четыре субстрата: опилки, шелуха кукурузы, стебли кукурузы и початки кукурузы значительно повлияли на количество плодовых тел гриба (рис. 1). В субстрате из стеблей кукурузы зафиксировано самое высокое среднее количество плодовых тел на урожай (5.17), а кукурузная шелуха имела самый низкий показатель 3,38, что значительно отличалось от других субстратов (рис. 3). Каждый из субстратов в течение 7-недельного периода сбора урожая имел разные периоды пиковой численности плодовых тел грибов. Опилки, традиционный субстрат для выращивания грибов в данной местности, и шелуха кукурузы дали самый высокий прилив плодовых тел в первую неделю сбора урожая (рис. 1), в то время как початки кукурузы и стебли кукурузы имели самые высокие пики в течение четвертой недели. Добавление субстратов значительно повлияло на количество плодовых тел, проросших на урожай.Среднее количество плодовых тел, полученных в каждом субстрате отдельно, было ниже, чем при добавлении в него рисовых отрубей. Среди субстратов, в которые были добавлены рисовые отруби, кукурузная шелуха давала наибольшее среднее количество плодовых тел (2,15) за период сбора урожая, за ней следовали стебли кукурузы (2,06), а наименьшее — початки кукурузы, которые давали 1,28 плодовых тел.
Субстраты значительно повлияли на сырой вес произведенных грибов (Рисунок 4). Опилки зафиксированы значительно () выше (42.18 г) свежих грибов на килограмм субстрата в урожае, за ними следуют стебли кукурузы (32,99 г), шелуха кукурузы (27,55 г) и значительно низкий вес грибов из субстрата кукурузных початков (18,67 г). Пятый период сбора урожая дал самую высокую массу свежих грибов, а наименьшую — во второй период сбора урожая (рис. 2). Самая высокая масса свежих грибов, собранных с субстрата, была зафиксирована на стебле кукурузы в течение первой недели сбора урожая (рис. 2). В субстратах с добавлением рисовых отрубей самый высокий показатель (92.2 г) вес свежих грибов на килограмм субстрата (рис. 4), но существенно не отличался ни от початка кукурузы (29,2 г), ни от шелухи кукурузы (42,8 г), ни от стебля кукурузы (32,7 г).
Биологическая эффективность (БЭ), которая является функцией степени использования питательных веществ субстрата, значительно различалась между субстратами. Опилки имели самую высокую биологическую эффективность 60,1%, а початки кукурузы имели самую низкую 14%. Из дополненных субстратов стебель кукурузы показал самую высокую биологическую эффективность 39.2%, затем кукурузная шелуха. Початки кукурузы имеют самую низкую биологическую эффективность 9,5% (рис. 5).
4. Обсуждение
Несколько съедобных грибов были успешно выращены на коммерческом уровне во всем мире с использованием отходов лигноцеллюлозы в качестве субстрата [18]. Идеальный субстрат должен содержать азот (добавка) и углеводы для быстрого роста грибов [19]. Сообщалось, что различные растительные остатки использовались при производстве вешенки либо в качестве основного субстрата, либо в сочетании с добавками [10].Вешенки можно выращивать на различных субстратах, включая рисовую солому, стебли/початки кукурузы, растительные остатки, багассу [12], пшеничную солому [13], отходы хлопка, макулатуру и стебли хлопка, которые подходят для высокой производительности для вешенка [14].
Реакция различных используемых субстратов показывает различия в отношении времени, необходимого для образования булавочных головок, созревания плодовых тел, периода между приливами, количества приливов и урожайности. Lozano [20] сообщил, что в течение 60 дней было проведено семь уборок, тогда как Jiskani [21] сообщил о 7.5 дней между приливами и Бугио [22] зафиксировали 9–15 дней между приливами. Было 7 приливов в течение 42 дней для всех субстратов, протестированных в этом эксперименте, исходя из выбранной нами скорости нереста 5%. Количество и частота смывов зависят от темпов нереста. Минимальный период между поливами 6,33 дня был принят при нерестовости 2%, а период 16,72 дня при нересте 10% [17]. Однако при использовании коэффициента нереста 1% в пересчете на сухую массу был получен только один смыв [20].
По общему мнению, второй сброс будет самым большим.Нередко первый поток бывает самым большим, а при небольшом количестве субстратов третий поток иногда может быть самым большим [23]. Число слива с наивысшим выходом в этом эксперименте не было определено, так как каждый субстрат имел свой пик в разные периоды. В среднем пятый период сбора давал наибольшую массу свежих грибов, а наименьший — во второй период сбора, что противоречит общему опыту, представленному в [23]. Результаты показали, что протестированные побочные продукты из кукурузы при выращивании вешенки влияли на вес полученного гриба, как сообщает Mendez et al.[11]. При выращивании вешенки в полевых условиях собранные плодовые тела дают только 9 г/кг субстрата [13] по сравнению с ~42 г/кг, зарегистрированными для опилок в этом эксперименте. Сообщается, что опилки являются лучшим субстратом для роста и плодоношения мицелия [24]. Высокий вес собранных грибов при обработке опилками может быть связан с хорошей аэрацией, как сообщают Чанг и Майлз [25], что на производство грибов влияет состав субстрата и степень аэрации.Пригодность субстратов была также подтверждена их сопоставимой биологической эффективностью с традиционными опилками. Известно, что питательные компоненты грибных субстратов влияют на рост мицелия [26]. Вешенки обладают способностью использовать биомолекулы для своего роста [27]. Высокопитательный субстрат также улучшает вегетативный рост мицелия, что приводит к интенсивному росту и позднему прищипыванию [28].
Содержание липидов в этих остатках не тестировалось в текущем эксперименте; однако, согласно Naraian et al.[29] Стебли кукурузы содержат более высокие липидные компоненты, чем початки и шелуха. Липиды, присутствующие в стеблях кукурузы, возможно, способствовали высокой биологической эффективности 44,4% (60,1% для опилок), которая представляет собой полезные и доступные питательные вещества в среде для выращивания. Однако в других отчетах биологическая эффективность достигала примерно 90–97 % через 50–60 дней при коэффициенте нереста 10 % [30] по сравнению с 5 %, используемыми здесь. Хотя коэффициент нереста 25% оказался лучше, Fan et al. [30] рекомендовали коэффициент нереста 10% с точки зрения экономики процесса, в то время как Bhatti et al.[17] также рекомендовали норму нереста 7% в пересчете на сухую массу, так как это приводило к раннему и высокоурожайному урожаю вешенки с минимальным периодом созревания плодовых тел, максимальным количеством махов и плодовых тел. Добавление субстратов стало одним из основных методов выращивания грибов. Идеальный субстрат должен содержать азот (добавка) и углеводы для быстрого роста грибов [19]. Рисовые отруби оказались подходящим материалом для добавления остатков кукурузы в качестве субстрата.Это повысило биологическую эффективность всех субстратов, кроме початков кукурузы. Айоделе и Акпая [31] сообщили, что добавление в опилки волокон масличной пальмы может увеличить рост мицелия и выход спорофоров древесных ушных грибов.
5. Заключение
Исследование показало, что стебли кукурузы потенциально пригодны для коммерческого производства вешенки. Многие местные органические субстраты имеют большой потенциал для использования в качестве субстратов и/или добавок для производства вешенки.В этом исследовании, несмотря на то, что опилки, как известно, являются наиболее подходящим субстратом для выращивания грибов, остатки кукурузы (с добавлением рисовых отрубей или без них) также оказались подходящим субстратом для выращивания вешенки на уровне фермы. Кукурузная шелуха и стебель оказались наиболее подходящими по количеству плодовых тел и свежей массе гриба и поэтому рекомендуются в качестве потенциального субстрата для выращивания вешенки. Следует ожидать различий в результатах, представленных другими исследователями, поскольку это может быть связано с различиями в требованиях к выращиванию вешенки, таких как температура, влажность и световой режим.
Конфликт интересов
Авторы заявляют об отсутствии конфликта интересов в отношении публикации данной статьи.
Благодарности
Авторы выражают благодарность руководству и персоналу Молодежной ассоциации/предприятия BenCom муниципалитета Течиман региона Бронг-Ахафо в Гане, где проводилось это исследование.
Артикул
Экспрессия андрогенных рецепторов у пациентов с трижды негативным раком молочной железы в латиноамериканской популяции
Марио Мургия-Перес* , Сандра Зинзия Энрикес-Брена, Ласаро Рамирес-Бальдеррама, Юнуэн Ибица Гарсия-Мендоса, Сауло Мендоса-Рамирес, Марта Алисия Эрнандес-Гонсалес, Бланка Мурильо-Ортис, Марко Антонио Ольвера-Ольвера.| Международный журнал рака и лечения
Исследовательская статья Аннотация Полный текст ПДФ Цитата Страна: МексикаУменьшение плода при беременности высокого порядка; Ретроспективное обсервационное исследование
Манал-шейкер Taha* , Абдулла Аль-Ибрагим, Олубусола Аму, Саусан Аль-Обейдли, Прем Чандра, Зина Аль Мансорри, Наджат Кеньяб, Наджа Аль-Джанахи.| Журнал педиатрии и младенцев
Исследовательская статья Аннотация Полный текст ПДФ Цитата Страна: КатарРаннее указание на отскок W.bancrofti Инфекция на Занзибаре
Шаали М Амэ , Фатьма Каболе, Салум Абуубакар, Альфонсина М. Нанаи, Гирмай Андемихаэль; Хьюз Нана Джунга. | Журнал прикладных микробиологических исследований
Исследовательская статья Аннотация Полный текст ПДФ Цитата Страна: ТанзанияПрогностическая функция отношения тромбоцитов к лимфоцитам при гинекологическом раке: систематический обзор и метаанализ
Пин Ли, Синь Цзэн ,Чонг Фан, Юджин Дай, Ицюань Ван, Мяо Мяо, Цань Жуй, Синьян Ван, Юй Лю, Тин Луань.| Международный журнал рака и лечения
Исследовательская статья Аннотация Полный текст ПДФ Цитата Страна: КитайФункция легких в когорте итальянских детей, родившихся недоношенными
Файнарди Валентина ,Боначини Илария, Сапиенца Элеонора, Корради Мара, Маньяни Чинция, Четта Альфредо, Писи Джованна.| Журнал педиатрии и младенцев
Ретроспективное исследование Аннотация Полный текст ПДФ Цитата Страна: ИталияЧрескожное эндоваскулярное лечение одной псевдоаневризмы АВФ: описание клинического случая
Оронзо Лаццари , Марчелло Наполи, Мария Луиза Лефонс, Витторио Страццери, Себастьяно Канната, Антонелла Реккиони, Фабио Пеннаккиотти.| Журнал клинических случаев и испытаний
Отчет о случае Аннотация Полный текст ПДФ Цитата Страна: ИталияМетастазы в мышцы одной ноги у пациентки с раком молочной железы: история болезни
Надя Пазинетти , Дариуш Гаргозлоо, Боргетти Паоло, Марта Маддало, Антонина Парафиорити, Росарио Маццола, Ванесса Фиглия, Джанпаоло Читони.| Journal of Clinical Case Reports and Trials
Case Report Abstract FullText Pdf Citation Country: ItalyThe Respiratory Sound Features of COVID-19 Patients Fill Gaps between Clinical Data and Screening Methods
Yiqun Hu, Wensheng Pan, Changhua Zhang, Jianfeng Cai ,Yinghui Huang, Sijun Meng, Yi Zhang, Shuisheng Wu, Yu Zhang, Yawei Zhang, Yixiang Ye, Qifeng Wei, Niangui Zhao, Jianping Jiang, Xiaoying Ji, Chunxia Zhou, Chao Zheng, Wen Zhang, Lizhong Xie, Yongchao Hu, Jianquan He, Jian Chen, Wangyue W.| Журнал медицинских наук и развития
Анализ Статья Аннотация Полный текст ПДФ Цитата Страна: КитайРезультаты детской эндохирургической аппендэктомии с одним разрезом (SIPESA), выполненной хирургами-резидентами, по сравнению с традиционной лапароскопией
Энаам Рабои ,Язид Овиви, Амин Аль-Саггаф, Турки Алофи, Алаа Галлаб, Ибтихал Аль-Гамди, Мазен Зидан, Мохамед Файез, Ахмед Атта, Мохамед Шалаби, Мохамед Аль-Онази, Мохаммед Аль-Мохайдли, Мохаммед Бабикер, Салех Камель М., Джавад Аль-Хинди А. , Халил Аль-Батниджи, И.| Журнал педиатрии и младенцев
Анализ Статья Аннотация Полный текст ПДФ Цитата Страна: Саудовская АравияНовые алгоритмы бактериального типирования PFGE: количество совместно мигрировавших фрагментов ДНК, связь PFGE с результатами WGS и компьютерным моделированием для оценки протоколов типирования PulseNet International
Ибрагим-Эльхалил М Адам ,Исам Абдокашиф, Асия Эльрашид, Хиба Байуми, Ахмед Муса, Эйтар Абдулгиом, Сафаа Мамун, Ситана Алнагар, Вафаа Мохаммед, Амна Эль-Хатиб, Мусааб Оши, Фарис Эль-Бакри.| Журнал прикладных микробиологических исследований
Фенитоиноподобный противоэпилептический эффект каннабидиола и родственных метаболитов фитоканнабиноидов: структурные данные молекулярного моделирования
Иштван Уджвари , Антал Лопата.| Журнал биомедицинских исследований и обзоров
Оценка приверженности лечению при хронической обструктивной болезни легких
G Рамья Бала Прабха , Шилпа К., Сарика К., Ликхита М., Рабиа Арши, Правин Кумар, Конде Аббулу.| J Клиническая аптека
Обзор статьи Аннотация Полный текст ПДФ Цитата Страна: ИндияРаспространенность НИЗ и их факторы риска в штате Хартум, Судан
Самах Мохамед Абдин Сайед ,Айман Мохамед Аабдин, Мохаммед Алтыб Альшейх Або-Шанаб, Мункаила Нома.| Международный журнал рака и лечения
Исследовательская статья Аннотация Полный текст ПДФ Цитата Страна: СуданМолекулярная характеристика и филогенетический анализ Wuchereria Bancrofti в образцах крови человека из Малинди и дельты реки Тана, эндемичных регионов Кении
Киньята Нэнси Мутану , Вамбуа Лиллиан, Мутахи Уилкинсон, Мугаса Клэр, Камау Луна, Соломон К.Лангат, Вачира Доркас, Ичугу Кристин, Вайги Эмили, Гитае Розмари, Лусвети Яфет, Кагай Джим. | Журнал биомедицинских исследований и обзоров
Исследовательская статья Аннотация Полный текст ПДФ Цитата Страна: КенияВычислительная алгебраическая геометрия и квантовая механика: инициатива в направлении постсовременной квантовой химии
Акихито Кикучи , Кикути И.| Журнал междисциплинарных исследований и обзоров
Основа для разработки платформы для моделирования и визуализации многомасштабных сложных систем: Monet
Херардо Л. Фебрес .| Журнал междисциплинарных исследований и обзоров
Высокая частота энтеропаразитозов в муниципалитете Ойапок, штат Амапа, Бразилия, на границе с Французской Гвианой
Рубенс Алекс де Оливейра Менезеш , Маргарете ду Сокорро Мендонса Гомеш, Анапаула Мартинс Мендес, Сильвестре Родригеш ду Насименту, Альваро Аугусто Рибейро Д’Алмейда Коуту, Матье Начер, Мартин Йоханнес Энк, Рикардо Луис Дантас Мачадо.| Журнал биомедицинских исследований и обзоров
Исследовательская статья Аннотация Полный текст ПДФ Цитата Страна: БразилияАгрессивная язва Маржолина на колене
Ачехбун Каутар , С. Галлуй, Х. Бэй Бэй, Ф. З. Мернисси, М. Илахиане.| Международный журнал рака и лечения
Фотографическое изображение Аннотация Полный текст ПДФ Цитата Страна: МароккоЛеонард Ван Зантен .| Научный журнал прикладных наук и исследований
Креативный обзор Аннотация Полный текст ПДФ Цитата Страна: Соединенные Штаты АмерикиЭкстракраниальные и диффузные метастазы в костный мозг анапластической олигодендроглиомы: клинический случай и обзор литературы
Евангелия Разис , Авраам Асси, Альберт Хуанг, Георгиос Ригакос, Сотириос Пападопулос, Саввас Пападопулос, Эфимия Вракиду, Константинос Дардуфас, Христос Мурмурис, Стефанос Лампропулос, Панайотис Номикос.| Журнал клинических случаев и испытаний
Отчет о случае Аннотация Полный текст ПДФ Цитата Страна: ГрецияВлияние химиотерапевтического лечения на Escherichia coli
Аватиф Аль Джудайби , Холуд аль-Захрани, Эффат аль-Джудаиби, Шади аль-Хайят, Халед Галал, Мохаммед Аль-Рашеди.| Международный журнал рака и лечения
Исследовательская статья Аннотация Полный текст ПДФ Цитата Страна: Саудовская АравияОбнаружение антигена малярии у лихорадящих пациентов
Хадига Ахмед Исмаил , Амаль Фатхи Гариб, Асмаа Хассан Фарли, Ховайда Махмуд Хагаг, Тайсир Сабер Мохаммед, Хайфа Али Аль Саиф, Тахани Мейд Альтагафи, Роаа Мансор Альтобаити, Афаф Бишара, Ахмед Махмуд Халифа, Усама Махмуд Халифа.| Научный журнал прикладных наук и исследований
Исследовательская статья Аннотация Полный текст ПДФ Цитата Страна: Саудовская АравияСвязь между гипотиреозом и хронической почечной недостаточностью у пациентов с сахарным диабетом 2 типа
Халид С Альджабри ,Ибрагим М. Альнасер, Фахарац, Самия А. Бохари, Мунира А. Альшариф, Патан М. Хан, Абдулла М. Маллошо, Хешам М. Абу-Эльсауд, Мохаммад М. Джалал, Рания Ф. Сафват, Рехаб Эль Борайе, Наваф К. Альджабри, Бандари К. Альджабри, Арва И. Альсураихи , Амджад I Хавсави.| International Journal of Endocrinology Research
Research Article Abstract FullText Pdf Citation Country: Saudi ArabiaFamilial Case of Type 1 Diabetes Mellitus (T1DM) with Similar Onset and HLA Analysis
Hiroshi Bando ,Yoshikane Kato, Setsuko Kanazawa, Mayumi Tanaka, Etsuko Sueki, Hiroe Kanagawa, Takafumi Kawata, Atsuko Kawahito, Aya Aihara.| Международный журнал эндокринологических исследований
Короткое сообщение Аннотация Полный текст ПДФ Цитата Страна: ЯпонияДоля и фактор риска ожирения среди девочек начальной школы в Эр-Рияде, Саудовская Аравия
Наджд Фаваз Алноджаиди , Амани Абдулазиз Аль-Рашед, Зуха Мухаммед Аль-Аммар, Фатима Саид Аль-Гамди, Хадиль Хусейн Асири, Хедая Салман Аль-Отаби, Хавраа Абдукарим Аль-Давуд, Мэрайя Али Аль-Амри, Неджд Ахмед Аль-Дривиш, Рахаф Раджи Аль-Харби, Охуд Халид Аль-Отайби.| Журнал педиатрии и младенцев
Исследовательская статья Аннотация Полный текст ПДФ Цитата Страна: Саудовская АравияКоэффициент интеллекта и фторид воды
Асмаа Абд Эль-Вакиль Эль-Сехмави , Сафаа Махмуд Хаммуда, Гамиль Э. Ибрагим, Самия С Баргаш, Рехам И Эламир.| Научный журнал прикладных наук и исследований
Исследовательская статья Аннотация Полный текст ПДФ Цитата Страна: ЕгипетБиодеградация композитов полимолочной кислоты и крахмала в компосте и почве
Хонгюн Тай , Осита Уилфред, Рэй Марриотт, Цююн Лю, Вячеслав Тверезовский, Саймон Керлинг.| Международный журнал наноисследований
Исследовательская статья Аннотация Полный текст ПДФ Цитата Страна: ВеликобританияСнижение экспрессии миокардиального титина при хронической алкогольной кардиомиопатии
Фернандес-Сола Хоаким ,Толл-Аргудо Марта, Тобиас-Бараха Эстер, Морено-Лозано Педро, Феррер-Курриу Гемма, Гитарт-Мампель Мариона, Планавила-Порта Ана, Гаррабу-Торнос Глория.| Журнал сердечно-сосудистых заболеваний и медицины
Исследовательская статья Аннотация Полный текст ПДФ Цитата Страна: ИспанияНаночастицы и их использование для обнаружения и лечения рака
Мохаммад Назмул Хасан , С. М. Шатил Шахриар, М. Фазлай Рабби, Лимана Афсарин Сэмми, Дилара Джахан, М. Эмран Хоссен, М. Д.-Рифат Шах, М. Д. Рашедул Ислам.| Научный журнал прикладных наук и исследований
Обзор статьи Аннотация Полный текст ПДФ Цитата Страна: Южная КореяЦерковь мормонов в Казахстане
Нурсулу Алтаева , Кудайберди Багашар, Нурзат Мукан, Кайрат Затов.| Научный журнал прикладных наук и исследований
Исследовательская статья Аннотация Полный текст ПДФ Цитата Страна: КазахстанКароль Сикора, д.Джон Петтингелл . | Международный журнал рака и лечения
Исследовательская статья Аннотация Полный текст ПДФ Цитата Страна: ВеликобританияПотребности духовного ухода за больными раком
проф.Мао Цзин , Фарес Савафта. | Научный журнал прикладных наук и исследований
Массовое образование в брюшной полости таза, выявляющее гигантскую аденокарциному предстательной железы
Фатима Захра Харбачи , Фуад Хаддад, Мохамед Тахири, Вафаа Хлива, Ахмед Беллабах, Вафаа Бадре.| Журнал клинических случаев и испытаний
Исследовательская статья Аннотация Полный текст ПДФ Цитата Страна: МароккоКлинический случай синдрома Бина
Булегенова Минира Гусейновна ,Качирина Д, Литош В, Каукенбаева Г.| Журнал педиатрии и младенцев
Отчет о случае Аннотация Полный текст ПДФ Цитата Страна: КазахстанБоль в груди в отделении неотложной помощи
Бенедита Бьянки де Агияр , Татьяна Перейра, Александра Мартинс, Магалис Перейра, Мигель Коста.| Медицинская визуализация и лучевая терапия
Отчет о случае Аннотация Полный текст ПДФ Цитата Страна: ПортугалияОценка метастазов в лимфатических узлах лица при карциноме головы и шеи
Тарек Мохамед Эльнаггар , Ахмед Фараг Эль-Касед, Хоссам Абд Эль-Кадер Эль-Фол, Мохамед Мостафа Ахмед Эль-Элайми, Валид Али Алзакри, Мохмед Сабри.| Журнал клинических случаев и испытаний
Отчет о случае Аннотация Полный текст ПДФ Цитата Страна: ЕгипетСравнительное исследование лечения детей с СДВГ только лекарствами по сравнению с другими лекарствами.Лекарства с когнитивно-поведенческой терапией
Фаиза Назир , Зунайра Алина, Абида Ниази, Амбрин Мехмуд, Хира Иджаз, Абида Хуссейн, Сабика Захир, Хамна Насар, Хина Шахид, Фаиза Сундус, Садаф Наваз, Ребекка Захир.| Научный журнал прикладных наук и исследований
Исследовательская статья Аннотация Полный текст ПДФ Цитата Страна: ПакистанДиагностика бактериального вагиноза с помощью нового клинически действенного молекулярного диагностического инструмента
Джеффри Шаман ,Джозеф П. Джарвис, Даг Рейнс2, Стивен Дж. Крадел, Джеймс Эллиотт, Эван Э. Даймонд, Эрик Аванисс-Агаджани, Фарид Яшарпур.| Журнал прикладных микробиологических исследований
Исследовательская статья Аннотация Полный текст ПДФ Цитата Страна: Соединенные Штаты АмерикиМинимально инвазивный доступ к метастазам в переднюю часть черепа в основании почки
Хоэль Кабальеро Гарсия , Иосмилл Моралес-Перес, Йоханнес Местре-Кабельо, Нелидо Гонсалес-Фернандес, Карлос Апарисио-Гарсия, Мисаэль Лопес-Санчес.| Научный журнал хирургии
Отчет о случае Аннотация Полный текст ПДФ Цитата Страна: КубаСлучай первичного псевдогипоальдостеронизма
Салавура Катерина , Канака Кристина, Ликопулу Эуаггелия, Зеннаро Мария-Кристина, Лазопулу Деспина.| Научный журнал прикладных наук и исследований
Исследовательская статья Аннотация Полный текст ПДФ Цитата Страна: ГрецияСвязь между дефицитом витамина D и сердечно-сосудистыми факторами риска у пожилых людей
Катарина Магальяйнс Порту , Ванесса де Лима Силва, Бривалдо Маркман Филью, Рита де Кассия Хоффманн Леао, Камила да Коста Лима Соуто, Вера Магальяйнс, Франсиско Бандейра.| Журнал сердечно-сосудистых заболеваний и медицины
Исследовательская статья Аннотация Полный текст ПДФ Цитата Страна: БразилияСвойства поверхности ПЭТ-полимера, обработанного методами плазменной иммерсии для упаковки пищевых продуктов
Перикл Лопес Сант-Ана , Хосе Роберто Р.Бортолето, Нильсон С. да Крус, Элидиан С. Рангель, Стивен Ф. Дюррант, Лаура Морейра Коста Ботти, Карлос Альберто Родригес Анхос, София Азеведо, Карин Изабель, Васко Тейшейра, Эбер Антонио Алвес Медейрос, Нильда де Фатима Ф. Соареш. | Международный журнал наноисследований
Исследовательская статья Аннотация Полный текст ПДФ Цитата Страна: БразилияМакрофаги, обработанные кротоксином, стимулируют продукцию АФК и убивают активность в совместно культивируемых нейтрофилах
Сандра Кокуццо Сампайо , Рената Беглиомини Бруно Де-Оливейра, Эллен Эми Като, Мария Кристина Чирилло, Татьяна Соареш Де-Лима, Татьяна Каролина Альба-Лурейро, Руи Кури.| Журнал прикладных микробиологических исследований
Исследовательская статья Аннотация Полный текст ПДФ Цитата Страна: БразилияЛипидная эмульсия для лечения послеоперационной когнитивной дисфункции (ПОКД)
Джозеф Элдор Туан Ань Нгуен, Киен Трунг Нгуен, Туи Куанг Луу, Киен Трунг Нгуен, Пхат Нгок Хо, Ви Нгуен, Сон Чыонг До, Хи Тхань До.| Журнал медицинских наук и развития
Исследовательская статья Аннотация Полный текст ПДФ Цитата Страна: ИзраильКлинические исходы и прогноз у пациентов с острым отеком легких (COPP APO)
Ашок Тахильяни , Тим Уотсон, Чиа Ю Вун, Хуан Вэнь Цзе, Чинг Мин Эр, Дэвид Фу, Хо Хи Хва, Рэндал Лоу, Фу Хи Лин.| Журнал сердечно-сосудистых заболеваний и медицины
Исследовательская статья Аннотация Полный текст ПДФ Цитата Страна: ИрландияХирургическая коррекция аневризмы аорты Бехчета в эпоху эндоваскулярной хирургии
Ахмед Муса ,Ибрагим Ханбал, Алаа Шараби, Оссама М.Закария, Ахмед М. Одех, Абдельфаттах К. Нассар, Сами Абдулхаким. | Научный журнал хирургии
Исследовательская статья Аннотация Полный текст ПДФ Цитата Страна: ЕгипетУровни эндотелина позволяют прогнозировать послеоперационный ОПП у пациентов с коронарным шунтированием
Роксана Гашгаи , Сабет А., Веттерстен Н., Ли Э., Клоптон П., Майзель А.С., Тауб П., Колетта Дж., Гольц Э., Мехта Р.| Журнал сердечно-сосудистых заболеваний и медицины
Исследовательская статья Аннотация Полный текст ПДФ Цитата Страна: Соединенные Штаты АмерикиКристина Мастаньеви ,Боян Сарканж, Винко Крстанович, Кресимир Мастаньевич.| Международный журнал пищевых продуктов и биологических наук
Редакция Аннотация Полный текст ПДФ Цитата Страна: ХорватияНовые бесспоровые вешенки — WUR
Производители привыкли к нынешнему разнообразию, но они также выиграют от большего выбора, поскольку это делает их менее уязвимыми.Йохан Баарс, исследователь грибов в WUR
Нидерландский грибной сектор находится под давлением жесткой конкуренции из-за рубежа. Когда в 1993 году Йохан Баарс начал исследовать шампиньоны, в Нидерландах все еще насчитывалась тысяча производителей шампиньонов. Сейчас их осталось всего около восьмидесяти, хотя вместе они дают больше грибов, чем тысяча в то время. «Рентабельность выращивания грибов низкая, поэтому производители были вынуждены увеличивать масштабы. Кроме того, некоторые производители решили найти нишу на рынке.”
Растущий рынок
Выращивание вешенки является одной из таких нишевых рыночных площадок, а также растущим рынком с ростом популярности вешенки в кулинарном мире. Мелко нарезанная шляпка гриба хорошо сочетается с ризотто, блюдами из макарон или супом из лесных грибов. Поэтому все больше и больше производителей освобождают место в своих графиках выращивания для вешенки, которая приносит более высокую прибыль, чем средний шампиньон. По словам Баарса, вплоть до прошлого века выращивание вешенки было проблематичным.«В Нидерландах было несколько производителей вешенки, но им приходилось защищаться от миллиардов переносимых по воздуху спор, распространяемых грибами. Для предотвращения аллергических реакций в легких им приходилось носить герметичные шлемы, что было неприятно. Кроме того, огромное количество переносимых по воздуху спор забивало воздушные фильтры, что означало более высокие счета за электроэнергию. Урожайность тоже была разочаровывающей; новые питомники давали впечатляющие урожаи, но через несколько месяцев численность падала, скорее всего, из-за того, что споры распространяли болезни.
Дефектный ген
В 1997 году Баарс и его коллеги начали исследования возможности выращивания бесспорового вешенки. «В 1959 году американский исследователь Блок нашел на дереве вешенку, которая затем попала в немецкую лабораторию. От этого одного гриба немецкому исследователю Эгеру удалось скрестить вариант, не дающий спор. Теперь мы знаем, что это происходит из-за дефектного гена. Мы начали выводить этот вариант в 1997 году. Мы хотели вырастить вешенку с большой мясистой шляпкой и привлекательной окраской.Первые испытания не увенчались успехом, в результате были получены небольшие пучки вешенок с маленькими шляпками и длинными ножками. Но к 2004 году мы вывели прекрасный новый сорт».
Коммерческий успех
Благодаря сочетанию проб и ошибок, а также мастерству, индустрии удалось добиться коммерческого успеха вариаций этого гриба. Хорошим примером является популярный SPOPPO, штамм, который устраняет риск респираторных заболеваний у рабочих и распространения инфекций через собственные споры.Девяносто процентов производителей в Северо-Западной Европе в настоящее время выращивают улучшенный сорт. Обратной стороной этого успеха является то, что выращивание устриц сильно зависит от этого бесспорового штамма, считает Баарс. «Это рискованно для отрасли. Отказ от штамма, который выделяет споры, невозможен, потому что производители больше не готовы справляться с давлением спор».
Выращивание СПОППО
Шестнадцать новых вариантов
WUR работала над выведением новых бесспоровых штаммов в течение шести лет.С хорошими результатами, говорит Баарс. «Мы разработали шестнадцать вариантов, которые, по нашему мнению, имеют потенциал. Эти варианты готовы для тестирования производителями. Испытания, которые мы провели в собственном питомнике, были очень многообещающими. Производители любопытны, и есть большой интерес попробовать новые варианты».
Если новые варианты окажутся схожими по качеству с вешенками, доступными в настоящее время в магазинах, производители будут их выращивать, прогнозирует Баарс. «Производители привыкли к нынешнему разнообразию, но они также выиграют от наличия большего количества вариантов, поскольку это делает их менее уязвимыми.Это может произойти уже через год или два».


