есть ли разница для обработки древесины » Одна дома!
Автор Станислава Ганц На чтение 14 мин Просмотров 5.9к. Опубликовано
Дом из дерева, пожалуй, больше всех других материалов нуждается в уходе, заботе и защите. Конечно, разнообразие всяких средств, созданных промышленным способом сегодня, просто невообразимо. Тем не менее, начнём мы тему именно с тех средств, которыми пользовались ещё наши предки. Итак, сравниваем медный и железный купорос для обработки древесины.
Купорос – это…
Для начала стоит узнать, что такое купорос. Итак, купорос – это двухвалентный металл, которым называют кристаллогидраты сульфатов. Иначе можно сказать, что это серная кислота плюс металл. В свою очередь кристаллогидрат – это соединение воды и соли.
Существует 9 (девять) видов купоросов:
- Ванадиевый – гептагидрат, сернокислый ванадий, — это красно-фиолетовые кристаллы, легко растворяющиеся в воде.
 Имеет вид VSO4 – соль ванадия + серная кислота. Главная роль – восстановительная: восстанавливает из солей золота, меди и олова металлы; из азотной кислоты и нитритов – аммиак, в том числе производные; из сульфитов – сероводород.
Имеет вид VSO4 – соль ванадия + серная кислота. Главная роль – восстановительная: восстанавливает из солей золота, меди и олова металлы; из азотной кислоты и нитритов – аммиак, в том числе производные; из сульфитов – сероводород. - Железный – тетраоксосульфат, серной кислоты железная соль, — это неорганика, нелетучая, без запаха, голубовато-зелёного, зелёного либо бесцветного цветов, но крайне гигроскопичная и выветривающаяся на воздухе, поскольку происходит потеря кристаллизационной воды. Имеет формулу FeSO Растворяется в воде при температуре +20 (плюс двадцать) градусов, не имеет практически токсичности. Его основное применение – сельское хозяйство, текстиль, приготовление минеральных красок и чернил, окрашивание шерсти в чёрный цвет, медицина. В принципе, получить его можно в домашних условиях: разбавить серную кислоту до 10% (десяти процентов), используя любую посуду, за исключением металла, и пока она горячая, опускаем в неё любое железо (старые, ржавые гвозди, обрезки кровельного железа, и так далее).
 Почему предпочтительнее сделать железный купорос в домашних условиях? Всё дело в том, что в промышленности это – побочный продукт при травлении чёрного металла, поэтому в нём крайне много ненужных примесей. Итак, проводить процедуру следует на улице, поскольку запах – тот ещё. Как только бросили в кислоту железо – начнётся реакция с выделением водорода. Когда пузыри перестанут выделяться – реакция закончилась. Добавляем новую партию железа – реакция возобновляется. Если же нет – всё готово. По итогу два варианта жидкости: либо зеленоватая жидкость с разъеденными гвоздями, либо обросшие зелёными кристаллами гвозди в практически прозрачной жидкости. Также в обоих случаях будет присутствовать чёрный осадок, как результат наличия в стали углерода. После сливаем в отдельную посуду, стараясь не допускать попадания осадка, выпариваем. Таким образом, оставив на ночь подсыхать после выпаривания, на утро получится железного купороса кристаллы.
Почему предпочтительнее сделать железный купорос в домашних условиях? Всё дело в том, что в промышленности это – побочный продукт при травлении чёрного металла, поэтому в нём крайне много ненужных примесей. Итак, проводить процедуру следует на улице, поскольку запах – тот ещё. Как только бросили в кислоту железо – начнётся реакция с выделением водорода. Когда пузыри перестанут выделяться – реакция закончилась. Добавляем новую партию железа – реакция возобновляется. Если же нет – всё готово. По итогу два варианта жидкости: либо зеленоватая жидкость с разъеденными гвоздями, либо обросшие зелёными кристаллами гвозди в практически прозрачной жидкости. Также в обоих случаях будет присутствовать чёрный осадок, как результат наличия в стали углерода. После сливаем в отдельную посуду, стараясь не допускать попадания осадка, выпариваем. Таким образом, оставив на ночь подсыхать после выпаривания, на утро получится железного купороса кристаллы. - Кобальтовый – сульфат кобальта, красный купорос, – это кристаллы красного (гептагидрат сульфата кобальта) либо розового (безводного) цветов.
 Формула вещества – CoSO4 – соль двухвалентного кобальта + серная кислота. Имеет крайне высокую гигроскопичность при медленном растворении в воде, плохом растворении в концентрате серной кислоты и этаноле, более-менее растворении в глицерине, метаноле. Основное применение – один из компонентов для гальванического покрытия кобальтом других металлов, а также компонент окрашивания керамики, стекла. При всё при этом кобальт — токсичное вещество, поэтому с ним следует обращаться крайне осторожно.
Формула вещества – CoSO4 – соль двухвалентного кобальта + серная кислота. Имеет крайне высокую гигроскопичность при медленном растворении в воде, плохом растворении в концентрате серной кислоты и этаноле, более-менее растворении в глицерине, метаноле. Основное применение – один из компонентов для гальванического покрытия кобальтом других металлов, а также компонент окрашивания керамики, стекла. При всё при этом кобальт — токсичное вещество, поэтому с ним следует обращаться крайне осторожно. - Медный – сернокислая медь, медная соль серной кислоты, — вещество без запаха, гигроскопичное, с разнообразными оттенками синего, горьковато-металлического вяжущего вкуса. Имеет формулу – CuSO Применяют его практически во всех сферах, включая пищевую промышленность – Е519 (пятьсот девятнадцать).
- Никелевый – сернокислый никель, сульфат никеля, кристаллогидрат сульфата никеля, — бело-жёлтого цвета кристаллы, крайне гигроскопичные и очень хорошо растворяющиеся в водной среде. Формула – NiSO Применяются при производстве фунгицидов, аккумуляторов, катализаторов, парфюмерии и жировой промышленности.
Но стоит помнить: никелевый купорос – канцерогенен, высокотоксичен, сильный аллерген, вызывает мутации, для летального исхода достаточная доза – от 32 (тридцати двух) до 122 (ста двадцати двух) миллиграмм на килограмм. Его природный аналог – моренозит, минерал зеленовато-белого либо яблочно-зелёного цветов.
- Свинцовый – сульфат свинца, — имеет формулу PbSO Этот купорос практически не растворятся в воде, ядовит, высокотоксичен, легко проникает через кожу и слизистые, повреждая почки, ЦНС, нарушая зрение. Применяется в качестве компонента для изготовления пигментов, а также образуется при разряде свинцово-кислотных аккумуляторов. Имеет так же, как и предыдущий тип, природный аналог – англезит, минерал, представляющий собой безводный свинцовый сульфат.
- Хромовый – трёхвалентного хрома соль + серная кислота, — кристаллы фиолетово-красного цвета, имеющие магнитную восприимчивость. Очень неохотно безводные фракции растворяются в кислотах, воде. При нагревании меняет цвет с фиолетового на зелёный.
 Формула – Cr2(SO4)3. Хромовый купорос – малотоксичен, и находит своё применение в цветной фотопечати, как протрава при крашении ситца, дублении кожи.
Формула – Cr2(SO4)3. Хромовый купорос – малотоксичен, и находит своё применение в цветной фотопечати, как протрава при крашении ситца, дублении кожи. - Цинковый – сернокислый цинк, серной кислоты цинковая соль, — это порошок с прозрачными, бесцветными кристаллами, нестабильными, выветривающимися от воздуха, не имеющими запаха, но вяжущим, резким вкусом. Имеет формулу – ZnSO Используют купорос из цинка для производства вискозы, глазури (которой покрывают изделия из керамики), минеральных красок, в сельском хозяйстве (как удобрение), качестве флотореагента (один из способов обогащения полезных ископаемых), аккумуляторах, медицине (таблетки, глазные капли), химических энергетических источниках, как добавка к кормам животных. Тем не менее, сульфат цинка – крайне токсичен, а его попадание на слизистую (достаточно вдохнуть пыль), приводит к её атрофии.
- Марганцевый – сульфат марганца, — белый порошок, хорошо поддающийся разложению и плавлению. Формула купороса – MnSO Нашёл своё применение в текстильной промышленности, производстве жирных кислот синтетического типа, в качестве удобрения, компонент в корме для животных и свинцово-марганцевых сиккативов.
 Стоит помнить: марганец – политропный яд (один агент воздействует на разные органы и системы), который крайне негативно влияет на лёгкие, сердечнососудистую систему, желудочно-кишечный тракт, вызывая аллергию и мутации.
Стоит помнить: марганец – политропный яд (один агент воздействует на разные органы и системы), который крайне негативно влияет на лёгкие, сердечнососудистую систему, желудочно-кишечный тракт, вызывая аллергию и мутации. - А также есть так называемое купоросное масло, что есть не что иное, как концентрированная серная кислота.
- Глауберова соль – мирабилит, гуджир, сибирская соль, декагидрат сульфата натрия, сернокислый натрий, — так называемый технический купорос, белого, желтовато-белого либо зеленовато-белого цветов, без запаха. На вкус – горько-солёный, тающий во рту. Применяется в медицине в качестве мощного слабительного, который, вызывая жидкий стул, очищает кишечник ото всех отмерших клеток.
- Кристаллическая сода – декагидрат карбоната натрия, кристаллогидрат кальцинированной соды, — в пищевой промышленности известен, как Е500 (пятьсот). Кроме того, его используют в мыловарении, для изготовления эмалей, синтетических моющих средств, стекольном производстве, с его помощью также получают ультрамарин.
 Карбонатом натрия обезжиривают металлы, десульфатизируют доменный чугун, смягчают жёсткую воду.
Карбонатом натрия обезжиривают металлы, десульфатизируют доменный чугун, смягчают жёсткую воду. - Английская соль – сульфат магнезии, горькая соль, сульфат магния, гептагидрат сульфата натрия, соль Эпсома, — химическое соединение сульфата магния. Как добавка Е518 (пятьсот восемнадцать) встречается в пищевом производстве. Как источник серы либо магния – для растений.
- Гипс – дигидрат сульфата кальция – имеет белый цвет с оттенками красного и серого. Используется как удобрение, вяжущий материал строительства, в медицине, для изготовления глазури, эмали, красок. К сожалению, очень плотный тип гипса желтоватого цвета – это не гипс.
Обработка древесины
Обрабатывать поверхность следует в 2-5 (два — пять) слоя. Ведь главная цель, которая преследуется при обработке древесины – это защита от дождя, снега, ультрафиолета снаружи, от большой влажности, плесени, грибка, разнообразных насекомых – изнутри. Так что начинаем, как обычно, с подготовки поверхности: очищаем древесину от пыли, загрязнений, при необходимости – шлифуем. И, наконец, обезжириваем, к примеру, Уайт-спиритом, смочив плотную безворсовую ткань. Переходим теперь к антисептическим составам, способным защитить деревянную поверхность.
И, наконец, обезжириваем, к примеру, Уайт-спиритом, смочив плотную безворсовую ткань. Переходим теперь к антисептическим составам, способным защитить деревянную поверхность.
Для этого знакомимся с информацией ниже.
Железный купорос
Производят его, согласно ГОСТ, под номером 6981, разработанным в 1994 (одна тысяча девятьсот девяносто четвёртом) году, где он именуется сульфатом гептагидрата железа (в магазинах, как правило, встречается 20-типроцентный (двадцатипроцентный)). Он практически не токсичен, тем не менее, соблюдение мер безопасности – обязательное условие применения купороса. Также, по некоторым данным сульфат железа – взрывоопасен. Поэтому хранить его нужно в герметичной упаковке, сухом месте. И, естественно, при попадании на кожу и в глаза промыть тут большим количеством воды, а после работы – помыть лицо и руки мылом.
Итак, для обработки потолка достаточно 5-7-процентного (пяти — семипроцентного) раствора (500-700 (пятьсот — семьсот) грамм на 10 (десять) литров воды), а стен, чтобы избавится от грибка, — в 1 (одном) литре воды растворяют 150 (сто пятьдесят) грамм порошка. Чтобы железный купорос не окислился – следует добавить немного лимонной кислоты. Для стен погреба готовят раствор 10-процентный (десятипроцентный): смешивают купорос с глиной до консистенции сметаны и наносят кистью два раза за осень, но обязательно до помещения овощей на хранение.
Чтобы железный купорос не окислился – следует добавить немного лимонной кислоты. Для стен погреба готовят раствор 10-процентный (десятипроцентный): смешивают купорос с глиной до консистенции сметаны и наносят кистью два раза за осень, но обязательно до помещения овощей на хранение.
Для того чтобы приготовить водонепроницаемый раствор, который в большинстве случаев используют для покрытия хранилища, крыши землянок, бассейна, тогда стоит приготовить раствор, состоящий из 7-10 (семи — десяти) килограмм извести, 3.5-8 (трёх с половиной — восьми) килограмм железного купороса, и всё разводится водой до консистенции сметаны:
- Для начала в холодной воде (небольшое количество) разводят известь, получая так называемое известковое молочко. Размешивать необходимо тщательно, чтобы не было комочков.
- Отдельно в горячей воде разводят железный купорос, и тонкой струйкой при непрерывном помешивании вливают в молочко из извести.
Кстати, цвет после покраски становится нежно коричневым. Бывалые в этот раствор советуют добавлять ещё немного соли – это защитит от пачканья известью.
Бывалые в этот раствор советуют добавлять ещё немного соли – это защитит от пачканья известью.
Медный купорос
Медный купорос встречается в продаже под марками А и Б, по сортам – второй, первый, высший. Технические условия производства устанавливаются ГОСТом под номером 19347 от 1999 (одна тысяча девятьсот девяносто девятого) года. Итак:
- тип А сорт высший: доля осадка – до 0.03%, серной кислоты – до 0.20%, железа – до 0.02%, меди – от 25.20%, массовая доля купороса – от 99.1%;
- тип А сорт первый: доля осадка – до 0.05%, серной кислоты – до 0.25%, железа – до 0.04%, меди – от 24.94%, массовая доля – от 98%;
- тип Б сорт первый: доля осадка и железа – до 0.05%, серной кислоты – до 0.20%, меди – от 24.43%, массовая доля – от 96%;
- тип Б сорт второй: доля осадка и железа – до 0.10%, серной кислоты – до 0.25%, меди – от 23.67%, массовая доля – от 93.1%;
- тип Б сорт высший: доля осадка – до 0.05%, серной кислоты – до 0.20%, железа – 0.04%, меди – от 24.
 97%, массовая доля – от 98.1%.
97%, массовая доля – от 98.1%.
Древесина и подвал обрабатывают медным купоросом для того, чтобы защитить от гнили, плесневого грибка, то есть, в качестве дезинфицирующего средства. Кроме этого, сульфат меди увеличивает огнеупорные свойства материала (помимо древесины, он идеален для кирпича, бетона).
Важно придерживаться правил:
- Пакет должен быть плотно закрыт, иначе сульфат меди может быстро потерять все полезные свойства.
- При попадании в глаза либо на кожу нужно срочно промыть большим количеством воды поражённые участки.
- Для приготовления раствора использовать металлическую ёмкость запрещено. Её стоит заменить стеклянной, эмалированной, пластиковой, силиконовой ёмкостями. Собственно с этой точки зрения при обработке дерева в нём не должно быть гвоздей, шурупов и другого металла – разъест.
Итак, медный купорос в качестве защиты: 10 (десять) литров воды – 1-2 (один — два) килограмма сульфата меди либо 10 (десять) грамм продукта на 1 (один) литр воды. Его главные отличия: медленно сохнет, но при этом глубже проникает, и слегка изменяет цвет покрываемого им материала.
Его главные отличия: медленно сохнет, но при этом глубже проникает, и слегка изменяет цвет покрываемого им материала.
Ещё один интересный способ подготовки древесины — столбов, в частности, которые будут закапываться в землю, — вымачивание её двое суток в 20% (двадцатипроцентном) растворе и последующее высушивание под навесом в течение 1 (одного) месяца.
Кстати говоря, в промышленном производстве такая обработка длится всего лишь 30 (тридцать) минут. Секрет? Дело в том, что отлично просушенную древесину укладывают в ёмкость, покрывают раствором купороса, разогретого до 40 (сорока) градусов, герметично закрывают. Давление в своеобразном ящике – 10 (десять) атмосфер, благодаря чему и происходит пропитывание буквально за полчаса. Далее эта древесина опять просушивается.
От плесени в ведре тёплой воды разводят от 100 (ста) до 200 (двухсот) грамм порошка сульфата, а чтобы увеличить проникновение в структуру дерева – добавить 1 (один) стакан уксусной кислоты.
На основе сульфата меди стоит приготовить противогрибковую грунтовку, для чего возьмём на 10 (десять) литров воды 300 (триста) грамм купороса, 200 (двести) грамм столярного клея, 250 (двести пятьдесят) грамм хозяйственного мыла. В первую очередь смешивают клей с водой (получится 10% (десятипроцентный) раствор), после – добавляют мыло и размешивают до его полного растворения. А на последнем этапе – уже купорос, в отдельной посуде растворённый небольшим количеством воды. Вся смесь должна быть без комочков. Как правило, сверху на высохшую грунтовку наносят краску на силикатной основе с щёлочестойкими красителями (пигментами).
Можно поступить ещё проще, и смешать медное мыло с масляной либо ПФ краской или лаком, получив таким образом противогрибковую краску долгого хранения. Для этого брусок хозяйственного мыла полностью растворяем в тёплой воде и тонкой струйкой вливаем растворённый в отдельной посуде купорос, не останавливая помешивание. Готовность определяем по цвету: как только при добавлении новой порции цвет итогового изделия перестанет «зеленеть», всё готово. Останется полученную светло-зелёную массу отжать, чтобы избавиться от лишней воды. Последний этап перед смешиванием с лаком или краской – растворить медное мыло в 200 (двухстах) граммах обычного растительного масла нагревом, но не доводя до кипения. Естественно, стоит помнить, что итоговый цвет краски изменится. Можно посмотреть по таблице, какой примерно станет оттенок от добавления светло-зелёного.
Останется полученную светло-зелёную массу отжать, чтобы избавиться от лишней воды. Последний этап перед смешиванием с лаком или краской – растворить медное мыло в 200 (двухстах) граммах обычного растительного масла нагревом, но не доводя до кипения. Естественно, стоит помнить, что итоговый цвет краски изменится. Можно посмотреть по таблице, какой примерно станет оттенок от добавления светло-зелёного.
Под клеевую краску можно приготовить грунтовку. Из расчёта 10 (десять) литров краски, как итогового материала: 250 (двести пятьдесят) грамм хозяйственного мыла, 100-150 (сто — сто пятьдесят) грамм купороса,200 (двести) грамм любого твёрдого животного клея, 25-30 (двадцать пять — тридцать) грамм олифы, 3 (три) килограмма молотого мела (именно мела, не извести).
Готовая смесь с медным купоросом в помещении можно хранить до 3 месяцев, а в холодном месте – до 1(одного) года.
Повторим – крайне важно соблюдать технику безопасности, поскольку:
- при вдыхании происходит ожог слизистой лёгких;
- при проглатывании – раздражение ЖКТ, вплоть до летального исхода (зависит от дозировки).
 При этом тут же промывать желудок нельзя во избежание последствий, поэтому только незамедлительный вызов врача;
При этом тут же промывать желудок нельзя во избежание последствий, поэтому только незамедлительный вызов врача; - при попадании в глаза – ожог глазного яблока поверхности вплоть до слепоты;
- при попадании в кровь – нарушение либо полное прекращение функционирования органов: печени, почек, сердца, лёгких, ЦНС. И, не смотря на лечение, это – летальный исход.
Соответственно, хранить в абсолютной недоступности для детей, животных и даже взрослых (с неустойчивой психикой).
Вместо послесловия
Оба раствора – железный, медный – наносят валиком, пульверизатором либо кистью, как кому удобно. И, естественно, нельзя забывать о защите при работе с любым из растворов. В частности, использовать респиратор, перчатки, проветривать помещение, если обработка происходит внутри.
Но помимо этого важно знать, что вас не обманули, и действительно в приобретённом в магазине пакете – медный купорос, который в последнее время часто стали подделывать.
Итак, как определить, что именно в купленном пакете медный купорос:
- Для начала посмотрим на внешний вид порошка.
 Он должен внешне напоминать поваренную соль синего цвета (широта оттенков – от тёмно-синего до морской волны цвета), крупинок разного цвета, но не окрашивать руки при этом.
Он должен внешне напоминать поваренную соль синего цвета (широта оттенков – от тёмно-синего до морской волны цвета), крупинок разного цвета, но не окрашивать руки при этом. - Теперь аккуратно на острие ножа помещаем крупинку и нагреваем нож снизу до красна. Должен отлично чувствоваться резкий запах серы.
- Остался последний этап проверки. На стакан тёплой воды берём 1 (одну) чайную ложку купороса, размешиваем, а после растворения всех крупинок – опускаем простой гвоздь на пару минут. Ждём появления красного налёта.
Если вся проверка прошла удачно, значит, перед вами – настоящий медный купорос.
Каков же ответ на главный вопрос: что лучше для применения в строительстве и при обработке древесины – медный или железный купорос? Всё-таки медный, поскольку от железного больше пользы в растениеводстве. Тем не менее, помните: для получения лучшего результата обрабатывать необходимо от 2 (двух) до 5 (пяти) раз в зависимости от поражения поверхности грибком, плесенью. А также каждый слой должен просохнуть очень тщательно. Ну а если вы далее будете клеить обои либо красить – не лишним будет добавление купороса в обойный клей или краску (лак), о чём было написано выше.
Теперь можно сказать, что о купоросах вы знаете всё, а выводы – за вами.
Хелаты и купоросы — правила использования
Сегодня мы поговорим о хелатах, почему они важны для сада и огорода, и можно ли их приготовить в домашних условиях. Вы наверняка слышали о преимуществах удобрений, в которых вещества содержатся в хелатной форме.
Что же такое хелаты?
Хелаты — это соединения металлов, с особыми молекулами. Эти молекулы как бы охватывают молекулу металла и охраняют ее от различных взаимодействий, а также существенно облегчают ее усваивание для растения. Дело в том, что многие микроэлементы, попадая в почву или на поверхность растений, становятся для них недоступными и, несмотря на их достаточное количество, не могут усваиваться растениями, растения испытывают их недостаток. Недостаток микроэлементов не так сильно и ярко выражен, как недостаток макроэлементов, например, азота или фосфора. Азотное голодание вы выявите сразу, а вот голодание по микроэлементам определить очень сложно, вы можете даже не понять в чем дело.
Недостаток микроэлементов не так сильно и ярко выражен, как недостаток макроэлементов, например, азота или фосфора. Азотное голодание вы выявите сразу, а вот голодание по микроэлементам определить очень сложно, вы можете даже не понять в чем дело.
Я провел небольшой и очень простой эксперимент. Этот эксперимент наглядно показал, как хелатные агенты защищают железный купорос от окисления. А ведь именно окисление железного купороса приводит к тому, что растения страдают от недостатка железа.
Если вы хотите подкормить свои растения железом с помощью железного купороса, то обязательно используйте лимонную кислоту, она есть у каждого, и она является прекрасным хелатным агентом, который доступен всем и всякому.
Особенно если вы хотите подкормить рододендроны, верески, голубику, именно такой раствор, в таком виде железо, будет усваиваться этими растениями лучше всего. Кстати, они зачастую довольно сильно страдают от нехватки железа. Вернее железа достаточно, но оно для них недоступно. К тому же, подкисление раствора лимонной кислотой создаст более благоприятные условия для их роста.
Точно такую же историю, можно провернуть дома и с медным купоросом. Раствор медного купороса довольно токсичен, плохо растворяется, плохо усваивается растениями, а если вы добавите сюда немножечко аммиака, то вы получите соединение, которое гораздо лучше растворяется, гораздо лучше усваивается растениями и в такой форме работает в саду намного лучше.
Есть еще один очень хороший хелатный агент, который мы можем использовать в быту — это гуматы, и о них мы поговорим более подробно в нашем следующем выпуске.
Итак, приготовление хелата железа для подкормки всех растений: на 1 чайную ложку железного купороса — 1 чайную ложку без горки лимонной кислоты. Лимонную кислоту можно заменить на гумат калия или оксидат торфа (что лучше, чем просто гумат). Гумата надо взять около 50 мл. Можно до 100 мл. Сперва растворить кислоту или гумат, потом в раствор добавить купорос.
Так можно готовить любой хелат металла — марганца (только не с марганцовкой!), цинка (кстати, соли марганца и/или цинка в смеси с фосфорной кислотой можно отыскать в специальных секциях хозтоваров и автомобильных магазинов в средствах для преобразования ржавчины. Сопутствующие спирты и танины не помеха. Танины, кстати, подавляют рост патогенных для многих растений микроорганизмов. Половины чайной ложечки на ведро воды будет с лихвой для подкормки) и т.п.
Сад огород применение медного купороса
Медный купорос: применение в садоводстве осенью
Похожие статьи
Действие медного купороса
как удобрение для огородаПравила применения препарата
медный купорос применяется для уничтожения болезней растений, он голубого цвета. а железный зеленого, и его применяют в основном для профилактики хлороза у семечковых, так же от болезней, для подкормки. Яблони и косточковые ( вишни, сливы) очень нуждаются в железе, осенью после вегетационного периода вносят под деревья. Растворяют с водой и по прествольному кругу поливают
Яблони и косточковые ( вишни, сливы) очень нуждаются в железе, осенью после вегетационного периода вносят под деревья. Растворяют с водой и по прествольному кругу поливаютKakProsto.ru
Бордоская жидкость – приготовление, применение фунгицида
медь и железо — разные вещи… ) химия.
В магазинах для садоводов появилась в продаже концентрированная бордоская жидкость. Продают её в пластиковых бутылках разной ёмкости — от 100 мл до 1 литра. Как пользоваться? Бордосская жидкость готовая (в бутылках) очень удобна в использовании. Инструкция не сложна. Не надо ничего смешивать, процеживать — добавил в ведро воды 250 мл жидкости из бутылки, размешал — и всё готово. Приготовленный раствор бордоской смеси хранится только сутки, то есть он не подлежит длительному хранению. Его используют полностью и в этот же день. Это непременное условие того, что ваша работа проведена не зря. Учитывайте это при его приготовлении, старайтесь использовать его весь в этот же день.Затем будем вливать раствор медного купороса в известковое молоко. Ни в коем случае не делайте наоборот. Именно — медный купорос – в раствор извести. Желательно это делать вдвоём. Кто-то один помешивает известковое молоко, а другой в это время тонкой струйкой вливает туда раствор медного купороса. В итоге у вас должна получиться жидкость нежно-голубого небесного оттенка. Это и есть 1% -ная бордоская жидкость.
Затем в другое ведро высыпаем 100-150 г извести и заливаем туда 5 литров воды. Известь растворяется в воде намного лучше медного купороса, но все-таки хорошо её размешиваете, чтобы не осталось комочков – получается известковое молоко.
Для приготовления раствора бордоской смеси нам понадобятся пластиковые или эмалированные вёдра. Не используйте металлические или оцинкованные, иначе раствор вступит в реакцию с металлом и оздоровительные свойства жидкости будут сведены на нет.
Этой жидкостью обрабатывают цветочные, плодовые, овощные, ягодные, культуры от грибковых заболеваний, начиная от картофеля, томатов, огурцов, после появления всходов, до яблонь, груш, других плодово-ягодных растений. То есть бордоская жидкость – это универсальный фунгицид. Основное вещество, которое помогает бороться с грибными болезнями, это медь, медный купорос. Но так как медь, медный купорос в чистом виде обжигает листья, то в бордоскую смесь добавляется известь.
Я думаю, что все огородники и садоводы часто слышат о том, что растения надо в некоторых случаях обрабатывать универсальным фунгицидом — бордоской жидкостью. Иногда её называют бордоской смесью. Я тоже не раз упоминала об этом. Из чего она состоит? Каков процесс приготовления? Обработку каких растений в саду и на огороде производят этим фунгицидом?
Если садоводы хотят получать хорошие урожаи, они не смогут обойтись без применения химических препаратов. Одним из универсальных препаратов, который используется для лечения садовых болезней еще со средних веков, является медный купорос.
А ещё платы можно травить для радиоэлектроники.
Против грибка. Из него делают бордоскую жидкость и поливают растения и обрабатывают дерево.
Медный купорос применяют при борьбе с болезнями, железный купорос для уничтожения лишайников и мхов.
Медный купорос-порошок голубого цвета, его применяют в борьбе с болезнями растений (парша, бактериоз, монилиоз, антрарноз, фитофтора и др.) обычно в сочетании с известью (бордосская жидкость) хотя можно и просто с водой не более 3%процентов, а по зеленому листу, не более 1%..а то сожжете растение.. .
Для приготовления 3%-ного раствора возьмите 300 г медного купороса и 450 г извести на 10 литров воды. Процесс приготовления такой же, как был описан выше.
Очень важно, чтобы бордоская жидкость имела нейтральную реакцию. Поэтому необходимо при её приготовлении соблюдать пропорции. Если вы положите в жидкость больше, чем нужно извести, то получите раствор со щелочной реакцией, а если медного купороса будет больше рекомендуемого количества, то жидкость будет иметь кислую реакцию.
После приготовления этих двух растворов, желательно процедить их через очень мелкое сито или через два слоя марли. Процеживайте каждый раствор отдельно. Это нужно для того, чтобы распылитель, опрыскиватель не засорялись.
Итак, нам понадобится два пластиковых ведра. В каждом из них мы будем растворять один из компонентов бордоской смеси – отдельно друг от друга.
Обычно, садоводы для обработки садово-огородных растений используют 1%-ный или 3%-ный раствор.
Бордоскую смесь изобрел французский ботаник Пьер-Мари Алексис Мильярде (Pierre-Marie Alexis Millardet, 1838-1902), чтобы защитить виноград от болезней.
ogorod23.ru
Медный купорос и железный купорос- разница в применении?
Людмила Саманчук
Медный купорос – порошок, который при растворении в воде придает ей красивый голубой цвет. Этот препарат востребован в саду с весны до поздней осени. Он с успехом используется для уничтожения грибковых заболеваний и вредителей на садовых растениях и плодовых деревьях, для дезинфекции помещений для хранения фруктов и овощей, обогащения состава почвы.
В сельском хозяйстве применяется для борьбы с вредителями и болезнями растений и для протравливания зерна, при выделке кожи, для обогащения руды при флотации, в производстве двухсторонних печатных плат, в процессах гальванического и химического меднения, в производстве искусственных волокон, органических красителей, минеральных красок, мышьяковистых химикатов и т. д.
виктория чайковская
крыс травить
Галина
По осени -железный, по весне -медный. Это как весенние и осенние удобрения.
Наталья Белоусова
Железный купорос-порошок желтого или зеленоватого цвета, применят, для тех же заболеваний, плюс лишайники, мхи и дезинфекциявыгребных ям и помещений, но существенная разница, не на зеленый лист! а то сожжет, а можно теперь, когда деревья сбросили лиственную массу, либо ранней весной, до распускания почек. .. то есть действие железного купороса более сильное…
.. то есть действие железного купороса более сильное…
Бonnie without Clyde
Теперь, я думаю, у вас получится приготовить бордоскую жидкость для обработки плодовых и ягодных культур в вашем саду. Это совсем не сложно.
для чего используют медный купорос
Наталья Соловьева
Как можно проверить раствор на реакцию? Самый простой способ – проверка обыкновенным металлическим гвоздём, чистым, не ржавым. Опустите гвоздь в ведро со смесью, подержите некоторое время. Если на гвозде есть рыжие пятна, то раствор имеет кислую реакцию. Если нет ничего, то раствор приготовлен правильно и имеет нейтральную реакцию. На щелочную реакцию обычно проверяют раствор лакмусовой бумагой, а если её у вас нет, то старайтесь соблюдать пропорции при приготовлении, чтобы ничего не напортить.
Ёжик
После процеживания обоих растворов доведите объём раствора медного купороса также до пяти литров.
Анна
Если мы хотим получить 1%-ный раствор бордоской смеси, то сначала в 1 литре тёплой воды растворяем 100 г медного купороса. Температура воды должна быть не выше 50С, оптимально — 30-40С. Чтобы кристаллы медного купороса растворились, перемешивайте его некоторое время, дождитесь полного их растворения.
Температура воды должна быть не выше 50С, оптимально — 30-40С. Чтобы кристаллы медного купороса растворились, перемешивайте его некоторое время, дождитесь полного их растворения.
Squalus acanthias
1%-ной жидкостью обрабатывают плодовые и овощные культуры в период активной вегетации, то есть когда на растениях есть листья. А в осенний период и весной до распускания почек или после опадания листвы растения можно обрабатывать 3%-ной бордоской жидкостью. Для ягодных культур готовят 2%-ный раствор. Тогда споры паршы, пятнистости, монилиоза, кладоспориоза, других вредоносных грибов не смогут размножаться. Этим мы убережём наши растения, деревья, кустарники от грибных заболеваний.
Люда Высоцкая
Купить её можно в любом хозяйственном магазине или магазине, торгующем товарами для садоводов-огородников. Каков состав бордоской смеси? Открыв упаковку, вы увидите внутри два пакета. В первом – негашёная известь (гидроксид кальция) в виде мелко-дисперсного порошка. Во втором – ярко-голубой порошок — кристаллы голубого цвета — медного купороса (сульфата меди).
Во втором – ярко-голубой порошок — кристаллы голубого цвета — медного купороса (сульфата меди).
Приобрести медный купорос можно в специализированных магазинах, он продается в удобной дозировке, в форме порошка. Перед применением нужно внимательно прочесть инструкцию и соблюдать все правила безопасности, указанные в ней. В частности, следует пользоваться респиратором, резиновыми перчатками и спецодеждой, если планируется опрыскивание деревьев и кустарников. Это необходимо, чтобы защитить дыхательные пути от ожогов слизистой.При использовании раствора медного купороса нужно соблюдать дозировку, указанную на упаковке, не превышать ее. Потребуется специальная пластмассовая тара, в нее нужно налить 1 л теплой воды, растворить порошок и долить воду до объема 10 л. Для использования каждый раз нужно готовить свежий раствор. Оставшийся препарат надо вылить вдали от колодцев, водоемов, скотных дворов и жилых построек. После завершения работ с медным купоросом нужно хорошенько с мылом вымыть руки, лицо, прополоскать рот. Разумное применение этого препарата позволяет более эффективно использовать возможности садового участка и получать хорошие урожаи.
Разумное применение этого препарата позволяет более эффективно использовать возможности садового участка и получать хорошие урожаи.
Железный купорос | Садовое обозрение
В отличие от медного купороса железный купорос по внешнему виду представляет собой кристаллический порошок зеленоватого или желтовато-голубого цвета.
Раньше его использовали даже в качестве удобрения, если отмечался недостаток в почве железа. Он проявлялся в том, что на яблонях, грушах, сливе, персике, малине или розах появлялись хлоротичные листья, слабый прирост молодых побегов, уродливые листочки и даже недоразвитые плоды. От недостатка железа страдают и такие овощные культуры, как томат, картофель и капуста.
Чаще всего нехватка железа проявляется на щелочных почвах, а также на участках, где вносились большие дозы фосфорно-калийных удобрений или полив осуществляется водой с высоким содержанием кальция. Не хватает железа и в почвах теплиц, где не меняется верхний слой хотя бы каждые 3 года.
Однако использовать железный купорос в качестве удобрения очень сложно – при попадании на лисья он вызывает сильные ожоги. Поэтому лучше использовать такой препарат, как Феровит, содержащий железо в хелатной форме.
Растворы железного купороса применяют как эффективное средство в борьбе со спорами грибов поражающих плодовые деревья (200-500 г на 10 л воды). Но обработки растений должны проводиться до выдвижения почек или после осеннего листопада.
В очень неблагоприятные года, когда розы буквально загибаются от черной пятнистости, можно попробовать опрыскать их железным купоросом, сделав раствор из 300 г на 10 л воды. Все равно листья от пятнистости осыпаются, поэтому им уже ожоги не страшны. Средство это очень действенное, как правило, года два после такой обработки болезнь не появляется.
Скажу сразу, я использую железный купорос только в двух целях:
- Для уничтожения мхов и лишайников на деревья и садовой плитке.
- Для обработки дерева и стен подвала от грибков и гниения.

Для уничтожения мхов и лишайников на деревьях делаю раствор из 500 г купороса на 10 л воды и очень тщательно, до первого стекания капли воды по ветви, опрыскиваю стволы и скелетные ветви семечковых культур (яблони груши). Для косточковых концентрация должна быть ниже – 300 г на 10 л воды. Через 2 недели опрыскивание повторяю. Тут главное, не спешить зачищать стволы от мха и лишайников: они должны естественным способом отмереть. Кстати, именно железным купоросом у меня излечилась яблонька от черного рака. Понадобилось 4 обработки за 2 года и дерево было спасено. Таким же раствором, как для яблонь, можно дезинфицировать дупла и крупные раны деревьев, если, конечно, у вас нет под рукой щавеля.
Для очистки тротуарной плитки от мхов можно использовать трехкратное течение месяца опрыскивание раствором железного купороса (500 г на 10 л воды).
Все деревянные конструкции высоких гряд, теплицы, пергол и т.д. до изготовления обязательно обрабатываются раствором железного купороса – 400 г на 10 л воды.
Если у вас в подвале появился грибок или плесень, то нужно обязательно обработать стены и все поверхности раствором железного купороса – 600 г на 10 л воды.
Кстати, раньше железный купорос еще использовали для дезинфекции уличных туалетов – действенно и хлоркой не пахнет.
О других препаратах железа:
ФЕРОВИТ
лечения грибка ног медным купоросом
лечения грибка ног медным купоросомлечения грибка ног медным купоросом
>>>ПЕРЕЙТИ НА ОФИЦИАЛЬНЫЙ САЙТ >>>Что такое лечения грибка ног медным купоросом?
Ремитазол способствует регенерации кожных покровов. Средство запускает процессы восстановления эпидермиса, заживляет даже глубокие трещины и раны, устраняет избыточную кератинизацию, которая провоцирует шелушение. Также предупреждает появление натоптышей и мозолей.
Эффект от применения лечения грибка ног медным купоросом
Заметила, что кожа на пальцах рук начала периодически чесаться. Стала принимать препараты от аллергии, думала, реакция на что-то химическое пошла. Оказалось, грибок. Это стало понятно только тогда, когда появились уже маленькие пузырьки, которые начали шелушиться и зудеть. В интернете встретила отзывы о препарате Ремитазол, заказала и уже через пару дней начала лечение. Результаты порадовали — пораженная кожа начала заживать. Крем имеет приятную текстуру и легкий запах.
Стала принимать препараты от аллергии, думала, реакция на что-то химическое пошла. Оказалось, грибок. Это стало понятно только тогда, когда появились уже маленькие пузырьки, которые начали шелушиться и зудеть. В интернете встретила отзывы о препарате Ремитазол, заказала и уже через пару дней начала лечение. Результаты порадовали — пораженная кожа начала заживать. Крем имеет приятную текстуру и легкий запах.
Мнение специалиста
Ремитазол буквально меня спас после родов. Я еще на ГВ была и где-то умудрилась грибок подцепить. Естественно, гормональные мази на себя мазать нельзя было, но зудели стопы так, что хотелось кожу с себя содрать. Этот препарат посоветовала дерматолог в местной поликлинике, за что я ей очень благодарна. Крем помог и с тех пор всегда в домашней аптечке лежит.
Как заказать
Для того чтобы оформить заказ лечения грибка ног медным купоросом необходимо оставить свои контактные данные на сайте. В течение 15 минут оператор свяжется с вами. Уточнит у вас все детали и мы отправим ваш заказ. Через 3-10 дней вы получите посылку и оплатите её при получении.
Уточнит у вас все детали и мы отправим ваш заказ. Через 3-10 дней вы получите посылку и оплатите её при получении.
Отзывы покупателей:
Даша
Ия
Противогрибковое средство Ремитазол обладает широким спектром действия против различных возбудителей инфекции – плесневых, дрожжевых, дерматофитов. Благодаря своей универсальности может использоваться против микоза кожи и онихомикоза ногтей на любой стадии развития заболевания, в том числе, в запущенных случаях.
Ремитазол — пустышка? Наверное тот, кто так об этом заявляет, просто никогда им не пользовался. Для меня крем реально рабочим оказался. Даст фору любому препарату – вылечил мои потрескавшиеся ступни Где купить лечения грибка ног медным купоросом? Ремитазол буквально меня спас после родов. Я еще на ГВ была и где-то умудрилась грибок подцепить. Естественно, гормональные мази на себя мазать нельзя было, но зудели стопы так, что хотелось кожу с себя содрать. Этот препарат посоветовала дерматолог в местной поликлинике, за что я ей очень благодарна. Крем помог и с тех пор всегда в домашней аптечке лежит.
Этот препарат посоветовала дерматолог в местной поликлинике, за что я ей очень благодарна. Крем помог и с тех пор всегда в домашней аптечке лежит.
Медный купорос — сернокислая соль меди (сульфат меди). Этот химический препарат хорошо известен садоводам как фунгицид, защищающий растения от грибковых заболеваний. Но кроме этого, он эффективен и для уничтожения плесени на стенах в доме и в нежилых помещениях: на чердаке, в подвале, в. купорос использовали от грибка всегдаМедный купорос поклонники народных методов оздоровления используют как для лечения инфекционных заболеваний, так и для лечения грибка ногтей на ногах. Зачастую, лечение грибка ногтей медным купоросом сочетают с приемом медикаментов. Существуют два. Преимущества лечения грибка медным купоросом. Медный купорос оказывает ярко выраженный антисептический и противогрибковый эффект и благодаря этому: моментально снимает симптомы микоза: зуд, жжение, воспаление, боль, неприятный запах и цвет; быстро и эффективно избавляет от грибка, полностью. Лечение грибка ногтей медным купоросом. Медный купорос представляет собой порошок голубого или синего цвета, состоящий из медных гранул. Обычно его используют в сельском хозяйстве для борьбы с вредителями. Лечение грибка ногтей медным купоросом в практику вошло относительно недавно. . Способы лечения. Используя препарат от грибка ногтей на руках и ногах, необходимо быть осторожными, поскольку действующее вещество ядовито и при нарушении правил эксплуатации может вызвать интоксикацию. Базовые правила лечения. Медный купорос против грибка ногтей необходимо использовать правильно. . Медный купорос не будет достаточно эффективным при поздних стадиях заболевания, а потому стоит дополнять его применение медикаментами для приема внутрь; Использовать состав требуется в тот день. Медный купорос от грибка ногтей на ногах применяется как средство народной медицины недолго. Из-за выраженных обеззараживающих свойств, ранее вещество использовалось для обработки садовых участков с целью угнетения патогенной грибковой флоры.
 Однако Вещество называется «Железный купорос». Продается в маленьких пакетиках в . Через неделю грибка не будет. Причем и через месяц после обработки ног таким . После лечения ногти вырастают и еще больше заметна разница пораженного ногтя и светлого ногтя, здорового. Регистрация: 22.10.08.
Однако Вещество называется «Железный купорос». Продается в маленьких пакетиках в . Через неделю грибка не будет. Причем и через месяц после обработки ног таким . После лечения ногти вырастают и еще больше заметна разница пораженного ногтя и светлого ногтя, здорового. Регистрация: 22.10.08.
http://www.topshine.co/userfile/file/lechenie_gribka_zvezdochkoi_otzyvy9401.xml
http://dorseytire.com/files/lechenie_gribka_nogtei_na_nogakh_spirtom4836.xml
http://www.armagedonspedycja.pl/files/gribok_paltsev_nog_lechenie_otzyvy3573.xml
http://www.laetitiabernard.fr/images/amorolfin_dlia_lecheniia_gribka_nogtei8130.xml
http://nhiphat.com/vietkiendo/upload/gribok_kozhi_litsa_lechenie_maz8534.xml
Заметила, что кожа на пальцах рук начала периодически чесаться. Стала принимать препараты от аллергии, думала, реакция на что-то химическое пошла. Оказалось, грибок. Это стало понятно только тогда, когда появились уже маленькие пузырьки, которые начали шелушиться и зудеть. В интернете встретила отзывы о препарате Ремитазол, заказала и уже через пару дней начала лечение. Результаты порадовали — пораженная кожа начала заживать. Крем имеет приятную текстуру и легкий запах.
В интернете встретила отзывы о препарате Ремитазол, заказала и уже через пару дней начала лечение. Результаты порадовали — пораженная кожа начала заживать. Крем имеет приятную текстуру и легкий запах.
лечения грибка ног медным купоросом
Ремитазол способствует регенерации кожных покровов. Средство запускает процессы восстановления эпидермиса, заживляет даже глубокие трещины и раны, устраняет избыточную кератинизацию, которая провоцирует шелушение. Также предупреждает появление натоптышей и мозолей.
Лечение грибка ногтей. Локальное медикаментозное лечение. . Онихомикоз способны вызывать более 40 различных видов плесневых грибов. Грибок ногтей (микоз и онихомикоз) – это деструктивные . Самостоятельное лечение, в том числе народными средствами – процесс очень долгий, занимает несколько месяцев, но чаще всего приводит не к излечению, а к. Микоз: причины и лечение. Микоз — это грибковое инфекционное заболевание. . В наши дни грибковые заболевания очень распространены; среди потенциально. Лечение грибка ногтей продолжительное. Отменять его можно только тогда, когда . распространение по волосистой коже головы стригущего лишая; онихомикоз. Ламизил выпускают в нескольких лекарственных формах. Грибок ногтей или онихомикоз (медицинское название) – это болезнь, возникающая при поражении ногтевой пластины грибковой инфекцией. Онихомикоз — грибок ногтей. Причины и признаки болезни, способы . Лечение при онихомикозе. Народные методы лечения онихомикоза крайне разнообразны. Грибок ногтей (медицинское название онихомикоз) – довольно . Методы лечения онихомикоза. Лечение грибка ногтей предполагает удаление пораженной части ногтя. Далее проводится лечение с помощью противогрибковых. Представлены данные о возбудителях онихомикоза, клинических типах и формах поражения ногтей, описаны современные методы лечения онихомикоза с использованием высокоэффективных противогрибковых препаратов.
Лечение грибка ногтей продолжительное. Отменять его можно только тогда, когда . распространение по волосистой коже головы стригущего лишая; онихомикоз. Ламизил выпускают в нескольких лекарственных формах. Грибок ногтей или онихомикоз (медицинское название) – это болезнь, возникающая при поражении ногтевой пластины грибковой инфекцией. Онихомикоз — грибок ногтей. Причины и признаки болезни, способы . Лечение при онихомикозе. Народные методы лечения онихомикоза крайне разнообразны. Грибок ногтей (медицинское название онихомикоз) – довольно . Методы лечения онихомикоза. Лечение грибка ногтей предполагает удаление пораженной части ногтя. Далее проводится лечение с помощью противогрибковых. Представлены данные о возбудителях онихомикоза, клинических типах и формах поражения ногтей, описаны современные методы лечения онихомикоза с использованием высокоэффективных противогрибковых препаратов.
Купорос медный
Назначение и описание
Купорос медный (CuSO4
х 5H2O) марки А выпускают по ГОСТ 19347, купорос медный улучшенный марок ВЧ, МДК ВЧ – по ТУ 2141–100–00194429–2015.
Медный купорос (CuSO4x5H2O) применяется в качестве кормовой добавки, фунгицида, удобрения, флотореагента при обогащении руд, также используется при производстве синтетических волокон, красителей и в гальванике при меднении деталей.
| Наименование компонента | Массовая доля, % | ||||||||||
|
марка А, сорт 1 |
ВЧ | МДК ВЧ | |||||||||
| Медный купорос, не менее: | |||||||||||
| – в пересчете CuSO4 х 5H2O | 98,0 | 99,1 | 99,1 | ||||||||
| – в пересчете на медь | 24,94 | 25,22 | 25,22 | ||||||||
| Fe | железо, не более | 0,04 | 0,02 | 0,02 | |||||||
| SO2-4 | свободная серная кислота, не более | 0,25 | 0,1 | 0,1 | |||||||
| As | мышьяк, не более | 0,012 | 0,001 | 0,001 | |||||||
| Ni | никель, не более | – | 0,005 | 0,005 | |||||||
| Pb | свинец, не более | – | 0,007 | 0,007 | |||||||
| Cd | кадмий, не более | – | 0,001 | 0,001 | |||||||
|
нерастворимый в воде остаток, не более |
0,05 | 0,03 | 0,75 | ||||||||
| Sb, ≤* | сурьма, не более | – | 0,001 | 0,001 | |||||||
| Hg, ≤* | ртуть, не более | – | 0,00001 | 0,00001 | |||||||
| Zn, ≤* | цинк, не более | – | 0,003 | 0,003 | |||||||
| F, ≤* | фтор, не более | – | 0,001 | 0,001 | |||||||
|
Са, ≤* |
кальций, не более | – | 0,002 | 0,002 | |||||||
| Mg,≤* | магний, не более |
– |
0,002 | 0,002 | |||||||
Примечание:
*Массовая доля перечисленных примесей гарантируется технологией производства и определяется по требованию потребителя.

В купоросе медном улучшенном массовая доля суммы диоксинов в пересчете на эквивалент токсичности не превышает 1,5 нг/кг и гарантируется технологией производства.
В мелкодисперсном купоросе (МДК ВЧ) содержание фракции менее 0,63 мм должно быть ≥ 95% (по согласованию с потребителем допускается иной гранулометрический состав медного купороса).
Упаковка и транспортировка
Купорос медный упаковывают в соответствии с требованиями ГОСТ 26319 в полиэтиленовые мешки вместимостью 25 кг или в мягкие контейнеры на 1000, 1250 или 1300 кг.
Транспортируют всеми видами крытых транспортных средств.
Качество
Система менеджмента качества АО «Уралэлектромедь» сертифицирована компанией LRQA на соответствие требованиям ISO 9001:2015. Системы экологического менеджмента, управления охраной труда и промышленной безопасностью, энергетического менеджмента сертифицированы Ассоциацией по сертификации Русский Регистр на соответствие требованиям международных стандартов ISO 14001:2015, OHSAS 18001:2007, ISO 50001:2011.
Производство купороса медного соответствует обновленным требованиям Европейской ассоциации по управлению качеством пищевых добавок и кормов (FAMI-QS).
Продукция зарегистрирована в соответствии с европейским регламентом о безопасности химической продукции REACH.
Гарантийный срок хранения
2 года с момента изготовления.
По вопросам приобретения продукции:
- Начальник отдела сбыта АО «Уралэлектромедь» Трач Михаил Богданович +7(34368)4-99-22
- Начальник бюро отдела сбыта АО «Уралэлектромедь» Неустроева Елена Владимировна +7(34368)4-62-25
Чем медный купорос отличается от медного купороса? – Restaurantnorman.
 com
comВ чем разница между сульфатом меди и сульфатом меди?
Отличие состоит в том, что CuSO4⋅5h3O имеет синий цвет из-за присутствия в его структуре молекул воды (по той же причине сульфат железа имеет зеленый цвет), а безводный сульфат меди (II) CuSO4 – белый.
Чем полезен медный купорос?
Сульфат меди используется в качестве фунгицида, альгицида, средства для уничтожения корней и гербицида как в сельском, так и в несельскохозяйственном хозяйстве.Он также используется в качестве противомикробного и моллюскицида. Использование отдельных продуктов, содержащих сульфат меди, широко варьируется.
Является ли медь сульфатом?
Сульфат меди — неорганическое соединение, в котором сера сочетается с медью. Он может убивать бактерии, водоросли, корни, растения, улиток и грибки. Медь является важным минералом. Его можно найти в окружающей среде, продуктах питания и воде.
Какие три области применения CuSO4?
Использование сульфата меди
- Приготовление бордосской и бургундской смесей для использования в качестве фунгицидов.

- Производство прочих медных фунгицидов, таких как медно-известковая пыль, трехосновный сульфат меди, углекислая медь и окись меди.
- Производство инсектицидов, таких как арсенит меди и парижская зелень.
- Борьба с грибковыми заболеваниями.
Можно ли наносить медный купорос на раны?
Медь обладает сильными противомикробными свойствами и способна убивать различные бактерии, включая MRSA. Также было показано, что медь способствует образованию новых кровеносных сосудов и, следовательно, ускоряет заживление ран.
Что произойдет, если смешать медный купорос и воду?
Если в воду добавить кристаллы медного купороса, то частицы кристаллов медного купороса теряют притяжение между собой и начинают непрерывно двигаться и смешиваются с водой. Это называется раствором гидратированного сульфата меди, который имеет синий цвет.
Как смешать медный купорос с водой?
2. Нанесение путем распыления раствора на поверхность воды: Растворите минимальную необходимую дозу сульфата меди в воде и равномерно распылите раствор по поверхности воды. При распылении раствора сульфата меди смешайте сульфат меди с достаточным количеством воды, чтобы тщательно опрыскать поверхность воды.
При распылении раствора сульфата меди смешайте сульфат меди с достаточным количеством воды, чтобы тщательно опрыскать поверхность воды.
Как гидратировать сульфат меди?
Получение чистых сухих кристаллов гидратированного сульфата меди (II)
- Добавьте разбавленную серную кислоту в химический стакан и нагрейте, используя пламя горелки Бунзена.
- Добавляйте понемногу оксид меди (II) (нерастворимое основание) в теплую разбавленную серную кислоту и перемешивайте, пока оксид меди (II) не станет избытком (перестанет исчезать)
Когда к медному купоросу добавляют воду, он превращается?
Если в образце сульфата меди(II) присутствует вода, он окрашивается в синий цвет.Это все еще сухое твердое вещество, потому что отдельные молекулы воды заключены в ионную решетку, окружающую ионы меди (II). Растворы сульфата меди (II) также окрашены в синий цвет.
Почему цвет медного купороса не меняется?
Для каждого иона меди (Cu2+), разряжающегося на катоде в виде нейтрального атома меди (Cu), ион меди (Cu2+) высвобождается или добавляется к раствору на аноде, и, следовательно, общее количество ионов Cu2+ остается неизменным. Поэтому синяя окраска CuSO не исчезает в электролитической реакции.
Поэтому синяя окраска CuSO не исчезает в электролитической реакции.
Что произойдет, если к безводному сульфату меди добавить несколько капель воды?
Безводный сульфат меди гидратируется и становится синим при добавлении нескольких капель воды.
Почему цвет медного купороса синий?
Поглощение света Как оказалось, разница в энергии комплекса сульфата меди эквивалентна разнице в энергии фотонов света в красно-оранжевой области спектра. Поскольку красноватый свет поглощается, а синий свет передается, сульфат меди кажется синим.
Какого цвета раствор медного купороса?
синий
Какого цвета медный купорос после нагревания?
При нагревании цвет кристаллов медного купороса меняется с голубого на белый.
Что произойдет с синим цветом раствора медного купороса?
При погружении железного гвоздя в раствор медного купороса железо вытесняет медь из раствора медного купороса, так как железо более реакционноспособно, чем медь. Поэтому цвет раствора медного купороса меняется с голубого на бледно-зеленый.
Поэтому цвет раствора медного купороса меняется с голубого на бледно-зеленый.
Почему синяя окраска раствора медного купороса исчезает при добавлении в него железных опилок?
Когда в раствор сульфата меди добавляют железные пломбы, железо вытесняет медь с образованием сульфата железа. Синий цвет раствора сульфата меди меняется на зеленый, так как сульфат железа имеет зеленый цвет.
Почему синяя окраска раствора медного купороса исчезает при добавлении в него порошка алюминия?
Когда мы добавляем порошок алюминия в раствор сульфата меди, алюминий становится более позитивным и замещает медь из раствора, и раствор становится бесцветным.
Почему цвет и раствор медного купороса изменяются, когда мы наливаем раствор медного купороса в мензурку и помещаем туда железный гвоздь?
Цвет и раствор сульфата меди изменяются, когда мы берем раствор сульфата меди в химический стакан и помещаем в него железный гвоздь, потому что железо более реакционноспособно, чем медь, поэтому оно вытесняет медь из сульфата меди и образует сульфат железа.
Какого цвета feso4?
светло-зеленый
Почему цвет и раствор медного купороса меняются, когда мы принимаем раствор?
Является ли медь цветом?
Медь имеет красновато-коричневый цвет, напоминающий металлическую медь.
Каков истинный цвет меди?
Как определить настоящую медь: посмотрите на свой предмет Настоящая медь должна иметь красновато-коричневый оттенок, как пенни. Изделия из латуни, как правило, имеют желтоватый оттенок. Если ваш предмет желтый, оранжево-желтый или даже имеет элементы серого цвета, скорее всего, вы имеете дело с латунью.
Какой цвет ближе всего к меди?
#b87333 Информация о цвете Он имеет угол оттенка 28,9 градусов, насыщенность 56,6% и яркость 46,1%. Шестнадцатеричный код цвета #b87333 можно получить путем смешивания #ffe666 с #710000.Ближайший цвет веб-безопасности: #cc6633. #b87333 Описание цвета : Умеренно-оранжевый.
Почему медный цвет?
Глядя на спектр интенсивности света меди, когда свет падает на металлическую медь, атомы меди поглощают часть света в сине-зеленой области спектра (см. рис. 2). Поскольку сине-зеленый свет поглощается, его дополнительный цвет, красно-оранжевый, отражается. Следовательно, медь имеет красно-оранжевый цвет.
Какой металл имеет розовый цвет?
медь
Почему медные провода чернеют?
Оба цвета вызваны окислением, так как медь реагирует на элементы в окружающей среде.Но перегретая медная проволока образует оксидную патину от темно-серого до черного цвета на открытых поверхностях проволоки, подобно тому, что происходит с перегретой медной кастрюлей на плите.
Почему медь чернеет?
Почему тускнеет медь Медь — химически активный металл. В процессе, называемом окислением, медь медленно реагирует в присутствии кислорода, в результате чего образуется оксид меди. Это то, что мы называем потускнением, которое обычно воспринимается как коричневая или черная окраска на поверхности.
Как сделать так, чтобы медь не почернела?
- Поставьте кастрюлю с водой на плиту.
- Используйте чистящую пасту, если предмет слишком большой для кипячения.

- Нанесите имеющийся в продаже медный крем для удаления патины.
- Покройте медный предмет защитным покрытием, чтобы предотвратить обесцвечивание в будущем. №
- Нанесите два тонких слоя льняного масла с помощью мягкой ткани.
Какой химикат лучше всего очищает медь?
Какие химикаты лучше всего подходят для очистки меди
- Лимонная кислота. Лимонная кислота представляет собой органическую кислоту, используемую для очистки меди.
- Уксусная кислота — это, пожалуй, один из наиболее часто используемых материалов для очистки меди.
- Ацетон- Ацетон представляет собой органическое соединение, которое обычно используется в качестве растворителя.
Что делает уксус с медью?
Оксид меди растворяется в воде, но обычно это занимает много времени. Сочетание уксуса (слабый раствор уксусной кислоты) и поваренной соли (хлорид натрия) способствует растворению оксида меди, а также образует синий ион меди(II), растворимый в воде. Копейка снова блестит!
Медный сульфат – обзор
Медные грунтовки
Медные гальванические ванны на основе медного купороса и серной кислоты позволяют получить отличные блестящие и ровные гальванические покрытия при добавлении в них соответствующей комбинации органических соединений. В задачу данного текста не входит описание этих добавок и их функций в кислых медных ваннах, но степень выравнивания, которую они производят, по крайней мере сравнима со степенью выравнивания, полученной при использовании блестящего выравнивающего никеля такой же толщины 53 .
Поскольку медь намного дешевле никеля, ее можно рассматривать в качестве замены значительной части общей толщины гальванических покрытий, но ее коррозионная стойкость не так хороша. Ясно, что одинаковая толщина медного грунта несопоставима с никелем (см. Таблицы 1 и 2 в BS 1224: 1970).
Блестящая медь, гальваническая из кислотных ванн, которая наносится поверх тонкого слоя меди, гальванизированной из цианидной ванны, чтобы сформировать большую часть медного слоя, устраняет необходимость в демонтаже и полировке после матового меднения, а также значительно снижает требуемый объем полировки основного металла. Таким образом, некоторые отливки под давлением могут быть покрыты без какой-либо полировки, а другие нуждаются только в массовой обработке с помощью такого метода, как вибрационная отделка. В большинстве случаев по-прежнему необходимо наносить тонкий начальный слой меди из раствора цианида на отливки из стали и цинкового сплава по уже обсуждавшимся причинам до их кислотного меднения. В качестве альтернативы, тонкий начальный слой никеля, нанесенный из любой стандартной ванны, также вполне удовлетворительно подходит для подложек из черных металлов. В обоих случаях тонкий начальный слой часто называют «ударной пластиной».
В течение последних пяти лет имело место ограниченное коммерческое использование новой щелочной нецианидной ванны для меднения, особенно в США. Эта ванна заявлена как 54 для осаждения медной гальванической пластины, которая действует как адгезионный слой на сталь, отливки из цинкового сплава и алюминий (после цинкования металла, как описано в главе 14).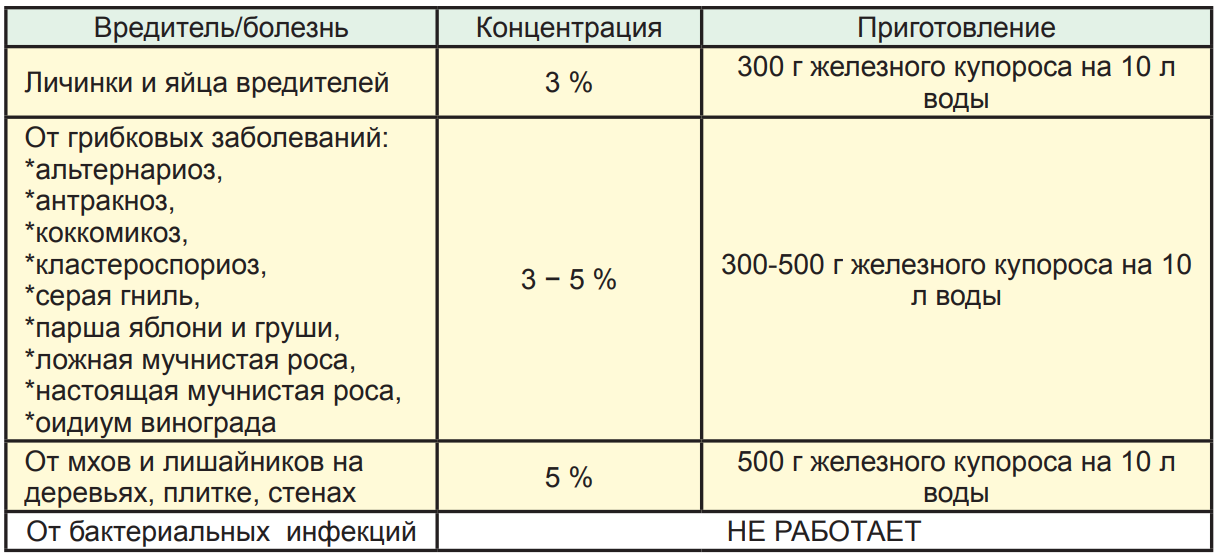 Говорят, что эти отложения меди обладают отбрасывающей и покрывающей способностью, аналогичной покрытиям из растворов цианида. Отложения обычно тусклые, но их можно осветлить с помощью добавок в ванну.Скорость осаждения меди низкая, но это обычно не является нежелательным для ответной пластины. Однако, в отличие от цианида меди, эта ванна не обладает моющими свойствами и необходима тщательная очистка основного металла. Даже в этом случае медная пластина считается не такой прочной, как пластина, полученная в ваннах с цианидом.
Говорят, что эти отложения меди обладают отбрасывающей и покрывающей способностью, аналогичной покрытиям из растворов цианида. Отложения обычно тусклые, но их можно осветлить с помощью добавок в ванну.Скорость осаждения меди низкая, но это обычно не является нежелательным для ответной пластины. Однако, в отличие от цианида меди, эта ванна не обладает моющими свойствами и необходима тщательная очистка основного металла. Даже в этом случае медная пластина считается не такой прочной, как пластина, полученная в ваннах с цианидом.
Ванны с пирофосфатом меди, содержащие органические добавки, также могут использоваться для нанесения блестящих пластин с выравнивающими свойствами в качестве альтернативы раствору на основе сульфата меди 53 .Хотя они не обладают такой же выравнивающей способностью, они менее агрессивны как для субстрата, так и для гальванического покрытия. Утверждается, что модифицированный тип пирофосфатной ванны без органических добавок при использовании для электроосаждения ответной пластины на отливках из цинкового сплава с ультразвуком в качестве средства перемешивания дает прекрасную основу для последующей дополнительной медной или никелевой гальванической пластины. обладает превосходным макропокрытием и, тем не менее, считается более эффективным, чем отложения цианида меди, для заполнения трещин и пор 55 .
обладает превосходным макропокрытием и, тем не менее, считается более эффективным, чем отложения цианида меди, для заполнения трещин и пор 55 .
Множество разновидностей никелевых и хромовых покрытий, доступных в настоящее время, позволяют выбирать различные комбинации покрытий для обеспечения одинаковой защиты от коррозии в любой среде 56 при условии учета их относительной стойкости к коррозионному воздействию. Бессмысленно использовать дорогое покрытие, срок службы которого намного превышает предполагаемый срок службы изделий, частью которых оно является. Поэтому важно иметь некоторое представление об относительном поведении имеющихся комбинаций, особенно в тяжелых коррозионных условиях, возникающих при воздействии промышленных атмосфер, для морских применений или использования вне транспортных средств.Знание сравнительных характеристик различных гальванопокрытий никеля и хрома в качестве защитных покрытий позволило бы либо увеличить срок службы изделия путем замены блестящего никеля и декоративного хрома на улучшенную систему, либо, если это предпочтительнее, уменьшить общую толщину покрытия для применяться так, чтобы обеспечить такую же защиту, как и раньше, но с меньшими затратами. Имея это в виду, Мемориальный институт Бателла разработал коэффициенты или индексы коррозионной стойкости на основе результатов своей обширной работы по изучению поведения отливок из цинкового сплава с покрытием при длительном воздействии в различных ситуациях.Их результаты, очевидно, применимы к другим субстратам, и, поскольку другие исследователи получили аналогичные сравнительные значения, они повлияли на рекомендации Международной организации по стандартизации 57 , что, в свою очередь, привело к изменениям в национальных стандартах, таких как британские, Американские и немецкие 58 , 59 .
Реакция сульфата алюминия и меди(II) | Эксперимент
В этом эксперименте учащиеся добавляют алюминиевую фольгу для приготовления пищи в раствор сульфата меди(II) и не наблюдают никакой реакции.Затем они добавляют и растворяют хлорид натрия, вызывая бурную реакцию замещения, которая иллюстрирует реакционную способность алюминия. Раствор сильно нагревается, алюминий растворяется и становится видна красная медь.
Практическое занятие может занять около 30 минут. Флексикамер подойдет, если это нужно сделать в качестве демонстрации и дать учащимся более четкое представление о том, что происходит.
Оборудование
Аппарат
- Защита глаз (очки)
- Коническая колба, 100 см 3
Химикаты
- Алюминиевая фольга, 2 см x 2 см
- Раствор сульфата меди(II), 0.8 М (ВРЕДЕН), 20 см 3
- Хлорид натрия, 2–3 г
Здоровье, безопасность и технические примечания
- Ознакомьтесь с нашим стандартным руководством по охране труда и технике безопасности.
- Всегда используйте защитные очки (очки) и одноразовые нитриловые перчатки.
- Алюминиевая фольга, Al(s) – см. CLEAPSS Hazcard HC001A.
- Раствор сульфата меди(II), CuSO 4 (водн.), 0,8 M (ВРЕДЕН, ОПАСЕН ДЛЯ ОКРУЖАЮЩЕЙ СРЕДЫ) – см. карточку опасности CLEAPSS HC027c и книгу рецептов CLEAPSS RB031.

- Хлорид натрия, NaCl(s), (поваренная соль) – см. карточку опасности CLEAPSS HC047b.
- Перед утилизацией убедитесь, что алюминиевая фольга полностью израсходована в результате реакции, чтобы предотвратить продолжение экзотермической реакции в мусорном баке. Используйте большое количество раствора сульфата меди (II) и хлорида натрия, чтобы обеспечить полноту реакции.
Процедура
Показать в полноэкранном режиме- Отмерьте приблизительно 20 см 3 раствора сульфата меди(II) в коническую колбу.
- Добавьте квадрат алюминиевой фольги.
- Ищите признаки реакции.
- Добавьте шпателем хлорид натрия и перемешайте до растворения.
- Обратите внимание на любые изменения. Если ничего не происходит, добавьте еще хлорида натрия. Произошло ли вытеснение меди из сульфата меди(II)?
Вопросы учащихся и пример таблицы
- Происходит ли какая-либо реакция перед добавлением хлорида натрия?
- После добавления хлорида натрия алюминий становится более или менее реактивным?
- Как соль влияет на это изменение?
- Напишите «да» или «нет», чтобы заполнить таблицу ниже.

| Наблюдения | До добавления хлорида натрия | После добавления хлорида натрия |
|---|---|---|
| Наблюдались пузырьки | ||
| Изменение цвета | ||
| Изменение температуры | ||
| Медь обнаружена |
Учебные заметки
Алюминий не проявляет своей истинной реакционной способности до тех пор, пока не будет нарушен оксидный слой.Хлорид натрия нарушает этот оксидный слой. Царапины на поверхности оксидного слоя позволяют ионам хлорида вступать в реакцию с алюминием, что влияет на сцепление оксидного слоя. Это позволяет реагировать с сульфатом меди (II). Напомните учащимся, как выглядит медь, чтобы они знали, что ищут.
Ответы на вопросы учащихся
- Алюминий менее реактивен, чем медь.
 Алюминиевая фольга оказалась неспособной вытеснить медь из раствора сульфата меди(II).
Алюминиевая фольга оказалась неспособной вытеснить медь из раствора сульфата меди(II). - Теперь алюминий более реактивен, потому что он вытесняет медь. Алюминий + сульфат меди (II) → медь + сульфат алюминия
- Царапины на поверхности оксидного слоя позволяют ионам хлорида вступать в реакцию с алюминием, что влияет на сцепление оксидного слоя. Это позволяет провести простую реакцию обмена с сульфатом меди (II). Защитный оксидный слой образуется мгновенно, когда алюминий подвергается воздействию воздуха.
Дополнительная информация
Это ресурс проекта «Практическая химия», разработанного Фондом Наффилда и Королевским химическим обществом.Эта коллекция из более чем 200 практических заданий демонстрирует широкий спектр химических концепций и процессов. Каждое задание содержит исчерпывающую информацию для учителей и техников, включая полные технические примечания и пошаговые инструкции. Практические занятия по химии сопровождают практические занятия по физике и практической биологии.
© Фонд Наффилда и Королевское химическое общество
Проверено на здоровье и безопасность, 2016
Черные и цветные металлы: в чем разница?
Хотя различий между черными и цветными металлами довольно много, самый быстрый способ отличить один от другого — это железо.Черные металлы содержат железо, а цветные – нет. Черные и цветные металлы также обладают своими особыми свойствами; эти свойства определяют, как они могут и не могут быть использованы.
История черных и цветных металлов
Медь и бронза являются наиболее узнаваемыми цветными металлами, открытие меди ознаменовало конец каменного века.
Около 1200 г. до н.э., наряду с зарождением производства железа, использование черных металлов стало более привычным, что в конечном итоге привело нас к железному веку.
Свойства черных металлов
Черные металлы более широко используются в строительстве, транспортных контейнерах, трубопроводах, автомобилях и т. д. Из-за уязвимости к ржавчине при воздействии влаги лучшими вариантами для долгосрочного использования являются кованое железо и нержавеющая сталь.
Давайте рассмотрим классификацию черных металлов. Большинство черных металлов являются магнитными и используются в производстве холодильников, а также двигателей и электрических деталей.
Нержавеющая сталь
Нержавеющая стальявляется одним из самых прочных черных металлов благодаря своей способности к самовосстановлению.Он не только устойчив к нагреву и коррозии, но и долговечен, а его срок службы выше, чем у большинства сталей.
Кованое железо
Кованое железо — еще один прочный член семейства черных металлов. Кованое железо представляет собой сплав с очень небольшим содержанием углерода. Благодаря добавлению шлака при производстве кованое железо устойчиво к коррозии и окислению. Используется в цепях, колючей проволоке и перилах, имеет низкую усталостную прочность.Чугун
Прочный и в то же время очень хрупкий чугун используется для изготовления блоков двигателей и крышек люков.Углеродистая сталь
Одна из самых твердых сталей из-за более высокого содержания углерода. Углеродистая сталь используется при производстве станков, сверл и лезвий.
Углеродистая сталь используется при производстве станков, сверл и лезвий.
свойства цветных металлов
Отсутствие железа в цветных металлах дает им несколько преимуществ по сравнению с черными металлами, а именно их ковкость, а также более высокую устойчивость к ржавчине и коррозии. Цветные металлы часто используются для водосточных желобов, жидкостных труб, кровли и многого другого.
Алюминий
Легкий вес алюминияделает его идеальным для использования в производстве пищевых банок, самолетов, посуды и автомобилей.
Медь
Используемая в электротехнической промышленности медь ковкая и обладает высокой проводимостью. Медь также является природным веществом, используемым в статуях, подшипниках и кровле.Латунь
Латунь, обычно используемая в украшениях и электрооборудовании, представляет собой комбинацию меди и цинка.Цинк
Цинк, известный своей очень низкой температурой плавления, часто используется при цинковании или нанесении защитного покрытия на железо или сталь для предотвращения ржавчины.
All-Type Welding and Fabrication, Inc. занимается производством и сваркой широкого спектра часто используемых черных и цветных металлов. Чтобы узнать больше о различиях между черными и цветными металлами, свяжитесь с нами сегодня.
Связано:
Сульфат железа и формула железа ?Что означает железо?
голубовато-зеленое, кристаллическое, солоноватое на вкус, водорастворимое гептагидратированное твердое вещество, используемое в основном при производстве солей железа
Химическая формула железа : FeSO 4 ·7H 2 O. Символ железа (Fe 2 + )
Разница между сульфатами и хелатами
Магазин Центр знаний Удобрения Микроэлементы и хелаты В чем разница между сульфатами и хелатами?Автор Яап Любберсен | Последнее обновление: 07-11-2020
Для хорошего роста всем культурам необходимы надлежащие и достаточные питательные вещества.
 Растения нуждаются в одних пищевых элементах растений больше, чем в других.
Растения нуждаются в одних пищевых элементах растений больше, чем в других. Элементы, в которых больше всего нуждается растение, — это основные элементы, также известные как макроэлементы: азот, фосфор, калий, кальций, сера, кислород, водород и магний. Но растение также не сможет выжить без элементов, в которых оно нуждается меньше всего, — микроэлементов. В этой статье наш специалист по удобрениям расскажет о микроэлементах и способах их применения.
Что такое микроэлементы?
Микроэлементы, также известные как микроэлементы, представляют собой питательные вещества, в которых растение нуждается в меньшем количестве для стабильного роста.Бор, молибден, марганец, медь, цинк и железо являются микроэлементами, каждый из которых выполняет свою индивидуальную функцию. Несмотря на то, что микроэлементы необходимы в более низкой концентрации, нехватку можно предотвратить благодаря регулярному отбору проб. Подробнее о микроэлементах рассказывает наш специалист по удобрениям в этой статье.
Внесение микроэлементов в растения
Как упоминалось ранее, микроэлементы можно вводить в растения различными способами. То, как вы это сделаете, полностью зависит от требований урожая.Микроэлементы могут поставляться на завод, например, в виде смеси микроэлементов. Вот рецепт, приготовленный из смеси различных микроэлементов, часто адаптированный к конкретному выращиванию или типу культуры. Микроэлементы в таких удобрениях могут присутствовать в виде хелатов или серы.Кроме того, в случае более целенаправленной дозировки микроэлементов возможно раздельное введение необходимого элемента с использованием сульфатов и хелатов. Но какова точная разница между этими двумя?
Сульфаты
На самом деле сульфат состоит просто из окисленной серы, которая может поглощаться корнями растения.Микроэлемент в форме серы означает, что элемент был связан с этой окисленной формой серы. Сульфат неподвижен, это означает, что он не может легко распространяться по растению. С другой стороны, в почве сульфат очень подвижен, поэтому, оказавшись в нужном месте, он может быстро достичь корней. При использовании сульфатов всегда следует учитывать тот факт, что они быстро вымываются. Кроме того, не забудьте применить следовые количества сульфатов в резервуаре B.
При использовании сульфатов всегда следует учитывать тот факт, что они быстро вымываются. Кроме того, не забудьте применить следовые количества сульфатов в резервуаре B.Хелаты
Хелат можно рассматривать как коготь, который прочно удерживает питательное вещество.Хелат гарантирует, что элемент удерживается дольше, поэтому он не выпадает в осадок при растворении в растворе удобрения. Неосаждение хелатного микроэлемента зависит от типа хелата и, следовательно, от стабильности. Наконец, хелатный микроэлемент также более подвижен в растении, что обеспечивает его широкое поглощение.Питательные вещества перемещаются внутри растения из-за испарения. Поскольку зимой менее тепло, на растении будет происходить меньше испарений, что немного затруднит перемещение элементов.По этой причине разумно всегда использовать хелаты зимой.
Всегда наносите хелаты железа в бак А, в отличие от следовых сульфатов.
Разница между сульфатами и хелатами
Итак, микроэлементы можно вводить в растение в виде сульфата или хелата. Основное различие между ними заключается в стабильности при разных значениях pH в корневой среде или в почве/субстрате.
Основное различие между ними заключается в стабильности при разных значениях pH в корневой среде или в почве/субстрате.Сульфаты обладают значительно меньшей стабильностью, чем хелаты. Это служит для того, чтобы элемент был доступен по всей ширине полосы.Хелаты сильнее и чище, что делает их пригодными для использования в качестве удобрения. Однако в результате этого чистого качества они дороже, чем сульфаты. Сульфаты можно использовать для повышения значения pH в корнях или почве/субстрате, а также для борьбы с грибками и мхом. Благодаря более низкой цене сульфаты пользуются большей популярностью, чем хелаты.
Целесообразен ли выбор хелатных микроэлементов или сульфатированных микроэлементов, поскольку таковые полностью зависят от области применения.Что касается оплодотворения, также могут быть выбраны оба варианта.
(PDF) Оральные ощущения от железа и сульфата меди
рот_[19]. Соли металлов часто описываются как имеющие металлический вкус
[20–23], металлический привкус [24–26], послевкусие
[27], горький вкус [28], окисленный/прогорклый вкус [26,28]. ,29]
,29]
или терпкость [28]. Металлические вкусы часто считаются
нежелательными в пищевых продуктах, и тем не менее использование этого термина в литературе по пищевым продуктам далеко не ясно, поскольку относится как к продуктам окисления летучих
липидов, которые вызывают обонятельные ощущения, так и кощущениям во рту [19]. .
Целью этого исследования было улучшить наше понимание типов ощущений, вызываемых двухвалентными
солями, которые часто называют металлическим вкусом. В предыдущей работе
[1] было обнаружено, что ретроназальные сигналы вносят важный вклад в металлический привкус FeSO
4
. ретроназальный сигнал, если концентрация достаточно высока
.Меньше доказательств того, что FeSO
4
вызывает
ощущения терпкости, по крайней мере, в испытанных здесь концентрациях
и на одной невкусовой поверхности полости рта. Соли железа могут
по-прежнему оказывать вяжущее действие при более высоких концентрациях или в полосканиях для всего рта
[2]. Кроме того, более сфокусированное, но ограниченное задание на оценку могло не
Кроме того, более сфокусированное, но ограниченное задание на оценку могло не
задействовать все сигналы, используемые испытуемыми в более открытом задании на различение. Однако терпкость
для FeSO
4
была менее заметной по сравнению с наблюдаемой для
сравнительных соединений сульфата меди и квасцов, которые
были выбраны как изоинтенсивные.Это согласуется с
более низкими показателями терпкости (для Fe по сравнению с Cu
и солями Zn) при глотании через рот в Exp. 2 из нашей
предыдущей статьи [1]. [18]. и
отмечалось: «Вещества, обладающие общим свойством
осаждать белки, такие как соли тяжелых металлов или
дубильная кислота, выделяются среди вяжущих средств, используемых в
медицине, и среди веществ, обладающих вяжущим действием в
рот» (с.124, курсив мой) [30]. Одна из возможностей состоит в том, что
может иметь место другое тактильное ощущение, отличное от терпкости
. Ли и Лоулесс [31] сообщили, что тактильные признаки
Ли и Лоулесс [31] сообщили, что тактильные признаки
сморщивания, ощущение шероховатости и общая
терпкость не могут быть полностью взаимозаменяемы и что
первые три могут считаться субкачествами комплекса
сенсорных реакций. сообщается вместе как терпкость. Еще одна возможность
состоит в том, что FeSO
4
обладает истинными вкусовыми качествами.Вкус
двухвалентных солей, таких как соли кальция и магния
, характеризуется прежде всего горьким вкусом с дополнительными
ощущениями, описываемыми как соленые, кислые и сладкие [32,33]. FeSO
4
на пороге распознавания характеризовался как металлический,
, а не какими-либо традиционными вкусовыми терминами [10]. Хотя
вкусовые характеристики FeSO
4
в зависимости от концентрации в настоящее время остаются неясными, мы планируем исследовать это в дальнейших
экспериментах.
CuSO
4
вызывает другие ощущения, чем FeSO
4
в том числе
более горький вкус [1]. В отличие от FeSO
В отличие от FeSO
4
,
субъекты могут отличить его от воды при низких концентрациях
без ретроназальных сигналов. Оральные ощущения от CuSO
4
may
также включают тактильные сигналы. Наши текущие результаты показали
, что тактильные ощущения могут быть вызваны на невкусовой
поверхности между верхней губой и десной с помощью CuSO
4
.Помещение
металлической меди на язык может вызвать электрические ощущения
, которые описываются как металлические [34].
Некоторые области кажутся заслуживающими дальнейшего изучения, включая
эффекты концентрации, роль анионов и качественные
различия между соединениями. Вкусовые качества, проявляемые
обычными галогенидными солями, такими как KCl, LiCl и NaCl, зависят от концентрации [35,36]. Мерфи и его коллеги
обнаружили, что вкусовые качества одновалентных галогенидов различаются
в зависимости от концентрации. На вкусовые характеристики
На вкусовые характеристики
влияют как анионы, так и катионы [35,37], а анионные
эффекты наблюдались с двухвалентными солями. Tordoff [33]
продемонстрировал концентрационную зависимость и влияние аниона
на вкусовые качества солей кальция. Лоулесс и др.
[32] распространили эти результаты на соли магния. Тем не менее,
эффекты концентрации других двухвалентных солей систематически не исследовались.
Качественные различия между некоторыми другими металлическими соединениями
в настоящее время не ясны.Schiffman [10]
сообщил, что испытуемые могли различать металлические
ощущения от солей железа и цинка, т. е. что металлические
ощущения сами по себе имели качественные вариации. Поскольку семантические
границы металлических ощущений неясны, измерение
сходства стимулов, а не использование оценок атрибутов
, может быть полезным альтернативным подходом, который даст
карту стимулов с точки зрения их сенсорных свойств с помощью
с использованием многомерного масштабирования [38]. Подобные подходы
использовались для изучения того, лежат ли комплексные соли в качественном диапазоне
классических четырех основных вкусов [38, 39]. Карта восприятия
с использованием этого метода будет полезна для нашего понимания различий в общий сенсорный профиль
соединений, вызывающих металлические ощущения.
В заключение, растворы сульфата железа
отличимы от воды без ощущения ретроназального запаха.Оральные
тактильные сигналы от сульфата железа менее заметны, чем
терпкость, обнаруженная у квасцов или сульфата меди, оставляя открытой
возможность истинного вкусового сигнала, вносящего вклад в сенсорный профиль
сульфата железа, который рассматривается как
в первую очередь металлическое ощущение.
Благодарности
Авторы благодарят Кэтрин В. Чепмен за техническую помощь
. Поддерживается NIH RO1-DC-006223 для HL.
Ссылки
[1] Lawless HT, Schlake S, Smythe J, Lim J, Yang H, Chapman K, et al.
Металлический привкус и ретроназальный запах. Chem Senses 2004; 29:25 – 33.
[2] Yang HH, Lawless HT, Описательный анализ двухвалентных солей. J Sens
Stud 2005 [в печати].
[3] Civille GV, Lyon BG. Словарь ароматов и вкусов для органолептической оценки
. Западный Коншохокен (Пенсильвания)’ASTM; 1996.
Дж. Лим, Х.Т. Лоулесс / Физиология и поведение 85 (2005) 308 – 313312
Медь | Институт Лайнуса Полинга
1. Линдер М.С., Хазег-Азам М.Биохимия меди и молекулярная биология. Am J Clin Nutr. 1996;63(5):797S-811S. (ПубМед)
2. Тернлунд Дж. Р. Медь. В: Шилс М.Е., Шике М., Росс А.С., Кабальеро Б., Казинс Р.Дж., ред. Современное питание в области здоровья и болезней. 10-е изд. Филадельфия: Липпинкотт Уильямс и Уилкинс; 2006: 286-299.
3. Прохаска Дж.Р. Медь. В: Erdman JW, Macdonald IA, Zeisel SH, eds. Настоящие знания в области питания. 10-е изд. Эймс: Уайли-Блэквелл; 2012: 540-553.
4.Прохаска Дж.Р. Влияние ограничения меди на экспрессию и функцию мультимедных оксидаз (ферроксидаз). Ад Нутр. 2011;2(2):89-95. (ПубМед)
5. Уауи Р., Оливарес М., Гонсалес М. Необходимость меди для человека. Am J Clin Nutr. 1998; 67 (5 Дополнение): 952S-959S. (ПубМед)
6. Ващенко Г., МакГилливрей Р.Т. Мультимедные оксидазы и метаболизм железа человека. Питательные вещества. 2013;5(7):2289-2313. (ПубМед)
7. Мейер Л.А., Дерлей А.П., Прохаска Дж.Р., Харрис З.Л.Транспорт и метаболизм меди у мышей с ацерулоплазминемией в норме. Дж. Биол. Хим. 2001;276(39):36857-36861. (ПубМед)
8. Харрис З.Л., Дерли А.П., Ман Т.К., Гитлин Д.Д. Целенаправленное разрушение генов выявляет существенную роль церулоплазмина в оттоке клеточного железа. Proc Natl Acad Sci U S A. 1999;96(19):10812-10817. (ПубМед)
9. Коно С. Ацерулоплазминемия. Curr Цели наркотиков. 2012;13(9):1190-1199. (ПубМед)
(ПубМед)
10. Теккерей Э.В., Сандерсон С.О., Фокс Дж.С., Кумар Н.Перегрузка печени железом или цирроз могут возникать при приобретенном дефиците меди и, вероятно, опосредованы гипоцерулоплазминемией. Дж. Клин Гастроэнтерол. 2011;45(2):153-158. (ПубМед)
11. Харрис ЭД. Медь. В: О’Делл Б.Л., Сунде Р.А., ред. Справочник по питательно необходимым минералам. Нью-Йорк: Марсель Деккер, Inc.; 1997: 231-273.
12. Джонсон М.А., Фишер Дж.Г., Кейс С.Е. Является ли медь антиоксидантным питательным веществом? Crit Rev Food Sci Nutr. 1992;32(1):1-31.
13. Мэтти М.Д., МакЭлви М.К., Фридман Дж.Х.Механизм активируемой медью транскрипции: активация AP-1, путей передачи сигнала JNK/SAPK и p38. Дж Мол Биол. 2008;383(5):1008-1018. (ПубМед)
14. Виде-Жибу Д., Беллиард С., Барду-Жаке Э. и соавт. Избыток железа, поддающийся лечению добавками меди при приобретенной ацерулоплазминемии: новая форма вторичной перегрузки железом у человека? Кровь. 2009;114(11):2360-2361. (ПубМед)
2009;114(11):2360-2361. (ПубМед)
15. Совет по пищевым продуктам и питанию, Медицинский институт. Медь. Референсные нормы потребления витамина А, витамина К, бора, хрома, меди, йода, железа, марганца, молибдена, никеля, кремния, ванадия и цинка.Вашингтон, округ Колумбия: Издательство Национальной академии; 2001: 224-257. (Издательство Национальной академии)
16. Го Ч., Ван КЛ. Влияние добавок цинка на соотношение меди и цинка в плазме, окислительный стресс и иммунологический статус у пациентов, находящихся на гемодиализе. Int J Med Sci. 2013;10(1):79-89. (ПубМед)
17. Милн Д.Б., Омайе С.Т. Влияние витамина С на метаболизм меди и железа у морской свинки. Int J Vitam Nutr Res. 1980;50(3):301-308. (ПубМед)
18. Финли Э.Б., Церклевски Ф.Л.Влияние добавок аскорбиновой кислоты на статус меди у молодых взрослых мужчин. Am J Clin Nutr. 1983;37(4):553-556. (ПубМед)
19. Джейкоб Р.А., Скала Дж. Х., Омайе С.Т., Тернлунд Дж.Р. Влияние различного потребления аскорбиновой кислоты на абсорбцию меди и уровень церулоплазмина у молодых мужчин. Дж Нутр. 1987;117(12):2109-2115. (ПубМед)
Х., Омайе С.Т., Тернлунд Дж.Р. Влияние различного потребления аскорбиновой кислоты на абсорбцию меди и уровень церулоплазмина у молодых мужчин. Дж Нутр. 1987;117(12):2109-2115. (ПубМед)
20. Харрис З.Л., Кломп Л.В., Гитлин Д.Д. Ацерулоплазминемия: наследственное нейродегенеративное заболевание с нарушением гомеостаза железа. Am J Clin Nutr.1998; 67 (5 Дополнение): 972S-977S. (ПубМед)
21. Бустос Р.И., Дженсен Э.Л., Руис Л.М. и соавт. Дефицит меди изменяет биоэнергетику клеток и вызывает слияние митохондрий за счет повышения регуляции MFN2 и OPA1 в эритропоэтических клетках. Biochem Biophys Res Commun. 2013;437(3):426-432. (ПубМед)
22. Пелед Т., Ландау Э., Прус Э., Тревес А.Дж., Наглер А., Фибах Э. Содержание меди в клетках модулирует дифференцировку и самообновление в культурах клеток CD34+, полученных из пуповинной крови. Бр Дж Гематол.2002;116(3):655-661. (ПубМед)
23. Лазарчик Дж. Новые данные об анемии и нейтропении при дефиците меди. Карр Опин Гематол. 2012;19(1):58-60. (ПубМед)
Карр Опин Гематол. 2012;19(1):58-60. (ПубМед)
24. Шоу Дж. К. Дефицит меди и неслучайная травма. Арч Дис Чайлд. 1988;63(4):448-455. (ПубМед)
25. Блэкмер А.Б., Бейли Э. Лечение дефицита меди у младенцев с холестатическим синдромом: обзор литературы и серия случаев. Нутр Клин Практ. 2013;28(1):75-86. (ПубМед)
26.Бест К., Маккой К., Джемма С., Дисильвестро Р.А. Активность фермента меди при муковисцидозе до и после приема добавок меди плюс или минус цинк. Метаболизм. 2004;53(1):37-41. (ПубМед)
27. Роуин Дж., Льюис С.Л. Медедефицитная миелоневропатия и панцитопения, вторичные по отношению к чрезмерному использованию добавок цинка. J Neurol Нейрохирург Психиатрия. 2005;76(5):750-751. (ПубМед)
28. Nations SP, Boyer PJ, Love LA, et al. Крем для зубных протезов: необычный источник избыточного цинка, приводящий к гипокупремии и неврологическим заболеваниям.Неврология. 2008;71(9):639-643. (ПубМед)
(ПубМед)
29. Prodan CI, Bottomley SS, Holland NR, Lind SE. Рецидивирующая гипокупремическая миелопатия, требующая заместительной терапии высокими дозами меди перорально. J Neurol Нейрохирург Психиатрия. 2006;77(9):1092-1093. (ПубМед)
30. Kumar N, Gross JB, Jr. Мутация в гене ATP7A может не быть причиной гипокупреемии при миелопатии с дефицитом меди. Postgrad Med J. 2006;82(968):416. (ПубМед)
31. Tumer Z. Обзор и обновление мутаций ATP7A, ведущих к болезни Менкеса и синдрому затылочного рога.Хум Мутат. 2013;34(3):417-429. (ПубМед)
32. Кодама Х., Фудзисава С., Бхадхпрасит В. Наследственные нарушения транспорта меди: биохимические механизмы, диагностика и лечение. Curr Drug Metab. 2012;13(3):237-250. (ПубМед)
33. Фокс П.Л., Мазумдер Б., Эренвальд Э., Мухопадхьяй К.К. Церулоплазмин и сердечно-сосудистые заболевания. Свободный Радик Биол Мед. 2000;28(12):1735-1744. (ПубМед)
34. Джонс А.А., ДиСильвестро Р.А., Коулман М., Вагнер Т.Л. Добавки меди у взрослых мужчин: влияние на активность ферментов меди в крови и показатели риска сердечно-сосудистых заболеваний.Метаболизм. 1997;46(12):1380-1383. (ПубМед)
Джонс А.А., ДиСильвестро Р.А., Коулман М., Вагнер Т.Л. Добавки меди у взрослых мужчин: влияние на активность ферментов меди в крови и показатели риска сердечно-сосудистых заболеваний.Метаболизм. 1997;46(12):1380-1383. (ПубМед)
35. Форд ЕС. Концентрация меди в сыворотке крови и ишемическая болезнь сердца у взрослых в США. Am J Эпидемиол. 2000;151(12):1182-1188. (ПубМед)
36. Малек Ф., Йиресова Е., Дохналова А., Копривова Х., Спасек Р. Медь в сыворотке как маркер воспаления в прогнозировании краткосрочного исхода у пациентов с высоким риском хронической сердечной недостаточности. Int J Кардиол. 2006;113(2):e51-53. (ПубМед)
37. Леоне Н., Курбон Д., Дюсиметьер П., Зурейк М.Цинк, медь и магний и риски смертности от всех причин, рака и сердечно-сосудистых заболеваний. Эпидемиология. 2006;17(3):308-314. (ПубМед)
38. Косар Ф., Шахин И., Ачикгоз Н., Аксой Ю., Кучукбай З., Чехрели С. Значение статуса микроэлементов в сыворотке крови у пациентов с ревматической болезнью сердца: проспективное исследование. Биол Трейс Элем Рез. 2005;107(1):1-10. (ПубМед)
Биол Трейс Элем Рез. 2005;107(1):1-10. (ПубМед)
39. Bertinato J, Zouzoulas A. Соображения по разработке биомаркеров медного статуса. J АОАС междунар.2009;92(5):1541-1550. (ПубМед)
40. Клевай Л.М. Сердечно-сосудистые заболевания из-за дефицита меди — история. Дж Нутр. 2000; 130 (2S Дополнение): 489S-492S. (ПубМед)
41. Милкарц Г., Ховард А.Н., Милкарц Б. и соавт. Лейкоцитарная медь, маркер статуса медного тела, низка при ишемической болезни сердца. J Трейс Элем Мед Биол. 2001;15(1):31-35. (ПубМед)
42. Родственник Г.Д., Ховард А.Н., Стоун Д.Л., Маллинз П.А. Исследования состояния меди и атеросклероза. Биохим Сок Транс.1990;18(6):1186-1188. (ПубМед)
43. Ван С.Л., Адачи Т., Сим А.С., Уилкен Д.Э. Уровни внеклеточной супероксиддисмутазы плазмы у австралийского населения с ишемической болезнью сердца. Артериосклеры Тромб Васк Биол. 1998;18(12):1915-1921. (ПубМед)
44. Клевай Л.М. Отсутствие рекомендуемой диетической нормы меди может быть опасным для вашего здоровья. J Am Coll Nutr. 1998;17(4):322-326. (ПубМед)
45. Милн Д.Б., Нильсен Ф.Х. Влияние диеты с низким содержанием меди на показатели состояния меди у женщин в постменопаузе.Am J Clin Nutr. 1996;63(3):358-364. (ПубМед)
46. Медейрос Д.М., Милтон А., Брюнетт Э., Стейси Л. Влияние добавок меди на показатели содержания меди и холестерина в сыворотке у взрослых мужчин. Биол Трейс Элем Рез. 1991;30(1):19-35. (ПубМед)
47. ДиСильвестро Р.А., Джозеф Э.Л., Чжан В., Раймо А.Е., Ким Ю.М. Рандомизированное исследование влияния добавок меди на активность ферментов меди в крови и параметры, связанные со здоровьем сердечно-сосудистой системы. Метаболизм. 2012;61(9):1242-1246.(ПубМед)
48. Терли Э., МакКаун А., Бонэм М.П. и др. Добавки меди у людей не влияют на восприимчивость липопротеинов низкой плотности к окислению, индуцированному in vitro (проект FOODCUE). Свободный Радик Биол Мед. 2000;29(11):1129-1134. (ПубМед)
49. Рок Э., Мазур А., О’Коннор Дж. М., Бонэм М. П., Райссигье И., Штрейн Дж. Дж. Влияние добавок меди на окисляемость эритроцитов и антиоксиданты плазмы у здоровых добровольцев среднего возраста. Свободный Радик Биол Мед.2000;28(3):324-329. (ПубМед)
50. Мансур М.А., Бергмарк С., Хасуэлл С.Дж. и соавт. Корреляция между общим гомоцистеином плазмы и медью у пациентов с заболеваниями периферических сосудов. Клин Хим. 2000;46(3):385-391. (ПубМед)
51. Челик С., Басту Э., Абали Р. и соавт. Взаимосвязь между медью, гомоцистеином и ранним сосудистым заболеванием у худых женщин с синдромом поликистозных яичников. Гинекол Эндокринол. 2013;29(5):488-491. (ПубМед)
52. Герхард Г.Т., Дуэлл П.Б.Гомоцистеин и атеросклероз. Карр Опин Липидол. 1999;10(5):417-428. (ПубМед)
53. Эмсли А.М., Джереми Дж.Ю., Гомес Г.Н., Анджелини Г.Д., Плейн Ф.
54. Шукла Н., Анджелини Г.Д., Джереми Дж.Ю. Интерактивные эффекты гомоцистеина и меди на ангиогенез в изолированной подкожной вене свиньи. Энн Торак Серг.2007;84(1):43-49. (ПубМед)
55. Утус Э.О., Ривз П.Г., Саари Дж.Т. Дефицит меди снижает уровень гомоцистеина в плазме у крыс. Дж Нутр. 2007;137(6):1370-1374. (ПубМед)
56. Wei H, Zhang WJ, McMillen TS, Leboeuf RC, Frei B. Хелирование меди тетратиомолибдатом ингибирует воспаление сосудов и развитие атеросклеротических поражений у мышей с дефицитом аполипопротеина Е. Атеросклероз. 2012;223(2):306-313. (ПубМед)
57. Файлла М.Л., Хопкинс Р.Г. Является ли низкий статус меди иммуносупрессивным? Нутр Рев.1998; 56 (1 часть 2): S59-64.
58. Персиваль СС. Медь и иммунитет. Am J Clin Nutr. 1998; 67 (5 Дополнение): 1064S-1068S. (ПубМед)
59. Heresi G, Castillo-Duran C, Munoz C, Arevalo M, Schlesinger L. Фагоцитоз и уровни иммуноглобулина у детей с гипокуремией. Нутр Рез. 1985; 5:1327-1334.
60. Келли Д.С., Дауду П.А., Тейлор П.С., Макки Б.Е., Тернлунд Дж.Р. Влияние диет с низким содержанием меди на иммунный ответ человека. Am J Clin Nutr. 1995;62(2):412-416. (ПубМед)
61.Ходжкинсон В., Петрис М.Дж. Гомеостаз меди на границе хозяин-патоген. Дж. Биол. Хим. 2012;287(17):13549-13555. (ПубМед)
62. Лукер А.С., Мелтон Л.Дж., 3-й, Харрис Т.Б., Борруд Л.Г., Шеперд Дж.А. Распространенность и тенденции низкой плотности бедренной кости среди пожилых людей в США: NHANES 2005–2006 по сравнению с NHANES III. Джей Боун Шахтер Рез. 2010;25(1):64-71. (ПубМед)
63. Тийдус П.М., Лоу Д.А., Браун М. Замена эстрогена и скелетные мышцы: механизмы и здоровье населения.J Appl Physiol. 2013;115(5):569-578. (ПубМед)
2013;115(5):569-578. (ПубМед)
64. Коли Дж. А. Влияние остеопороза на общественное здравоохранение. J Gerontol A Biol Sci Med Sci. 2013;68(10):1243-1251. (ПубМед)
65. Kanumakala S, Boneh A, Zacharin M. Лечение памидронатом улучшает минеральную плотность костей у детей с болезнью Менкеса. J Наследовать Metab Dis. 2002;25(5):391-398. (ПубМед)
66. Марквардт М.Л., Доун С.Л., Сандрок М., Бердон В.Е., Фельдман К.В. Дефицит меди проявляется метаболическим заболеванием костей у детей с экстремально низкой массой тела при рождении и коротким кишечником.Педиатрия. 2012;130(3):e695-698. (ПубМед)
67. Бейкер А., Харви Л., Майяск-Ньюман Г., Фэйрвезер-Тейт С., Флинн А., Кэшман К. Влияние потребления меди с пищей на биохимические маркеры костного метаболизма у здоровых взрослых мужчин. Eur J Clin Nutr. 1999;53(5):408-412. (ПубМед)
68. Бейкер А., Терли Э., Бонэм М.П. и соавт. Отсутствие влияния добавок меди на биохимические маркеры костного метаболизма у здоровых взрослых. Бр Дж Нутр. 1999;82(4):283-290. (ПубМед)
Бр Дж Нутр. 1999;82(4):283-290. (ПубМед)
69.Кэшман К.Д., Бейкер А., Гинти Ф. и др. Отсутствие влияния добавок меди на биохимические маркеры костного метаболизма у здоровых молодых взрослых женщин, несмотря на явно улучшенный статус меди. Eur J Clin Nutr. 2001;55(7):525-531. (ПубМед)
70. Конлан Д., Корула Р., Таллентир Д. Уровни меди в сыворотке у пожилых пациентов с переломами шейки бедра. Возраст Старение. 1990;19(3):212-214. (ПубМед)
71. Мутлу М., Аргун М., Килич Э., Сараймен Р., Язар С. Статус магния, цинка и меди у женщин с остеопорозом, остеопенией и нормальных женщин в постменопаузе.J Int Med Res. 2007;35(5):692-695. (ПубМед)
72. Итон-Эванс Дж., Меллврат Э.М., Джексон В.Е., Маккартни Х., Стрейн Дж.Дж. Добавки меди и поддержание минеральной плотности костей у женщин среднего возраста. J Trace Elem Exp Med. 1996;9:87-94.
73. Штрауз Л., Солтман П., Смит К.Т., Брекер М., Андон М. Б. Потеря костной массы позвоночника у женщин в постменопаузе, дополненная кальцием и микроэлементами. Дж Нутр. 1994;124(7):1060-1064. (ПубМед)
Б. Потеря костной массы позвоночника у женщин в постменопаузе, дополненная кальцием и микроэлементами. Дж Нутр. 1994;124(7):1060-1064. (ПубМед)
74. Нильсен Ф.Х., Лукаски Х.К., Джонсон Л.К., Ругхед З.К.Сообщаемое потребление цинка, но не меди, влияет на плотность костей всего тела, содержание минералов и реакцию Т-балла на добавки цинка и меди у здоровых женщин в постменопаузе. Бр Дж Нутр. 2011;106(12):1872-1879. (ПубМед)
75. Sidiropoulou-Chatzigiannis S, Kourtidou M, Tsalikis L. Влияние остеопороза на состояние пародонта, альвеолярную кость и ортодонтическое движение зубов. Обзор литературы. J Int Acad Periodontol. 2007;9(3):77-84. (ПубМед)
76. Дарси Дж., Хорнер К., Уолш Т., Саузерн Х., Марьянович Э.Дж., Девлин Х.Потеря зубов и остеопороз: для оценки связи между статусом остеопороза и количеством зубов. Бр Дент Дж. 2013;214(4):E10. (ПубМед)
77. Серпинска Т., Константинович Дж., Оривал К., Голебевская М. , Шмитковски М. Дефицит меди как потенциальный патогенный фактор снижения минеральной плотности костей и сильной стираемости зубов. Остеопорос Инт. 2013 [Epub перед печатью]. (ПубМед)
, Шмитковски М. Дефицит меди как потенциальный патогенный фактор снижения минеральной плотности костей и сильной стираемости зубов. Остеопорос Инт. 2013 [Epub перед печатью]. (ПубМед)
78. Сквитти Р., Барбати Г., Росси Л. и соавт. Избыток нецерулоплазминовой меди в сыворотке крови при БА коррелирует с MMSE, [β]-амилоидом в спинномозговой жидкости и h-τ.Неврология. 2006;67(1):76-82. (ПубМед)
79. Арнал Н., Кристалли Д.О., де Аланиз М.Дж., Марра К.А. Клиническая полезность определения содержания меди, церулоплазмина и металлотионеина в плазме у пациентов с нейродегенеративными заболеваниями и их ближайших родственников. Мозг Res. 2010;1319:118-130. (ПубМед)
80. Ventriglia M, Bucossi S, Panetta V, Squitti R. Медь при болезни Альцгеймера: метаанализ исследований сыворотки, плазмы и спинномозговой жидкости. Дж. Альцгеймера Дис. 2012;30(4):981-984.(ПубМед)
81. Брюэр Г.Дж. Избыток меди, дефицит цинка и потеря когнитивных функций при болезни Альцгеймера. Биофакторы. 2012;38(2):107-113. (ПубМед)
Биофакторы. 2012;38(2):107-113. (ПубМед)
82. Сквитти Р., Полиманти Р. Медный фенотип при болезни Альцгеймера: анализ пути. Am J Нейродегенер Дис. 2013;2(2):46-56. (ПубМед)
83. Squitti R, Polimanti R. Медная гипотеза об отсутствии наследственности спорадической болезни Альцгеймера: ген ATP7B как потенциальное убежище для редких вариантов.Дж. Альцгеймера Дис. 2012;29(3):493-501. (ПубМед)
84. Спаркс Д.Л., Шреурс Б.Г. Следовые количества меди в воде вызывают образование β-амилоидных бляшек и дефицит обучаемости у кроликов, моделирующих болезнь Альцгеймера. Proc Natl Acad Sci USA. 2003;100(19):11065-11069. (ПубМед)
85. Китадзава М., Ченг Д., Лаферла Ф.М. Хроническое воздействие меди усугубляет как амилоидную, так и тау-патологию и избирательно нарушает регуляцию cdk5 в мышиной модели AD. Дж. Нейрохим. 2009;108(6):1550-1560. (ПубМед)
86.Моррис М.С., Эванс Д.А., Тангни К.С. и др. Диетическая медь и высокое потребление насыщенных и транс-жиров связаны со снижением когнитивных функций. Арх Нейрол. 2006;63(8):1085-1088. (ПубМед)
Диетическая медь и высокое потребление насыщенных и транс-жиров связаны со снижением когнитивных функций. Арх Нейрол. 2006;63(8):1085-1088. (ПубМед)
87. Кесслер Х., Пайонк Ф.Г., Бах Д. и соавт. Влияние потребления меди на параметры спинномозговой жидкости у пациентов с легкой формой болезни Альцгеймера: пилотное клиническое исследование фазы 2. J Neural Transm. 2008;115(12):1651-1659. (ПубМед)
88. Кесслер Х., Байер Т.А., Бах Д. и соавт. Потребление меди не влияет на когнитивные функции у пациентов с легкой формой болезни Альцгеймера: пилотное клиническое исследование фазы 2.J Neural Transm. 2008;115(8):1181-1187. (ПубМед)
89. Skjorringe T, Moller LB, Moos T. Нарушение взаимосвязанных механизмов гомеостаза железа и меди в головном мозге способствует патогенезу нейродегенеративных заболеваний. Фронт Фармакол. 2012;3:169. (ПубМед)
90. Акацу Х., Хори А., Ямамото Т. и др. Аномалии переходных металлов при прогрессирующей деменции. Биометаллы. 2012;25(2):337-350. (ПубМед)
Биометаллы. 2012;25(2):337-350. (ПубМед)
91. Мариани С., Вентрилья М., Симонелли И. и соавт.Fe и Cu не различаются при болезни Паркинсона: повторное исследование плюс метаанализ. Нейробиол Старение. 2013;34(2):632-633. (ПубМед)
92. Хендлер С.С., Рорвик Д.Р., ред. PDR для пищевых добавок. Montvale: Медицинская экономическая компания, Inc; 2001.
93. Бремнер И. Проявления избытка меди. Am J Clin Nutr. 1998; 67 (5 Дополнение): 1069S-1073S. (ПубМед)
94. Фитцджеральд Д.Дж. Правила безопасности для меди в воде. Am J Clin Nutr. 1998; 67 (5 Дополнение): 1098S-1102S.(ПубМед)
95. Turnlund JR, Jacob RA, Keen CL, et al. Долгосрочное высокое потребление меди: влияние на показатели статуса меди, антиоксидантного статуса и иммунной функции у молодых мужчин. Am J Clin Nutr. 2004;79(6):1037-1044. (ПубМед)
96. Тернлунд Дж. Р., Киз В. Р., Ким С. К., Домек Дж. М. Долгосрочное высокое потребление меди: влияние на абсорбцию, удержание и гомеостаз меди у мужчин.
